Definición y etiopatogeniaArriba
La polimiositis (PM) es una miopatía inflamatoria crónica, adquirida e idiopática. La dermatomiositis (DM) es una forma de miopatía inflamatoria asociada con dermatitis. En ambas enfermedades los cambios inflamatorios pueden afectar al corazón, al intersticio pulmonar y a los vasos sanguíneos.
La etiología es desconocida. Se cree que en la etiopatogenia de la PM/DM los mecanismos autoinmunes desempeñan un papel esencial.
Recientemente se ha distinguido un nuevo subtipo clínico e histopatológico de miopatía inflamatoria, denominado miopatía necrotizante autoinmune →Diagnóstico diferencial.
Cuadro clínico e historia naturalArriba
La PM y la DM son las miopatías inflamatorias idiopáticas más comunes en adultos. Las mujeres enferman 2 veces más a menudo que los hombres. La enfermedad puede ocurrir a cualquier edad, si bien hay un pico de incidencia entre los 10-15 años de edad (forma juvenil) y otro entre los 35-65 años. El inicio puede ser agudo (días), subagudo (semanas) o crónico (meses, años). La mayoría de los enfermos no tratados evoluciona lentamente a la atrofia y contractura muscular. La mortalidad a los 5 años ~50 %. La asociación con una neoplasia maligna en la DM es 6 y en la PM 2 veces más probable (existe un incremento del riesgo para el cáncer de: ovario, mama, pulmón, estómago, intestino, fosa nasal y faringe, páncreas, vejiga y también de linfoma no Hodgkin).
1. Síntomas generales: debilidad, aumento de la temperatura corporal y pérdida de peso.
2. Síntomas de afectación muscular:
1) debilidad muscular generalmente simétrica y localizada en cintura escapular, cintura pélvica y también cuello y espalda (casi en todos los enfermos), lo que origina problemas al incorporarse de una posición sentada, levantar objetos pesados, peinarse, subir escaleras, etc.; los músculos están a menudo dolorosos y sensibles
2) debilidad de los músculos respiratorios, que provoca insuficiencia respiratoria
3) debilidad de los músculos de faringe, esófago y laringe, que provoca disfagia y disfonía
4) compromiso de los músculos oculares (raro): nistagmo, visión borrosa.
3. Manifestaciones cutáneas: ocurren en la DM. Su aparición y gravedad no siempre se correlacionan con afectación muscular, ya que pueden preceder a la miositis o aparecer solos (CADM, dermatomiositis sine miositis). A menudo los cambios eritematosos se acompañan de prurito y/o sensibilidad a la luz solar.
1) Eritema alrededor de los ojos de color violáceo y en forma de gafas (→fig. 17.6-1), (eritema en heliotropo periorbitario), a veces con edema de párpados (signo patognomónico), y que aparece en un 30-60 % de los enfermos; eritema de escote en forma de V; además eritema de cuello y hombros (signo de mantón), eritema en la superficie lateral de caderas y muslos (signo de pistolera).
2) Pápulas de Gottron: pápulas eritematovioláceas, hiperqueratósicas, localizadas en la superficie extensora de las articulaciones (más frecuentemente interfalángicas y metacarpofalángicas →fig. 1.8-5; y a veces de muñecas, codos, rodillas y tobillos); el signo de Gottron hace referencia a las manchas eritematosas o violáceas que aparecen en la misma localización (signos patognomónicos; en ~70 % de los enfermos).
3) Otros: engrosamiento, descamación y agrietamiento de la piel en las puntas de los dedos y el lado palmar de las manos (denominadas manos de mecánico, raramente); eritema con edema, petequias y telangiectasias en el área de lechos ungueales, úlceras tróficas como resultado de la coexistencia de vasculitis cutánea, eritrodermia generalizada, inflamación del tejido subcutáneo (paniculitis), livedo reticular, alopecia focal que no deja cicatrices.
PERSPECTIVA LATINOAMERICANA
En pacientes con tono de piel moderadamente oscuro existen los signos de la quemadura solar, como exantema rojo brillante en frente, mejillas, nariz y mentón (áreas de promiencia ósea), y del bronceado solar (hiperpigmentación café-grisácea con descamación en las mismas áreas) que ayudan en el diagnóstico de dermatomiositis. Fueron descritos en México en 2020.
4. Manifestaciones cardíacas: aparecen en un 70 % de los casos, por lo general taquicardia o bradicardia, raramente síntomas de insuficiencia cardíaca.
5. Cambios pulmonares: síntomas de enfermedad pulmonar intersticial (en un 30-40 %), principalmente tos seca y disnea progresiva, que progresan a insuficiencia respiratoria crónica. Neumonía por aspiración en enfermos con disfagia.
6. Cambios en el sistema digestivo: síntomas de alteración de la motilidad de esófago, estómago e intestinos, incluyendo reflujo gastroesofágico. En casos graves ulceraciones y hemorragia.
7. Cambios articulares: síntomas de artritis sin erosiones o dolor articular, en especial periférico, principalmente en las articulaciones de la mano (en un 20-50 %).
8. Calcificaciones: en el tejido subcutáneo, músculos esqueléticos, tendones y fascias (en >10 %), a veces masivas.
9. Fenómeno de Raynaud (en un 10-15 %).
DiagnósticoArriba
Exploraciones complementarias
1. Pruebas de laboratorio
1) Análisis de sangre. Aumento de los niveles de las enzimas musculares en suero: CK, AST, ALT, LDH, aldolasa (la actividad normal no excluye PM/DM), aumento de la concentración de mioglobina, aumento de la VHS, aumento de la concentración de proteína C-reactiva y de las gammaglobulinas en el suero.
2) Pruebas inmunológicas: autoanticuerpos AAN (en un 40-80 %), incluyendo anticuerpos específicos de PM/DM (antisintetasa aminoacil-tRNA [más frecuentemente anti-Jo-1], anti-SRP y anti-Mi-2) y anticuerpos asociados (anti-Ro, anti-La, anti-U1-RNP, anti-U2-RNP, anti-Ku, anti-Sm, anti-PM/Scl).
2. Electromiografía: muestra signos de daño muscular primario.
3. Examen histológico
1) biopsia de músculo: muestra la presencia de un infiltrado inflamatorio, principalmente con linfocitos. El tipo de células, las estructuras afectadas y la aparición de atrofia perifascicular dependen de la forma de la enfermedad
2) biopsia de pulmón (quirúrgica): puede revelar enfermedad pulmonar intersticial (varias formas).
4. Pruebas de imagen En la RMN de músculos: aumento de la señal en secuencias potenciadas T1 y T2. Las más sensibles para la detección de inflamación activa son las imágenes potenciadas en T2 con supresión de tejido adiposo o secuencias STIR, pero los cambios no son patognomónicos para PM/DM. El estudio permite facilitar la elección de una ubicación óptima para la biopsia muscular. En la radiografía y la TC de alta resolución de tórax pueden observarse cambios intersticiales. La radiografía de huesos y articulaciones puede revelar numerosas calcificaciones, principalmente en el tejido subcutáneo y músculos y también osteoporosis.
5. ECG: por lo general se observan cambios no específicos del segmento ST y de la onda T, taquicardia sinusal y raramente bloqueo AV I o II.
Criterios diagnósticos
El diagnóstico se establece sobre la base de los síntomas y signos clínicos, que especialmente incluyen debilidad muscular de localización y curso típicos, así como por la presencia de lesiones cutáneas características en asociación con los resultados del examen histológico de los músculos y de la electromiografía. Pueden ser útiles los criterios diagnósticos propuestos por Bohan y Peter →tabla 17.6-1. Criterios de clasificación de miopatías inflamatorias según EULAR/ACR →tabla 17.6-2. Dichos criterios no deben utilizarse para determinar el diagnóstico, sino para diferenciar miositis idiopáticas de otras enfermedades sistémicas del tejido conectivo.
Diagnóstico diferencial
1) Miopatías inflamatorias idiopáticas distintas de una PM/DM: principalmente inflamación muscular en el curso de otras enfermedades sistémicas del tejido conectivo (síndromes de superposición), miositis asociada a cáncer, miopatía necrótica autoinmune (clínicamente se parece a la PM, a menudo está asociada con una enfermedad sistémica del tejido conjuntivo, una infección viral [p. ej. VIH], anticuerpos anti-SRP, una terapia con estatinas o un cáncer; en cualquier caso se caracteriza por la ausencia de la típica infiltración de células mononucleares en el examen histológico, por lo general responde bien a inmunosupresores); miositis por cuerpos de inclusión (predomina debilidad muscular distal, a veces asimétrica, no hay cambios de la piel), miositis con eosinofilia, miositis focal (tumor doloroso frecuentemente situado en la extremidad inferior, el inicio en general es agudo, sin traumatismo previo, en un 90 % desaparece sin tratamiento), miositis de los músculos oculomotores.
2) Enfermedades con daños musculares secundarios o debilidad muscular →tabla 17.6-3. Buscar neoplasia maligna.
TratamientoArriba
Tratamiento farmacológico
1. Glucocorticoides: prednisona VO 1 mg/kg/d (máx. 80 mg/kg); inicio agudo o evolución más grave → inicialmente se puede utilizar metilprednisolona iv. 0,5-1,0 g durante 3 días. Después de la mejoría (normalización de marcadores de daño muscular, aumento de la fuerza muscular), pero no antes de 4-8 semanas desde el inicio del tratamiento, reducir la dosis diaria del glucocorticoide oral gradualmente, p. ej. en un 25 % o ~10 mg/mes, hasta alcanzar una dosis de mantenimiento de 5-10 mg/d y continuar el tratamiento durante varios años, a veces durante toda la vida. Algunos recomiendan la reducción de la dosis en 5 mg cada semana hasta 20 mg/d, luego en 2,5 mg cada 2 semanas hasta 10 mg/d, y finalmente en 1 mg cada mes hasta la retirada del fármaco.
2. Si dentro del plazo de 6 semanas desde el inicio del tratamiento no hay una mejoría satisfactoria o si el curso de la enfermedad es rápido → añadir uno de los fármacos enumerados más adelante (preparados →tabla 17.1-6). Metotrexato VO o por vía parenteral (IM o VSc) 1 × semana, con ácido fólico o folínico; empezar, dependiendo de la gravedad de la enfermedad, con dosis desde 10-15 mg 1 × semana; si los síntomas no mejoran, aumentar gradualmente en 5 mg cada 2-3 meses o más rápidamente. Azatioprina 1,5-2 mg/kg/d, reducir la dosis en 25 mg cada mes a una dosis de mantenimiento de 50 mg/d; el efecto terapéutico se revela después de >3 meses. Ciclosporina a dosis de 2,5-5 mg/kg/d. Ciclofosfamida a dosis de 1,0 g iv. 1 × mes, eventualmente 1-3 mg/kg 1 ×d VO Generalmente se utiliza en caso de enfermedad pulmonar intersticial o vasculitis grave. Micofenolato de mofetilo 2-3 g/d, en caso de ineficacia o intolerancia a metotrexato y ciclosporina. Hidroxicloroquina 200 mg 2 × d o cloroquina 250 mg 2 × d, indicados en lesiones refractarias de la piel. IGIV: indicada en caso de ineficacia de la terapia inmunosupresora; 0,4 g/kg/d durante 5 días consecutivos 1 × mes, durante 3-7 meses consecutivos. Rituximab 750 mg/m2 de la sc. (máx. 1 g) 2 veces con un intervalo de 2 semanas. En casos refractarios a terapia inmunosupresora se hacen intentos con el uso de tacrolimus y fármacos anti-TNF.
Rehabilitación
Para la recuperación de la fuerza es importante la kinesioterapia. En la fase aguda de la enfermedad utilizar principalmente ejercicios pasivos para prevenir contracturas, y durante la recuperación ejercicios isométricos y activos con gravedad minimizada, después los ejercicios isotónicos y aeróbicos. Los ejercicios en el agua son muy beneficiosos. El ejercicio físico durante este período no debe superar el 60 % del consumo máximo de oxígeno.
ObservaciónArriba
Evaluación periódica de la fuerza muscular (p. ej. mediante MMT-8), niveles séricos de CK, EMG. En enfermos con enfermedad pulmonar intersticial: TC de alta resolución, pruebas de función pulmonar y test de la marcha de 6 min. Es importante la vigilancia oncológica debido al aumento del riesgo de aparición de neoplasias malignas, que es mayor durante los primeros 3 años desde el diagnóstico de la PM/DM, y que persiste incluso después de 5 los años de este diagnóstico. El riesgo de cáncer aumenta, entre otros, por: edad >50 años, DM, lesiones graves de la piel, presencia de anti-155/140 kD, falta de anticuerpos asociados o combinados con la PM/DM.
PronósticoArriba
Con el tratamiento adecuado la supervivencia a los 10 años es >80 %. Factores de mal pronóstico son p. ej. la edad avanzada, compromiso de órganos internos, especialmente pulmones, coexistencia de un tumor maligno y presencia de anticuerpos anti-SRP.
TABLAS Y FIGURASArriba
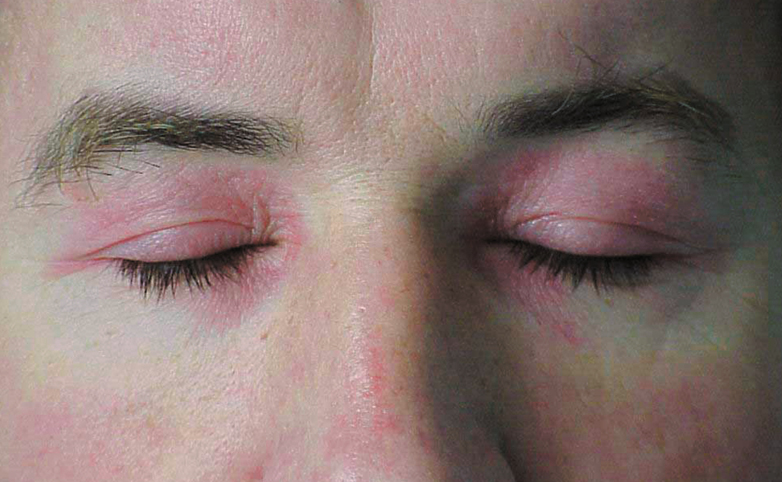
Fig. 17.6-1. PM/DM. Eritema en heliotropo periorbitario
Tabla 17.6-1. Criterios diagnósticos de polimiositis (PM) y de dermatomiositis (DM) según Bohan y Peter
|
1) Debilidad simétrica y progresiva de los músculos de la cintura escapular y pélvica.
2) Hallazgos histológicos característicos de la miositis.
3) Aumento de la actividad de CK o aldolasa en suero.
4) Características electromiográficas de daño muscular primario. |
|
Diagnóstico |
Cierto |
Probable |
Posible |
|
Número de signos |
|
PM |
4 |
3 |
2 |
|
DM |
3 o 4 |
2 |
1 |
|
y lesiones cutáneas característicasa |
|
a Signo de Gottron, eritema en heliotropo de los párpados, eritema de escote o brazos. |
Tabla 17.6-2. Criterios de clasificación de miopatías inflamatorias idiopáticas según EULAR/ACR (2017)
|
Característica/síntoma o signo |
Ejemplo (definición) |
Puntuación |
|
|
Con biopsia |
Sin biopsia |
|
Edad de inicio de los síntomas |
≥18 años y <40 años |
1,5 |
1,3 |
|
≥40 años |
2,2 |
2,1 |
|
Debilidad muscular |
– debilidad de los músculos proximales de los miembros superiores (simétrica, normalmente progresiva)a |
0,7 |
0,7 |
|
– debilidad de los músculos proximales de los miembros inferiores (simétrica, normalmente progresiva)a |
0,5 |
0,8 |
|
– los músculos flexores del cuello son relativamente más débiles que los extensoresa |
1,6 |
1,9 |
|
– los músculos proximales de los miembros inferiores son relativamente más débiles que los distalesa |
1,2 |
1,9 |
|
Signos cutáneos |
– eritema en heliotropob (→fig. 17.6-1) |
3,2 |
3,1 |
|
– pápulas de Gottronc |
2,7 |
2,1 |
|
– signo de Gottrond |
3,7 |
3,3 |
|
Otros síntomas y signos clínicos |
Trastornos de la deglución o de la motilidad esofágica |
0,6 |
0,7 |
|
Pruebas de laboratorio |
– anticuerpos anti-Jo-1 (resultado positivo de una prueba realizada con un método estandarizado y aceptado) |
3,8 |
3,9 |
|
– aumento de la actividad sérica de CK, AST, ALT, LDH (el valor más alto en el transcurso de la enfermedad) |
1,4 |
1,3 |
|
Biopsia muscular |
– infiltrados de células mononucleares en el epimisio que rodean las fibras musculares, sin penetrarlas |
1,7 |
– |
|
– infiltrados de células mononucleares en el perimisio y/o fascículos vasculares (en el perimisio o epimisio) |
1,2 |
– |
|
– atrofia perifascicular (las células que aparecen dispuestas en varias filas alrededor de los fascículos vasculares y nerviosos son visiblemente más pequeñas que las células de ubicación más central) |
1,2 |
– |
|
– vacuolas ribeteadas (se tiñen de azul en tinción hematoxilina-eosina y de rojo en tinción de Gomori modificada) |
3,1 |
– |
|
a En el examen físico o a través de otra medición
b Eritema alrededor de los ojos de color violáceo, a veces con edema palpebral
c Pápulas eritematosas o violáceas, hiperqueratósicas, localizadas en la superficie extensora de las articulaciones, más frecuentemente interfalángicas y metacarpofalángicas; también pueden presentarse en muñecas, codos, rodillas y tobillos
d Manchas eritematosas o violáceas en la misma localización que las pápulas.
Nota: los criterios de clasificación pueden utilizarse cuando no hay otra causa que explique la sintomatología. El diagnóstico se considera seguro (probabilidad de ≥90 %) si el resultado es de ≥8,7 con biopsia o de ≥7,5 sin biopsia y es probable (≥55 %) cuando el resultado es de, respectivamente, ≥6,7 y ≥5,5.
ALT — alanina-aminotransferasa, AST — aspartato-aminotransferasa, CK — creatina-cinasa, LDH — lactato deshidrogenasa
A partir de: Arthritis Rheum., 2017, 69: 2271-2282; modificado |
Tabla 17.6-3. Enfermedades y agentes que dañan los músculos, o que causan síntomas del daño muscular
|
Enfermedades del sistema endocrino |
Síndrome de Cushing, hipotiroidismo, hipertiroidismo, hiperparatiroidismo e hipoparatiroidismo |
|
Trastornos metabólicos |
Deficiencia de carnitina, trastorno metabólico de vitamina A, glucogénesis |
|
Enfermedades del sistema nervioso |
Distrofias musculares genéticas, neuropatía proximal, síndrome de Lambert-Eaton, miastenia grave, esclerosis lateral amiotrófica |
|
Infecciones |
Virales, bacterianas, parasitarias (toxoplasmosis, triquinosis) |
|
Trastornos electrolíticos |
Reducción o aumento de la concentración plasmática de: sodio, potasio, calcio, magnesio y fosfato |
|
Enfermedades granulomatosas |
Sarcoidosis |
|
Fármacos |
Amiodarona, quinidina, cimetidina, ciclosporina, danazol, D-penicilamina, interferón-α, interleucina-2, colchicina, ácido ε-aminocaproico, fenilbutazona, fenitoína, glucocorticoides, hidralazina, carnitina, hipolipemiantes (fibratos, estatinas, ácido nicotínico), antimaláricos (cloroquina e hidroxicloroquina), levodopa, penicilina, procainamida, rifampicina, sulfonamidas, L-triptófano, ácido valproico, vincristina, zidovudina |
|
Sustancias tóxicas |
Monóxido de carbono, alcohol, heroína, cocaína |
|
Factores físicos |
Descarga eléctrica, traumatismo, hipertermia |
Tabla 17.1-6. Fármacos modificadores de la enfermedad (FARME) utilizados en la AR
|
Fármaco |
Dosificación |
Contraindicaciones |
Efectos adversos |
Observación |
|
Convencionales sintéticos (csFARME) |
|
Cloroquina
|
VO 250 mg 1 × d |
Enfermedades de la retina, alteraciones visuales, insuficiencia renal, porfiria, psoriasis, deficiencia de glucosa-6-fosfato deshidrogenasa, hepatitis B o C no tratada con insuficiencia hepática en clase C de Child-Pugh |
Daño retiniano (de la mácula lútea), especialmente “en ojo de buey”; exantema; dolor abdominal, diarrea, pérdida de apetito, náuseas; otros, muy raros, como miopatía, visión borrosa, trastornos de acomodación, cambios en la pigmentación de la piel y de las membranas mucosas, neuropatía periférica, miocardiopatía |
Examen oftalmológico con campimetría y tomografía de coherencia óptica de dominio espectral (SD-OCT) al inicio y, si no hay factores de riesgo de retinopatíaa, después de 5 años y luego una vez al año. Por ficha técnica, se debe realizar el examen oftalmológico (oftalmoscopia y campimetría) antes del tratamiento, posteriormente cada 3-4 meses y ante la aparición de cualquier alteración visual. |
|
Hidroxicloroquina |
VO 200 mg 1-2 × d
(≤5,0 mg/kg/d) |
Véase más arriba; aceptable en casos seleccionados con hepatitis B activa |
Véase más arriba; el riesgo de lesión ocular es muy bajo en los primeros 5-7 años del tratamiento (es mayor en casos de edad avanzada, enfermedad renal, antecedentes de retinopatía) |
Examen oftalmológico con campimetría y tomografía de coherencia óptica de dominio espectral (SD-OCT) al inicio y, si no hay factores de riesgo de retinopatíaa, después de 5 años y posteriormente una vez al año. No requiere pruebas rutinarias de laboratorio |
|
Ciclosporina
|
VO 2,5 mg/kg/d dividida en 2 dosis cada 12 h, y luego incrementar en 0,5 mg/ kg/d cada 2-4 semanas hasta obtener mejoría clínica o hasta una dosis total de 5 mg/kg/d |
Insuficiencia renal; hipertensión arterial; infecciones crónicas |
Insuficiencia renal; hipertensión arterial; anemia; vellosidad excesiva, hirsutismo en mujeres; trastornos de la sensibilidad; hiperplasia gingival; inmunodeficiencia con riesgo aumentado de infecciones
Nota: muchos medicamentos interfieren con la ciclosporina, lo que aumenta el riesgo de efectos adversos |
ECG al inicio; presión arterial y glucemia durante cada visita; creatinina en el suero cada 2 semanas hasta establecer la dosis, después cada mes; la disfunción renal causada por ciclosporina es reversible en gran medida, pero no completamente; hemograma, ALT y AST, albúmina (como más adelante): considerar la monitorización de la concentración sérica del fármaco |
|
Leflunomida
|
VO 20 mg 1 × d |
Infecciónb; leucopenia <3000/µl; trombocitopenia <50 000/µl; mielodisplasia; neoplasia linfoproliferativa tratada en los últimos ≤5 años; daño hepáticoc,d,e; embarazo y lactancia; disfunción renal grave o moderada |
Diarrea, dolor abdominal, náuseas; exantema; alopecia; daño hepático; daño renal; aumento de presión arterial; efecto teratogénico (se necesita un método anticonceptivo eficaz); en el caso de complicaciones posteriores a la interrupción de la administración del fármaco puede acelerarse su eliminación mediante la colestiramina (8 g 3 × d durante 11 días) o carbón activado (50 g 4 × d durante 11 días); en mujeres que desean quedarse embarazadas y en hombres que planean paternidad deben medirse repetidamente las concentraciones del metabolito de leflunomida de eliminación acelerada |
Hemograma, concentración de creatinina/TFGe, ALT y AST, albúmina: cada 2 semanas hasta establecer una dosis fija durante 6 semanas, a continuación cada mes durante 3 meses, luego por lo menos cada 12 semanas; con mayor frecuencia en enfermos con mayor riesgo de toxicidad; en el caso de un aumento sostenido de ALT/AST >3 × LSN hay que suspender el fármaco y considerar la biopsia hepática para evaluar daños; presión arterial y peso corporal durante cada visita |
|
Metotrexato
|
VO, IM o Vsc 10-15 mg 1 × semana, la dosis se aumenta gradualmente hasta un máx. de 25-30 mg; administración concomitantef de ácido fólico (≥5 mg/semana) o de ácido folínico con el fin de evitar los efectos adversos (citopenia, úlceras orales y náuseas) |
Véase más arriba + neumonía intersticial/fibrosis pulmonar g; aclaramiento de creatinina <30 ml/min |
Aumento de la actividad de las enzimas hepáticas en el suero, fibrosis y cirrosis hepática (muy raramente); factores de riesgo: falta de suplementación del ácido fólico, esteatohepatitis no alcohólica, sexo masculino, hiperlipidemia no tratada, creatininemia aumentada, consumo de alcohol, obesidad, diabetes, hepatitis B y C; citopenia debida a la supresión de la médula ósea y a sus complicaciones (dependiendo de la dosis); úlceras orales, incidencia de un 30 %; náuseas a las 24-48 h de la ingesta; cambios intersticiales pulmonares, frecuencia de un 2-6 %, independientemente del tiempo de tratamiento y de la dosis de metotrexato; efecto teratogénico: se necesita un método anticonceptivo eficaz; el metotrexato debe retirarse (hombre y mujer) tres meses antes de un intento de concebir. Efectos más leves (por falta de ácido fólico): mucositis, alopecia, trastornos del tracto digestivo |
Véase más arriba + prueba de la función pulmonar y radiografía de tórax antes del tratamiento (vigente desde el año anterior) y durante el tratamiento, si se desarrolla tos o disnea |
|
Sulfasalazina |
VO 1 g 2 × d (óptimamente 3-4 g/d, la dosis debe aumentarse gradualmente); simultáneamente la administración de ácido fólico (5 mg/semana) o de ácido folínico |
Hipersensibilidad a sulfonamidas y a salicilatos; casos de ileostomía; daño hepáticoc,d,h; insuficiencia renal; porfiria; deficiencia de glucosa-6-fosfato deshidrogenasa |
La mayoría de los efectos adversos se produce en los primeros meses de tratamiento: se pueden evitar al comenzar con una dosis baja e incrementar gradualmente; pérdida de apetito, dispepsia, náuseas, vómitos, dolor abdominal (frecuencia de un 30 %); cefaleas y mareos; fiebre; reacciones alérgicas de la piel (urticaria, hipersensibilidad a la luz solar) y de las articulaciones; anemia hemolítica (en enfermos con deficiencia de glucosa-6-fosfato deshidrogenasa en eritrocitos), anemia aplásica esporádica; granulocitopenia (1-3 %), puede ocurrir en cualquier momento del tratamiento (por lo general en los primeros 3 meses); un aumento de actividad de ALT/AST en el suero; cambios intersticiales pulmonares raramente |
Hemograma, ALT/AST, creatinina/eTFG séricas: véase más arriba; no se requieren nuevos controles pasados 12 meses, si el estado clínico es estable |
|
Puntuales sintéticos (psFARME) |
|
Tofacitinib
Baricitinib
Upadacitinib
Filgotinib |
5 mg 2 × d (5 mg 1 × d en enfermos con insuficiencia hepática en clase B de Child-Pugh o con aclaramiento de creatinina <30 ml/min)
2-4 mg 1 × d (2 mg/d en enfermos ≥75 años, con aclaramiento de creatinina 30-60 ml/min e infecciones crónicas o recurrentes, tratados con probenecid)
15 mg 1 × d
200 mg 1 × d (100 mg 1 × d en enfermos ≥75 años o con aclaramiento de creatinina 15-60 ml/min) |
– infecciones activas o crónicas graves (también locales)
– recuento de linfocitos <500/µli
– recuento de neutrófilos <1000/µl
– concentración de hemoglobina <8 g/dlj
– insuficiencia hepática grave (clase C de Child-Pugh)
– neoplasia activa
– episodios tromboembólicos recurrentes (si no hay anticoagulación)
– embarazo y lactancia (en caso de planificar procreación se recomienda un intervalo de 4 semanas desde la última dosis)
– en enfermos >65 años utilizar tofacitinib solo si no hay otra alternativa
|
– infecciones, también oportunistas
– reactivación de infecciones virales (especialmente de varicela y herpes zóster)
– eventos tromboembólicos en enfermos con factores de riesgo de trombosis
– linfopenia, neutropenia, anemia
– hiperlipidemia |
Antes del tratamiento: como en fármacos biológicos; durante el tratamiento, entre otros:
– hemograma de sangre periférica con fórmula leucocitaria, AST/ALT y creatinina con TFGe (al inicio, después de 4 y 12 semanas de tratamiento y luego cada 3 meses)
– lipidograma al inicio y después de 3 meses de tratamiento
– evaluación para detectar cáncer de piel no melanoma antes de iniciar la terapia y cada año durante el tratamiento |
|
Biológicos (bFARME) |
|
Abatacept
|
infusión iv. 30 min; <60 kg — 500 mg, 60-100 kg — 750 mg, >100 kg — 1 g; las dosis posteriores a las 2 y 4 semanas de la primera infusión, y luego cada 4 semanas |
Infecciones b; hepatitis viralesd,h, embarazo y lactancia |
Infecciones graves (incluidas oportunistas); probablemente leucoencefalopatía multifocal progresiva (muy raramente) |
Antes del tratamiento: radiografía de tórax y test de tuberculina/test IGRA, hemograma, ALT/AST, creatinina sérica, pruebas de hepatitis; se recomienda la vacunación contra: neumococo (periódicamente), gripe (anualmente), hepatitis B (si existen factores de riesgo); vacunas vivas contraindicadas; durante el tratamiento vigilar los síntomas de infección; en mujeres indicación de mamografía antes del tratamiento |
|
Adalimumab
|
VSc 20-40 mg cada 1 o 2 semanas |
Infecciones crónicas, véase más arriba + insuficiencia cardíaca (NYHA III o IV y FEVI ≤50 %); esclerosis múltiple u otra enfermedad desmielinizante; neoplasia linfoproliferativa tratada en los últimos ≤5 años k |
Infecciones graves (incluyendo oportunistas); formación de autoanticuerpos, incluyendo: ANA, Anti-dsDNA, anticardiolipinas y antiquimeras; raras veces se desarrolla lupus inducido por fármacos: en este caso suspender el tratamiento; citopenias (principalmente leucopenia); síndromes desmielinizantes, neuritis óptica (muy raras veces): los síntomas desaparecen después de la interrupción del fármaco; reactivación de la infección por VHB; aumento de la actividad de ALT/AST en el suero |
|
Etanercept
|
VSc 25 mg 2 × semana o 50 mg 1 × semana |
|
Infliximab
|
iv. 3-10 mg/kg inicialmente en las semanas 0, 2 y 6, después cada 8 semanas o 3-5 mg/kg cada 4 semanas |
|
Golimumab |
VSc 50 mg 1 × mes |
Véase más arriba |
Véase más arriba |
Véase más arriba |
|
Certolizumab
|
VSc 200 mg 2 × d en las semanas 0, 2 y 4, a continuación una dosis de mantenimiento de 200 mg cada 2 semanas |
Véase más arriba |
Véase más arriba |
Véase más arriba |
|
Rituximab
|
iv. 1 g 2 veces en un intervalo de 14 días; se puede repetir después de 6 meses |
Infecciones b; hepatitis viralesd,h, embarazo y lactancia |
Reacciones alérgicas; infecciones; probablemente leucoencefalopatía multifocal progresiva (muy raras veces); reactivación de la infección por VHB |
Véase más arriba + concentración de inmunoglobulinas séricas |
|
Tocilizumab
|
iv. 8 mg/kg cada 4 semanas |
Infección b; hepatitis viralesd,l; ALT/AST >5 × LSN; neutropenia <500/µl, y trombocitopenia <50 000/µl; embarazo y lactancia |
Infecciones, neutropenia y trombocitopenia, aumento de la actividad sérica de ALT/AST (particularmente con el uso concomitante de fármacos potencialmente hepatotóxicos, p. ej. FARME), trastornos lipídicos, perforación intestinal en enfermos con diverticulitis (poco común) |
Véase más arriba (debido a la supresión de la respuesta de fase aguda, debe vigilarse sobre todo el desarrollo de infección) + ALT/AST cada 4-8 semanas durante los primeros 6 meses de tratamiento, y luego cada tres meses; hemograma después de 4-8 semanas de tratamiento, y luego según las indicaciones |
|
a Dosis de cloroquina >2,3 mg/kg/d, de hidroxicloroquina >5 mg/kg/d, disminución de la TFGe, uso de tamoxifeno, maculopatía.
b Infecciones que requieran hospitalización o administración parenteral de antibióticos, tuberculosis (activa o latente, si el enfermo no recibe tratamiento profiláctico contra la tuberculosis), infección activa por varicela zóster y herpes zóster, infección fúngica activa grave (en el caso de agentes biológicos también presumiblemente infección del tracto respiratorio superior viral con fiebre y úlceras de la piel infectadas, no cicatrizadas).
c Actividad de ALT y/o AST >2 × LSN.
d Hepatitis B o C aguda.
e Hepatitis B o C aguda o crónica (independientemente del tratamiento y del grado de insuficiencia hepática).
f No administrar el mismo día que el metotrexato.
g El antecedente de enfermedad pulmonar no es contraindicación absoluta para usar cualquier FARME.
h Hepatitis B crónica (salvo hepatitis tratada en la insuficiencia hepática en clase A de Child-Pugh: la sulfasalazina puede administrarse en insuficiencia hepática clase A o B) o hepatitis C crónica en clase B o C (el etanercept está indicado como potencialmente seguro en enfermos con hepatitis C crónica).
i Para tofacitinib <750/µl
j Para tofacitinib <9 g/dl
k El rituximab está indicado en enfermos con AR aptos para el tratamiento biológico, en los que (en cualquier momento) se ha tratado una neoplasia linfoproliferativa o el melanoma o que en los últimos 5 años han padecido cáncer de piel o una neoplasia sólida.
l No hay pruebas de la seguridad de uso del tocilizumab en la hepatitis viral crónica.
ALT — alanina-aminotransferasa, AR — artritis reumatoide, AST — aspartato-aminotransferasa, FEVI — fracción de eyección del ventrículo izquierdo, TFGe — tasa de la filtración glomerular estimada |
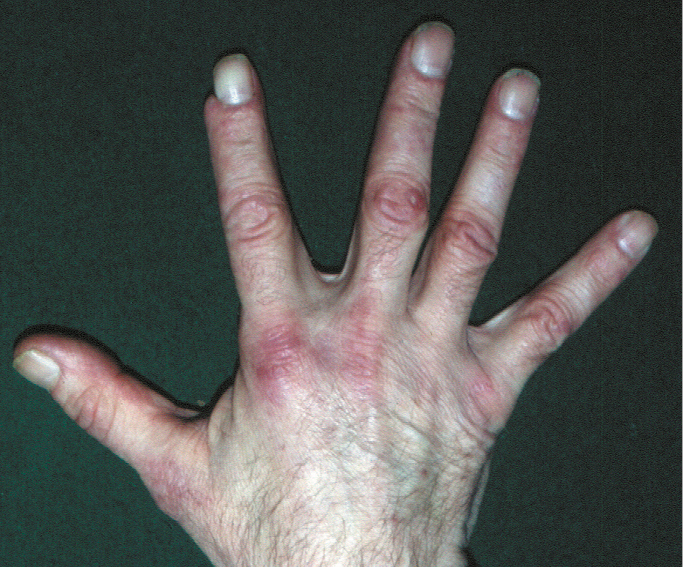
Fig. 1.8-5. Polimiositis y dermatomiositis. Pápulas violáceas sobre articulaciones interfalángicas y metacarpofalángicas (pápulas de Gottron)
 Español
Español
 English
English
 українська
українська






