Definición y etiopatogeniaArriba
La enfermedad hepática grasa no alcohólica (NAFLD) es una esteatosis hepática confirmada por una prueba de imagen o histológica sin detectar causas de esteatosis secundaria, tales como abuso de alcohol, uso crónico de fármacos que causan esteatosis, enfermedades hereditarias monogénicas. La NAFLD es la esteatosis de ≥5 % de los hepatocitos en el estudio histológico o contenido de grasa hepática >5,6 % en espectroscopia protónica por resonancia magnética (1H-ERM) o en resonancia magnética con contraste de fase. La NAFLD con mayor frecuencia está asociado al síndrome metabólico (→Síndrome metabólico) y causa riesgo elevado de ateroesclerosis precoz y muerte por causas cardiovasculares. La NAFLD abarca tanto la esteatosis hepática no alcohólica (NAFL; esteatosis simple o con una leve inflamación lobular, sin causas de esteatosis secundaria →tabla 7.11-1, mínimo riesgo de progresar a cirrosis), como la esteatohepatitis no alcohólica, que deriva de esta (NASH; esteatosis hepática con hepatitis crónica progresiva, balonamiento de los hepatocitos, con o sin fibrosis hepática; la NASH sin tratamiento evoluciona a fibrosis, cirrosis y hepatocarcinoma).
La causa de la NAFLD es una dieta hipercalórica (alimentos tipo comida rápida), rica en carbohidratos refinados, especialmente en fructosa, grasas saturadas y bebidas azucaradas, la cual, junto con escasa actividad física lleva a sobrepeso y obesidad. La insulinorresistencia, alteraciones en la regulación de la adiponectina y el estrés oxidativo desempeñan el papel principal en su patogenia; también es significativa la influencia de factores genéticos.
Los principales factores de riesgo de la NAFLD son: obesidad (sobre todo visceral), diabetes mellitus tipo 2, dislipidemia, síndrome metabólico, síndrome del ovario poliquístico. Entre los factores de riesgo se enumeran también: hipotiroidismo, hipopituitarismo, hipogonadismo, apnea del sueño, estado tras pancreatoduodenectomía y psoriasis.
Debido a la patogenia de la enfermedad, se ha propuesto cambiar la nomenclatura: en vez de enfermedad hepática grasa no alcohólica utilizar el nombre enfermedad del hígado graso asociada a la disfunción metabólica (metabolic dysfunction-associated fatty liver disease, MAFLD).
CUADRO CLÍNICO E HISTORIA NATURALArriba
Síntomas: generalmente ausentes. Algunos pacientes refieren cansancio, debilidad, malestar general o sensación de incomodidad en el cuadrante superior derecho del abdomen. La enfermedad se diagnostica con frecuencia de forma accidental al realizar una ecografía prescrita por otras causas, o después de identificar una actividad irregular de enzimas hepáticas (ALT, AST) en el suero.
Signos: generalmente obesidad, hepatomegalia (<75 % de los enfermos) o esplenomegalia (<25 %) u otros rasgos de hipertensión portal (raramente).
La fibrosis suele progresar lentamente (en un promedio de 1 grado en 14 años en la NAFL y 7 años en la NASH), pero en un ~20 % de los enfermos la fibrosis es de progresión rápida. En los enfermos con NASH el riesgo de fibrosis hepática y carcinoma hepatocelular está aumentado, pero la causa principal de muerte son las enfermedades cardiovasculares.
DIAGNÓSTICOArriba
Exploraciones complementarias
1. Pruebas de laboratorio: normalmente se observa un incremento leve o moderado de la actividad de ALT, AST (AST/ALT <1) y GGT (~50 % de los casos), hiperbilirrubinemia (raramente), dislipidemia (un 25-75 % de los enfermos), hiperglucemia o un test de tolerancia a la glucosa alterado (frecuentemente), hipoalbuminemia y alargamiento del TP (en enfermedad hepática avanzada), aumento de la concentración de hierro y ferritina (bastante frecuente).
2. Pruebas de imagen. Ecografía: aumento de la ecogenicidad hepática (esteatosis), con menor frecuencia hepatomegalia. En caso de cirrosis, presencia de signos de hipertensión portal. Exploración difícil en caso de obesidad, no detecta esteatosis leve (<20 % del peso del hígado) y no distingue la NAFL de la NASH. TC: buena valoración del hígado y de otros órganos (no se recomienda su uso rutinario por la radiación ionizante). RMN: valoración precisa de esteatosis leve (5-10 % de los hepatocitos), pero disponibilidad limitada; 1H-ERM es el único método verificado de medición cuantitativa de contenido de grasa hepática.
3. Valoración no invasiva de la fibrosis: a fin de seleccionar enfermos con fibrosis avanzada o cirrosis (F3-F4). Métodos
1) escalas basadas en parámetros bioquímicos: NAFLD Fibrosis Score (NFS, http://nafldscore.com), FIB-4 (http://gihep.com/calculators/hepatology/fibrosis-4-score/), Enhanced Liver Fibrosis (ELF), FibroTest
2) elastografía ecográfica (transitoria [FibroScan], exactitud limitada en obesidad; de ondas de corte), o elastografía por RMN.
4. Examen histológico de biopsia hepática: patrón de oro para el diagnóstico (necesario para distinguir con certeza la NAFL de la NASH), pero comporta un riesgo de complicaciones. Indicaciones:
1) sospecha de NASH, especialmente en caso de que las pruebas no invasivas indiquen fibrosis significativa (≥F2)
2) dudas diagnósticas, p. ej. otras causas de esteatosis, alta concentración de hierro sérico, presencia de autoanticuerpos (AAN, SMA, AMA), abuso de fármacos
3) coexistencia de la NAFLD con otras enfermedades hepáticas crónicas.
Procedimiento diagnóstico
Algoritmo de actuación →fig. 7.11-1.
Evaluación del enfermo con sospecha de NAFLD:
1) consumo de alcohol (descartado un consumo de ≥30 g/d por un hombre y de ≥20 g/d por una mujer)
2) antecedentes personales y familiares de diabetes, hipertensión arterial y enfermedades cardiovasculares
3) IMC, perímetro de la cintura, cambios del peso corporal
4) indicadores de la infección por el VHB y VHC
5) uso de fármacos relacionados con esteatosis
6) actividad de enzimas hepáticas (AST, ALT, GGT)
7) glucemia en ayunas, HbA1c, PTGO (eventualmente insulina en ayunas y prueba HOMA-IR)
8) hemograma
9) concentraciones de colesterol total, HDL, triglicéridos y ácido úrico en plasma
10) ecografía.
Diagnóstico ampliado, en función de la valoración inicial de la probabilidad o de los resultados de las pruebas
1) concentración de ferritina y saturación de transferrina por hierro
2) pruebas de detección de enfermedad celíaca, enfermedades de la glándula tiroides y síndrome del ovario poliquístico
3) pruebas de detección de enfermedades hepáticas raras: enfermedad de Wilson, enfermedades autoinmunes, déficit de α1-antitripsina
Criterios diagnósticos
1. NAFLD: esteatosis hepática en el estudio histológico o prueba de imagen y exclusión de otras causas de la acumulación de grasa en el hígado (→tabla 7.11-1).
2. NAFL: NAFLD sin balonamiento de los hepatocitos.
3. NASH: NAFLD con esteatosis de ≥5 % de los hepatocitos, inflamación lobular y portal y balonamiento de los hepatocitos.
Diagnóstico diferencial
Como en la hepatitis B crónica →Hepatitis B crónica.
TRATAMIENTOArriba
1. Modificación del estilo de vida: es esencial y abarca la reducción del aporte calórico, así como el aumento de la actividad física con el fin de reducir el peso corporal →tabla 7.11-2. En enfermos con NASH una reducción del peso corporal de ≥5 % puede reducir la esteatosis hepática, de ≥7 %: causar remisión de la esteatohepatitis, mientras que de ≥10 %: regresión o estabilización de la fibrosis. En personas con el IMC ≥25 kg/m2, el objetivo es reducir el peso corporal en ≥10 % (con pérdida de ~0,5-1 kg/semana), y en personas con normopeso: una reducción en un 3-5 % del peso corporal inicial. Con el fin de obtener una reducción significativa del peso corporal, es necesario reducir el aporte calórico en la dieta en 500-1000 kcal/d en comparación con el peso inicial, o hasta 1200 kcal/d en mujeres y 1400-1500 kcal/d en hombres. Se recomienda seguir una dieta mediterránea u otra similar, reducir la ingesta de ácidos grasos saturados (sobre todo de carne roja y carne procesada), y de productos edulcorados con fructosa, así como evitar el consumo de alcohol. El café puede resultar beneficioso para el curso de la NAFLD (≥2 tazas diarias).
El ejercicio físico refuerza el efecto de la dieta pobre en calorías. La actividad física, independientemente de la reducción de peso, puede reducir el contenido de grasa hepática. Se recomiendan 150-300 min/semana de actividad física de intensidad moderada (3-6 MET) o de 75-150 min/semana de alta intensidad (>6 MET), preferentemente en forma de ejercicios aeróbicos (caminatas, ciclismo).
En enfermos con NASH y obesidad mórbida en los que no se ha conseguido la reducción de peso, los efectos beneficiosos (incluida la mejoría de cambios histopatológicos en el hígado) pueden obtenerse con la cirugía bariátrica.
En enfermos con cirrosis hepática en el curso de NAFLD, con frecuencia se presenta la obesidad sarcopénica, por lo que requieren un asesoramiento profesional dietético y relacionado con ejercicios físicos.
2. Farmacoterapia: en enfermos con NASH confirmada histológicamente puede utilizarse la vitamina E 800 UI/d durante ≤1 año (contraindicada en casos de diabetes y cirrosis hepática; interrumpir si la actividad de ALT y AST no está reducida después de 6 meses) o la pioglitazona (registrada solo para el tratamiento de diabetes) 30 mg/d.
3. Tratamiento sintomático de las complicaciones de cirrosis hepática →Cirrosis hepática.
4. Trasplante hepático: en caso de cirrosis terminal o hepatocarcinoma.
ObservaciónArriba
En todos los enfermos con NAFLD diagnosticada, se debe determinar la estadificación de la cirrosis hepática →fig. 7.11-1. Controlar la actividad de ALT y AST cada 2-3 meses. No existen recomendaciones inequívocas en cuanto a la realización de ecografías de forma regular o a la determinación de α-fetoproteína en NAFLD, ni en NASH sin fibrosis avanzada. Monitorización de los enfermos con cirrosis hepática →Cirrosis hepática.
TABLAS Y FIGURASArriba
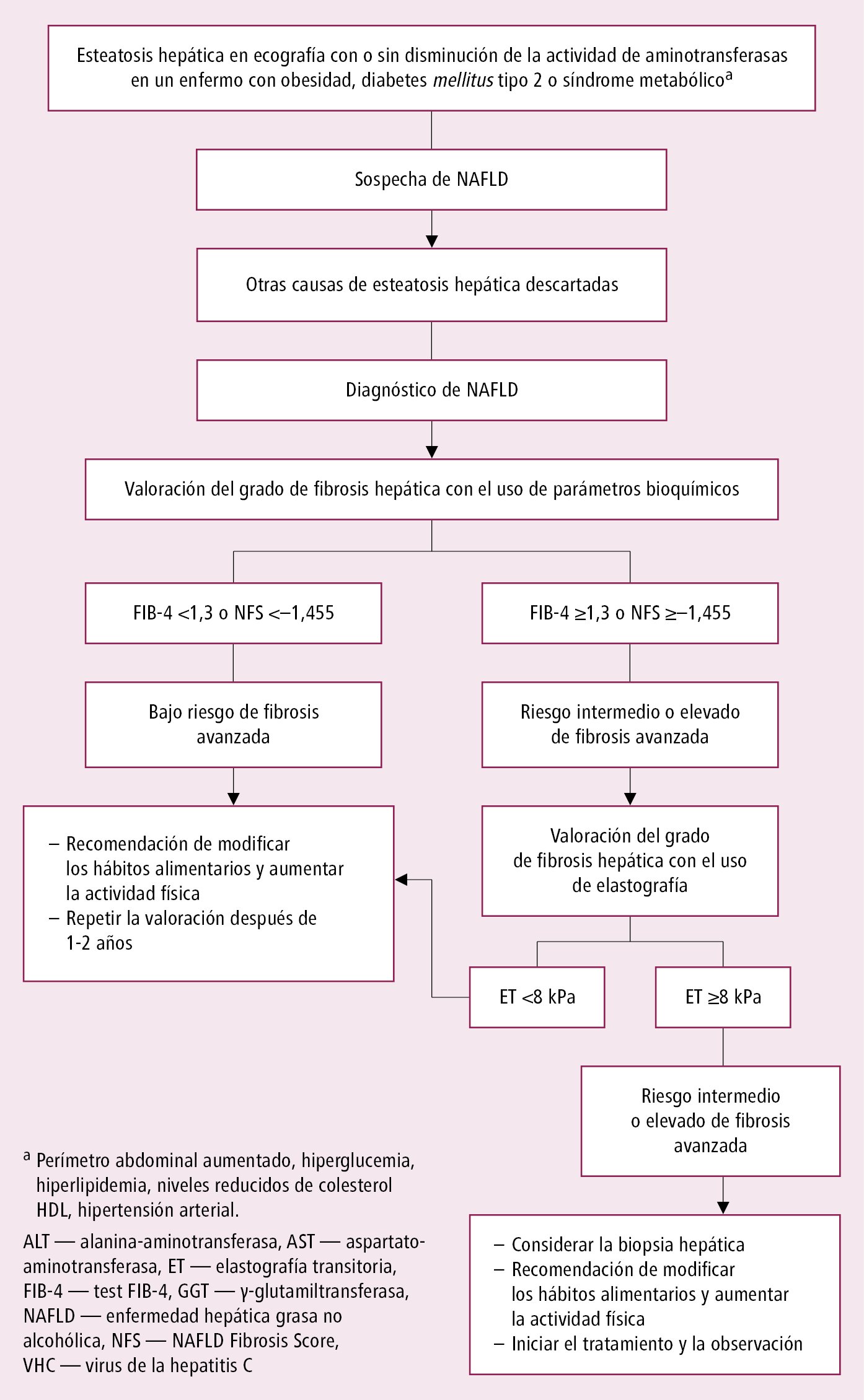
Fig. 7.11-1. Estrategia de diagnosticar y tratar la NAFLD
Tabla 7.11-1. Causas de esteatosis hepática
|
Alcohol |
|
Sustancias hepatotóxicas
– fármacos: antibióticos (tetraciclina, bleomicina, puromicina), citostáticos (metotrexato, L‑asparaginasa), vitaminas (vitamina A a dosis altas), y otros (amiodarona, estrógenos, glucocorticoides, salicilatos, valproato sódico, warfarina)
– sustancias químicas: clorohidrocarburos, tetracloruro de carbono, disulfuro de carbono, fósforo, sales de bario, hidrazina
– toxinas de hongos (α‑amanitina) |
|
Trastornos metabólicos y factores nutricionales
– sobrealimentación y obesidad, ayuno prolongado, desnutrición proteica (kwashiorkor)
– diabetes mellitus
– síndrome de Cushing
– déficit de zinc
– nutrición parenteral total a largo plazo (déficit de colina y carnitina)
– hiperlipidemias |
|
Trastornos de digestión y absorción
– enfermedades del páncreas
– resección del intestino
– anastomosis intestinal (p. ej. anastomosis yeyunoileal)
– síndrome de absorción deficiente
– enfermedad celíaca
– enfermedad inflamatoria intestinal (colitis ulcerosa, enfermedad de Crohn) |
|
Alteraciones congénitas del metabolismo
– abetalipoproteinemia
– déficit de acil‑CoA deshidrogenasa de ácidos grasos de cadena media
– enfermedades de almacenamiento: ésteres de colesterol (enfermedad de Wolman), esfingomielina (enfermedad de Niemann‑Pick), gangliósidos (enfermedad de Tay‑Sachs), glucocerebrósidos (enfermedad de Gaucher), cobre (enfermedad de Wilson), hierro (hemocromatosis hereditaria), glucógeno (glucogenosis), galactosa, fructosa, tirosina, homocisteína, ácido fitánico (síndrome de Refsum)
– trastornos congénitos del ciclo de la urea |
|
Enfermedades infecciosas
– hepatitis C
– hepatitis D fulminante
– endotoxemia |
|
Otras
– síndrome de Reye
– complicaciones del embarazo: esteatosis hepática aguda de embarazo, eclampsia, síndrome HELLP (hemólisis, aumento de la actividad de enzimas hepáticas y trombocitopenia) |
Tabla 7.11-2. Cambio de estilo de vida en el tratamiento de la enfermedad hepática grasa no alcohólica (NAFLD)
|
Reducción del aporte calórico |
– Reducir el aporte calórico en 500-1000 kcal a fin de reducir el peso corporal en 0,5-1 kg/semana
– Objetivo: reducción del peso corporal en ≥10 %
– Aplicar a largo plazo, junto con un aumento de actividad física y terapia cognitivo‑conductual |
|
Composición de la dieta |
– Baja o moderada ingesta de grasas y moderada o alta ingesta de carbohidratos
– Dietas ricas en proteínas o cetogénicas bajas en carbohidratos |
|
Consumo de fructosa |
Evitar bebidas y comidas ricas en fructosa |
|
Consumo de alcohol |
Categóricamente mantener el consumo de alcohol debajo del nivel de riesgo (es decir, 2 uds. de alcohol diarios en hombres y 1 ud. en mujeres) |
|
Consumo de café |
No hay limitaciones relacionadas con el hígado |
|
Entrenamiento y actividad física |
– 150-300 min/semana de ejercicios aeróbicos de intensidad moderada en 3-5 sesiones (p. ej. caminar rápido, bicicleta fija)
– el entrenamiento de resistencia también es eficaz, mejora el funcionamiento del sistema locomotor, ejerce influencia positiva en los factores de riesgo metabólicos
– un alto nivel de cansancio, por culpa del cual se limita la actividad y se produce somnolencia durante el día, dificulta la realización de los ejercicios recomendados |
 Español
Español
 English
English
 українська
українська





