Від Редакції: У даній статті представлено вибрану практичну інформацію щодо діагностики та лікування хронічних коронарних синдромів. Після кожної рекомендації у квадратних дужках вказано його силу та якість даних, на яких вона базується, відповідно до класифікації, представленої у таблиці 1.
Скорочення: АВК — антагоніст вітаміну К, АКШ — аортокоронарне шунтування, АМР — антагоніст мінералокортикоїдних рецепторів, АСК — ацетилсаліцилова кислота, БКК — блокатор кальцієвих каналів, БЛНПГ — блокада лівої ніжки пучка Гіса, БРА — блокатор рецептора ангіотензину, ГКС — гострий коронарний синдром, ДГП БКК — дигідропіридиновий блокатор кальцієвих каналів, ЕКГ — електрокардіограма, ЗПА — захворювання периферичних артерій, іАПФ — інгібітор ангіотензинперетворюючого ферменту, ІМТ — індекс маси тіла, КПІ — кісточково-плечовий індекс, КТ — комп’ютерна томографія, КТ-ангіографія — комп’ютерна томографічна ангіографія, КХ — коронарна хвороба, ЛЗ — лікарський засіб, ЛПНЩ — ліпопротеїди низької щільності, МРТ — магнітно-резонансна томографія, МНВ — міжнародне нормалізоване відношення, неДГП БКК — недигідропіридиновий блокатор кальцієвих каналів, НОАК — нові оральні антикоагулянти не антагоністи вітаміну К, ОФЕКТ — однофотонна емісійна комп'ютерна томографія, ПЕТ — позитронно-емісійна томографія, РГ — рентгенографія, рШКФ — розрахована швидкість клубочкової фільтрації, СН — серцева недостатність, СРТ — серцева ресинхронізуюча терапія, СС — серцево-судинний, ССЗ — серцево-судинне захворювання, ТІА — транзиторна ішемічна атака, УЗД — ультразвукове дослідження, ФВЛШ — фракція викиду лівого шлуночка, ФП — фібриляція передсердь, ХКС — хронічні коронарні синдроми, ХС ЛПНЩ — холестерин ліпопротеїдів низької щільності, ХХН — хронічна хвороба нирок, ЦД — цукровий діабет, ЧКВ — черезшкірне коронарне втручання, ШКТ — шлунково-кишковий тракт, ARNI — інгібітор рецепторів ангіотензину-неприлізину, DAPT (dual antiplatelet therapy) — подвійна антитромбоцитарна терапія, ESC — European Society of Cardiology, FFR (fractional flow reserve) — фракційний резерв кровотоку, HbA1c — глікозильований гемоглобін, IVUS — внутрішньосудинне ультразвукове дослідження, iwFR (instantaneous wave‑free ratio) — миттєвий резерв кровотоку, LAD (left anterior descending coronary artery) — ліва передня низхідна коронарна артерія, PCSK9 (proprotein convertase subtilisin/kexin type 9) — пропротеїнова конвертаза субтилізин/кексинового типу 9, PTP (pre‑test probability) — ймовірність захворювання перед проведенням тесту, STEMI — інфаркт міокарда з елевацією сегмента ST
Коронарна хвороба (КХ) полягає у формуванні атеросклеротичних бляшок в епікардіальних артеріях, що може призводити до їх стенозу або оклюзії. Це хронічне захворювання, найчастіше прогресуюче, навіть під час здавалося б асимптомних періодів. Може протікати з тривалими стабільними періодами, однак у будь-який момент може розвинутися загострення.
У клінічних настановах змінено термінологію, ввівши термін хронічні коронарні синдроми (ХКС) замість стабільної КХ. Вказана зміна підкреслює той факт, що КХ може маніфестуватись як гострий коронарний синдром (ГКС) або ХКС.
Виокремлено 6 найпоширеніших клінічних ситуацій:
1) хворі зі „стабільними” стенокардіальними симптомами і/або задишкою, у яких підозрюється КХ
2) хворі з уперше діагностованою серцевою недостатністю (СН) або дисфункцією лівого шлуночка i підозрою на КХ
3) асимптомні хворі або хворі зі стабільними симптомами, які перенесли ГКС впродовж останнього року, або хворі, яким упродовж останнього часу проведено реваскуляризацію
4) асимптомні або симптомні хворі, у яких діагностовано КХ або проведено реваскуляризацію понад рік тому
5) хворі зі стенокардією i підозрою на вазоспастичне або мікросудинне захворювання
6) асимптомні хворі, у яких КХ діагностовано під час скринінгових досліджень.
Хоча усі згадані вище клінічні ситуації класифікуються як ХКС, однак кожна з них асоціюється з іншим ризиком серцево-судинних (СС) подій. Цей ризик може змінюватись в перебігу захворювання у залежності від ступеня контролю факторів СС ризику, оптимальності змін стилю життя і/або фармакологічного лікування та ефективності реваскуляризації. Саме тому ХКС слід розглядати як різні стадії розвитку КХ, за винятком ситуацій, коли у клінічній картині домінує гострий тромбоз коронарної артерії.
|
клас (сила) рекомендації | |||
|
I |
наукові дані або широко прийнятий погляд вказують на те, що діагностична або терапевтична тактика являється корисною та ефективною (що означає: рекомендується/показана) | ||
|
II |
наукові дані або погляди щодо придатності чи ефективності визначеної діагностичної або терапевтичної тактики є суперечливими | ||
|
|
IIa |
наукові дані або погляди вказують на корисність або ефективність визначеної діагностичної чи терапевтичної тактики (що означає: необхідно зважити застосування) | |
|
IIb |
корисність або ефективність визначеної діагностичної чи терапевтичної тактики слабше підтверджена науковими даними або поглядами (що означає: можна розглянути застосування) | ||
|
III |
наукові дані або широко прийнятий погляд вказують на те, що визначена діагностична або терапевтична тактика не являється корисною ані ефективною, а в деяких випадках може бути шкідливою (що означає: не рекомендується) | ||
|
рівень доказовості даних | |||
|
A |
дані походять з численних рандомізованих досліджень або метааналізів | ||
|
B |
дані походять з одного рандомізованого дослідження або з великих досліджень без рандомізації | ||
|
C |
узгоджена думка експертів або дані походять з малих досліджень чи з ретроспективних досліджень або реєстрів | ||
Діагностична тактика
Виділяють наступні етапи тактики дій:
1) оцінка суб'єктивних та об'єктивних симптомів (у разі нестабільності симптомів відповідна тактика відповідно до інших клінічних настанов ESC)
2) врахування супровідних захворювань i якості життя (фармакологічне лікування, якщо реваскуляризація є необґрунтованою, можливо додаткові неінвазивні функціональні візуалізаційні дослідження, якщо діагноз КХ є сумнівним)
3) оцінка ЕКГ у спокої, результатів лабораторних досліджень, РГ грудної клітки в окремих хворих i ехокардіографії у спокої (відповідна тактика у разі зниження фракції викиду лівого шлуночка [ФВЛШ])
4) оцінка ймовірності захворювання перед проведенням тесту (PTP) i клінічної ймовірності КХ (виключення інших причин болю у грудній клітці)
5) вибір відповідного діагностичного дослідження
6) вибір відповідного методу лікування на основі вираженості симптомів i ризику серцевих подій.
У всіх хворих слід зібрати детальний анамнез — оцінити різновид болю у грудній клітці (типовий ангінозний, нетиповий ангінозний, неангінозний) і його вираженість за шкалою CCS та потенційну наявність задишки.
Об'єктивне обстеження дозволяє діагностувати анемію, артеріальну гіпертензію, клапанну хворобу серця, гіпертрофічну кардіоміопатію i аритмії. Рекомендується також розрахунок індексу маси тіла (ІМТ) та пошук симптомів захворювань інших артерій, окрім коронарних (також можуть протікати асимптомно), за допомогою дослідження пульсу на периферичних артеріях, аускультації сонних і стегнових артерій та оцінки кісточково-плечового індексу (КПІ), a також пошук симптомів супровідних захворювань, зокрема хвороб щитоподібної залози i нирок та цукрового діабету (ЦД).
Важливо виключити нестабільну стенокардію.
Якщо на основі оцінки хворого підозрюється клінічна нестабільність або ГКС, рекомендують серійні вимірювання концентрації серцевого тропоніну в крові, найкраще з використанням високочутливого або ультрачутливого тесту, щоб виключити пошкодження міокарда, пов'язане з ГКС [I/A].
У всіх осіб із підозрою на КХ рекомендують проведення наступних лабораторних досліджень:
1) загального аналізу периферичної крові (зокрема концентрації гемоглобіну) [I/B]
2) визначення концентрації креатиніну в сироватці крові i оцінку функції нирок [I/A]
3) аналіз ліпідного профілю (зокрема концентрації холестерину ЛПНЩ [ХС ЛПНЩ]) [I/A].
У хворих із підозрою або діагностованим ХКС рекомендують проведення скринінгових досліджень щодо ЦД 2-го типу — визначення відсотка глікозильованого гемоглобіну (HbA1c) i концентрації глюкози в плазмі крові натщесерце, a якщо результати цих досліджень неоднозначні — додатково проведення перорального глюкозо-толерантного тесту [I/B].
У разі клінічної підозри на захворювання щитоподібної залози рекомендують оцінку тиреоїдної функції [I/C].
Рекомендується проведення ЕКГ із 12‑ти відведень у спокої у всіх осіб:
1) із болем у грудній клітці, який не має іншої чіткої екстракардіальної причини [I/C]
2) під час епізоду стенокардії, який міг би вказувати на нестабільність КХ, або безпосередньо після такого епізоду [I/C].
Зміни сегмента ST під час надшлуночкових тахіаритмій не слід оцінювати як доказ наявності КХ [III/C].
Амбулаторний моніторинг ЕКГ:
1) рекомендують у хворих із болем у грудній клітці, у яких підозрюється аритмія [I/C]
2) найкраще із 12‑ти відведень, слід зважити у хворих, у яких підозрюється вазоспастична стенокардія [IIa/C]
3) рутинно не рекомендується у хворих, у яких підозрюється ХКС [III/C].
Рекомендується проведення трансторакального ехокардіографічного дослідження у всіх хворих [I/B], щоб:
1) виключити інші, окрім КХ, причини стенокардії
2) діагностувати сегментарні порушення скоротливості, що вказують на КХ
3) оцінити ФВЛШ, що є необхідним для стратифікації СС ризику
4) оцінити діастолічну функцію серця [I/B].
Якщо результат ехокардіографічного дослідження неоднозначний, тоді можна зважити проведення магнітно-резонансної томографії (МРТ) серця [IIb/C].
Проведення ультразвукового дослідження (УЗД) сонних артерій (лікарем, який пройшов відповідну підготовку) слід зважити з метою виявлення атеросклеротичних бляшок у хворих із підозрою на ХКС, у яких атеросклероз не був діагностований раніше [IIa/C].
Рекомендується проведення РГ грудної клітки у хворих із нетиповими симптомами, хворих із суб'єктивними та об'єктивними симптомами СН та у хворих із підозрою на захворювання легень [I/C].
На основі даних із клінічних досліджень відомо про те, що, порівнюючи з попередніми клінічними настановами, знижено PTP (тобто ймовірність захворювання перед проведенням додаткових досліджень) для КХ, яка базується на віці i статі пацієнта та наявних симптомах (табл. 2). Запроваджено також нове поняття „клінічної ймовірності КХ”, яке включає різні фактори ризику КХ, що модифікують PTP.
Клінічна ймовірність КХ нижча, ніж PTP, якщо виявлено:
1) нормальний результат електрокардіографічного тесту з фізичним навантаженням
2) відсутність кальцинатів у коронарних артеріях під час комп'ютерної томографії (КТ; результат 0 за шкалою Агатстона).
Клінічна ймовірність КХ вища, ніж PTP, якщо спостерігаються:
1) фактори СС ризику (дисліпідемія, ЦД, артеріальна гіпертензія, тютюнопаління, позитивний сімейний анамнез щодо серцево-судинного захворювання [ССЗ])
2) зміни на ЕКГ у спокої (зубці Q, зміни сегмента ST або зубця T)
3) дисфункція лівого шлуночка, що вказує на КХ
4) патологічний результат електрокардіографічного тесту з фізичним навантаженням
5) кальцинати в коронарних артеріях за результатами КТ.
|
Симптом |
30–39 років |
40–49 років |
50–59 років |
60–69 років |
≥70 років | |||||
|
Ч |
Ж |
Ч |
Ж |
Ч |
Ж |
Ч |
Ж |
Ч |
Ж | |
|
типовий ангінозний біль |
|
|
|
|
|
|
|
|
|
|
|
нетиповий ангінозний біль |
|
|
|
|
|
|
|
|
|
|
|
нехарактерний біль |
|
|
|
|
|
|
|
|
|
|
|
задишкаa |
|
|
|
|
|
|
|
|
|
|
|
Ймовірність КХ перед проведенням тесту (PTP) >15 % (сині поля) означає хворих, у яких неінвазивні дослідження є найбільш придатними. В осіб із PTP 5–15 % (голубі поля) можна зважити проведення діагностичних досліджень щодо наявності КХ після оцінки клінічної ймовірності КХ (див. текст). a якщо це єдиний або основний суб'єктивний симптом | ||||||||||
Вибір діагностичного дослідження, якому надається перевага, залежить від багатьох факторів.
Слід зважити надання переваги проведенню КТ-ангіографії, якщо:
1) клінічна ймовірність КХ низька
2) на основі характеристики пацієнта можна очікувати отримання візуалізації доброї якості
3) локально це дослідження доступне та виконують його особи з відповідним досвідом
4) необхідна інформація щодо наявності атеросклерозу
5) відсутність КХ в анамнезі.
Слід зважити надання переваги проведенню неінвазивним функціональним дослідженням для виявлення ішемії міокарда, якщо:
1) клінічна ймовірність КХ висока
2) реваскуляризація є ймовірною
3) локально це дослідження доступне та виконують його особи з відповідним досвідом
4) необхідною є також оцінка життєздатності міокарда.
Слід зважити надання переваги проведенню інвазивної коронарографії, якщо:
1) клінічна ймовірність КХ висока i спостерігаються тяжкі суб'єктивні симптоми із рефрактерністю до фармакологічного лікування
2) спостерігаються типові стенокардіальні симптоми під час фізичного навантаження низької інтенсивності, a клінічна оцінка (зокрема електрокардіографічний тест з фізичним навантаженням) вказує на високий ризик серцевих подій
3) наявна дисфункція лівого шлуночка, яка вказує на КХ.
Рекомендується проведення неінвазивного функціонального візуалізаційного дослідження для виявлення ішемії міокарда (стрес-ехокардіографії, стрес-МРТ серця, однофотонної емісійної комп'ютерної томографії [ОФЕКТ] чи позитронно-емісійної томографії [ПЕТ]) або КТ-ангіографії коронарних артерій як початкового дослідження для діагностики КХ у симптомних хворих, у яких виключно клінічна оцінка не дозволяє виключити КХ зі значущим стенозом коронарних артерій [I/B].
Рекомендується, щоб рішення щодо вибору початкового неінвазивного дослідження приймати на основі клінічної ймовірності КХ та інших характеристик пацієнта (здатність виконувати фізичне навантаження, ймовірність отримання візуалізації високої якості, очікуваний ступінь опромінення, ризик, асоційований з даним дослідженням, та протипоказання до його проведення), що впливають на результат дослідження, та враховуючи досвід даного центру і доступність досліджень [I/C].
Проведення неінвазивного функціонального візуалізаційного дослідження для виявлення ішемії міокарда рекомендують, якщо КТ-ангіографія не дозволила оцінити функціональне значення змін в коронарних артеріях або її результат недіагностичний [I/B].
Проведення коронарографії під час діагностики КХ рекомендують у хворих із високою клінічною ймовірністю КХ, суттєвими симптомами, які рефрактерні до фармакологічного лікування, або з типовою стенокардією, яка спостерігається під час невеликого фізичного навантаження, та у яких клінічна оцінка вказує на високий ризик серцевих подій. Необхідною є доступність інвазивної функціональної оцінки i її слід використовувати, щоб оцінити звуження перед проведенням реваскуляризації, якщо вони не є дуже високого ступеня (>90 % діаметру артерій) [I/B]. У той же час коронарографію з можливістю інвазивної функціональної оцінки слід зважити з метою підтвердження діагнозу КХ у хворих із сумнівним діагнозом, поставленим на основі неінвазивних досліджень [IIa/B].
Проведення КТ-ангіографії коронарних артерій:
1) слід зважити як альтернативу для коронарографії, якщо результати інших неінвазивних досліджень неоднозначні чи недіагностичні [IIa/C]
2) не рекомендується, якщо у зв'язку з обширними кальцинатами в коронарних артеріях, аритмією, значним ожирінням, нездатністю затримати дихання на прохання або іншими характеристиками малоймовірним є отримання візуалізації високої якості [III/C].
Не рекомендують ставити діагноз КХ зі значущим стенозом артерій на основі виявлення під час КТ-ангіографії кальцинатів у коронарних артеріях [III/C].
Проведення електрокардіографічного тесту з фізичним навантаженням:
1) рекомендують в окремих хворих з метою оцінки переносимості фізичного навантаження, наявності симптомів, аритмій, відповіді артеріального тиску i ризику серцевих подій (якщо така інформація може вплинути на подальшу тактику дій) [I/C]
2) можна зважити як альтернативне дослідження з метою підтвердження чи виключення КХ, якщо неінвазивні візуалізаційні дослідження недоступні [IIb/B]
3) можна зважити у лікованих хворих із метою оцінки контролю симптомів i ішемії міокарда [IIb/C]
4) не рекомендується у хворих із депресією сегмента ST ≥1 мВ при ЕКГ у спокої та у хворих, лікованих дигоксином [III/C].
Оцінка ризику
У хворих з діагностованим ХКС виділяють наступні категорії ризику на основі річного ризику смерті внаслідок серцевих причин:
1) високий ризик — ≥3 %
2) середній ризик — 1–2,9 %
3) низький ризик — 0–0,9 %.
Визначення високого ризику СС подій в залежності від різновиду діагностичного дослідження представлено у таблиці 3.
Рекомендується, щоб стратифікацію ризику проводити на основі клінічної оцінки i результату діагностичного дослідження, на підставі якого початково поставлено діагноз КХ [I/B].
Рекомендується проведення ехокардіографії у спокої з метою визначення функції лівого шлуночка у всіх хворих з підозрою на КХ [I/C]. Ехокардіографічна оцінка глобальної поздовжньої деформації надає додаткову, порівнюючи з ФВЛШ, інформацію, i можна зважити таку оцінку, якщо ФВЛШ становить >35 % [IIb/B].
Рекомендується стратифікація ризику у хворих із підозрою або вперше діагностованою КХ, найкраще за допомогою функціональної візуалізації або КТ-ангіографії коронарних артерій (якщо на це дозволить доступність таких досліджень i досвід локального центру), або за допомогою електрокардіографічного тесту з фізичним навантаженням (якщо хворий може виконати значне навантаження, a ЕКГ дозволяє діагностувати ішемічні зміни) [I/B]. Якщо КТ-ангіографія коронарних артерій доступна з метою стратифікації ризику, тоді перед тим, як скерувати на коронарографію асимптомного хворого або хворого з легко-вираженими симптомами, слід додатково провести візуалізаційні дослідження з навантаженням [IIa/B].
Проведення коронарографії у комбінації з інвазивними функціональними тестами:
1) з вимірюванням фракційного резерву кровотоку [FFR] — рекомендують з метою стратифікації СС ризику у симптомних хворих із клінічним профілем високого ризику, особливо, якщо суб'єктивні симптоми не відповідають достатнім чином на лікування i розглядається питання про реваскуляризацію з метою покращення прогнозу [I/A]
2) з вимірюванням FFR/миттєвого резерву кровотоку (iwFR) — рекомендують в асимптомних хворих або хворих зі слабко-вираженими симптомами, які отримують фармакотерапію та у яких результати неінвазивних досліджень вказують на високий ризик i розглядається питання про реваскуляризацію з метою покращення прогнозу [I/A]
3) з оцінкою FFR – слід зважити з метою стратифікації ризику у хворих із неоднозначними або спірними результатaми неінвазивних досліджень [IIa/B]
4) із проведенням внутрішньосудинного ультразвукового дослідження (IVUS) — можна зважити з метою стратифікації ризику у хворих із стенозом стовбура лівої коронарної артерії середнього ступеня [IIb/B].
Проведення коронарографії не рекомендується, якщо слугує лише стратифікації ризику [III/C].
|
Показник, що оцінюється при діагностичному дослідженні |
Визначення високого ризику |
|
річна смертність внаслідок серцево-судинних захворювань, визначена на основі електрокардіографічного тесту з фізичним навантаженнямa |
>3 % |
|
ділянка ішемії міокарда при візуалізаційному дослідженні |
>10 %б |
|
ураження коронарних артерій, виявлені під час КТ-ангіографії чи коронарографії |
значущі стенозив |
|
FFR і iwFR при інвазивному функціональному дослідженні |
FFR ≤0,8, iwFR ≤0,89 |
|
a оцінка ризику з застосуванням індексу Duke, який враховує потужність навантаження в MET, зміни сегмента ST під час навантаження або після його завершення, а також клінічні прояви (без стенокардії, стенокардія або стенокардія, що стала причиною припинення навантаження); калькулятор доступний на сайті http://www.cardiology.org/tools/medcalc/duke б >10 % при перфузійній сцинтиграфії серця (ОФЕКТ) або позитронно-емісійній томографії (ПЕТ); при магнітному резонансі серця ≥2-х сегментів (з 16-ти) з новим дефектом перфузії або добутамін-індукована дисфункція ≥3-х сегментів (з 16-ти); ≥3-х сегментів (з 16-ти) з порушенням рухливості стінки (гіпокінез чи акінез) при стрес-ехокардіографії в тобто трисудинне ураження зі стенозами в проксимальному сегменті, стеноз стовбура лівої коронарної артерії, стеноз проксимального сегмента лівої передньої низхідної коронарної артерії КТ‑ангіографія – комп’ютерна томографічна ангіографія, FFR – фракційний резерв кровотоку, iwFR – миттєвий резерв кровотоку | |
Рекомендується, окрім фармакологічного лікування, коригувати фактори, пов'язані зі стилем життя (див. нижче) [I/A]. Для того, щоб допомогти пацієнтами формувати здоровий стиль життя, рекомендують когнітивно-поведінкові втручання [I/A].
У хворих із ХКС рекомендують:
1) кардіологічну реабілітацію, що базується на програмі вправ, як ефективний спосіб формування здорового стилю життя та досягнення контролю над факторами ризику [I/A]
2) психологічні втручання з метою полегшення симптомів депресії у хворих із ХКС [I/B]
3) щорічну вакцинацію проти грипу, особливо у хворих похилого віку [I/B].
Рекомендується залучення мультидисциплінарної команди (що складається, напр., з кардіолога, лікаря первинної ланки, медсестри, дієтолога, фізіотерапевта, психолога і фармацевта) [I/A].
Рекомендовані модифікації стилю життя у хворих із ХКС:
1) відмова від тютюнопаління — застосування фармакологічних та поведінкових методів, що має на меті полегшити процес відмови від шкідливої звички, уникання пасивного куріння
2) здорова дієта — дієта, що багата овочами, фруктами та продуктами із цільних злаків; обмеження вживання насичених жирних кислот до <10 % від повної енергетичної потреби; обмеження вживання алкоголю до <100 г/тижд. або <15 г/добу
3) фізична активність — 30–60 хвилин фізичного навантаження середньої активності впродовж більшості днів тижня; користь приносить навіть нерегулярна активність
4) досягнення і збереження відповідної маси тіла (ІМТ <25 кг/м2) або принаймні зниження маси тіла завдяки дотриманню рекомендованого поступлення енергії та підвищеній фізичній активності
5) інші — вживання ЛЗ відповідно до рекомендацій; сексуальна активність низької або середньої інтенсивності асоціюється з низьким ризиком у стабільних асимптомних хворих.
Загальні рекомендації
Для лікування симптомних хворих застосовують 1–2 антиангінальні/антиішемічні ЛЗ у комбінації з ЛЗ, що попереджують розвиток СС подій [I/C].
Рекомендується, щоб проводити навчання хворих, інформуючи їх про захворювання, фактори ризику і стратегію лікування [I/C]. Також рекомендується, щоб у відповідний час (напр. 2–4 тиж. після призначення ЛЗ) оцінювати відповідь хворого na лікування [I/C].
Алгоритм антиішемічного лікування представлено на рисунку 1.
Рекомендується застосування:
1) нітратів короткої дії — з метою негайного полегшення стенокардії напруги [I/B] (нітрогліцерин в аерозолі діє швидше, порівнюючи з призначенням сублінгвально; ізосорбіду динітрат має дещо повільніший початок дії, ніж нітрогліцерин, а його ефект може зберігатись ≤1 год після призначення сублінгвально або кілька годин після перорального прийому таблетки)
2) β‑блокаторів і/або блокаторів кальцієвих каналів (БКК) — як лікування першої лінії з метою контролю частоти ритму серця i симптомів [I/A]; a якщо β‑блокатор або БКК не забезпечують достатнього контролю стенокардії, слід зважити комбіноване застосування β‑блокатора i дигідропіридинового БКК (ДГП БКК) [IIa/C]. Слід зважити вказану комбінацію як лікування першої лінії [IIa/B]. Дозу β‑блокатора необхідно підібрати таким чином, щоб частота ритму серця у спокої складала 55–60/хв.
Слід зважити застосування:
1) нітратів тривалої дії — як лікування другої лінії, якщо початкове лікування β‑блокатором і/або недигідропіридиновим БКК (неДГП БКК) є протипоказаним, погано переноситься або є недостатнім для досягнення контролю над симптомами [IIa/B]. Призначаючи нітрат тривалої дії, слід зважити рекомендацію перерв (10–14 год), під час яких хворий вживає ЛЗ у низькій дозі або не приймає його взагалі, що спрямоване на зниження ризику розвитку толерантності до ЛЗ [IIa/B]. Застосування нітратів не рекомендується у хворих із гіпертрофічною кардіоміопатією з обструкцією вихідного тракту, ані у хворих, що одночасно вживають інгібітори фосфодіестерази [III/B]
2) нікорандилу, ранолазину, івабрадину або триметазидину — як лікування другої лінії з метою зменшення частоти розвитку проявів стенокардії i покращення переносимості фізичного навантаження у хворих, у яких лікування β‑блокатором, БКК i нітратом тривалої дії є протипоказаним, погано переноситься або є недостатнім для досягнення контролю над симптомами [IIa/B]; можна зважити застосування із цією метою ранолазину чи триметазидину як лікування першої лінії у хворих з низькою стартовою частотою ритму серця i низьким артеріальним тиском [IIb/C].
В окремих хворих можна зважити комбіноване лікування β‑блокатором або БКК з ЛЗ другої лінії (ранолазином, нікорандилом, івабрадином або триметазидином) у рамах лікування першої лінії, в залежності від частоти ритму серця, артеріального тиску i переносимості ЛЗ [IIb/B].
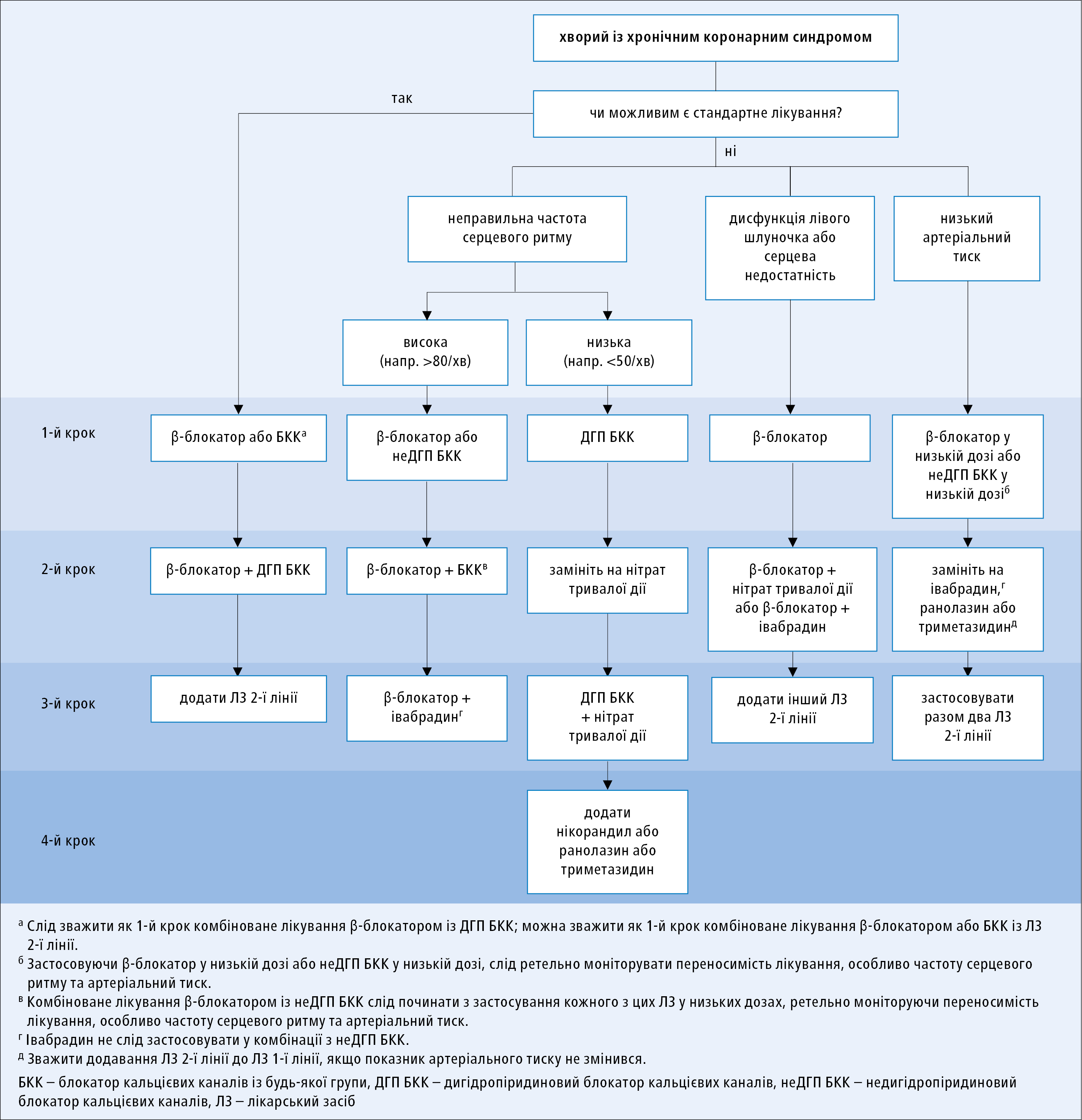
Рисунок 1. Алгоритм фармакологічного антиішемічного лікування у хворих із хронічними коронарними синдромами
Антитромбоцитарна терапія у хворих із синусовим ритмом
У хворих після інфаркту міокарда або коронарної реваскуляризації рекомендують застосування ацетилсаліцилової кислоти (АСК) у дозі 75–100 мг/добу [I/A], a у хворих із непереносимістю АСК — клопідогрель у дозі 75 мг/добу [I/B]. У хворих без інфаркту міокарда i коронарної реваскуляризації в анамнезі, але з результатами візуалізаційних досліджень, що однозначно вказують на КХ, можна зважити застосування АСК у дозі 75–100 мг/добу [IIb/C].
U симптомних або асимптомних хворих із захворюванням периферичних артерій (ЗПА) або ішемічним інсультом чи транзиторною ішемічною атакою (ТІА) в анамнезі можна зважити застосування клопідогрелю в дозі 75 мг/добу на противагу АСК [IIb/B].
Додавання другого антитромботичного ЛЗ (варіанти: ривароксабан 2,5 мг 2 × на день, клопідогрель 75 мг/добу, прасугрель 10 або 5 мг/добу, тікагрелор 60 мг 2 × на день) до АСК з метою довготривалої вторинної профілактики у хворих без високого ризику кровотечі (тобто без наступних факторів високого ризику: інтракраніальний крововилив або ішемічний інсульт в анамнезі, інше інтракраніальне захворювання в анамнезі, нещодавно перенесена кровотеча зі шлунково-кишкового тракту (ШКТ) або анемія внаслідок ймовірної кровотечі з ШКТ, інша хвороба ШКТ, пов’язана з підвищеним ризиком кровотечі, печінкова недостатність, геморагічний діатез або коагулопатія, дуже похилий вік або синдром старечої астенії, ниркова недостатність, що вимагає діалізної терапії або з рШКФ <15 мл/хв/1,73 м2):
1) слід зважити у хворих із високим ризиком ішемічних подій (КХ із множинним/дисемінованим ураженням артерій та ≥1-м із наступних факторів: ЦД, що вимагає фармакологічного лікування, черговий інфаркт міокарда, ЗПА, хронічна хвороба нирок [ХХН] з рШКФ 15–59 мл/хв/1,73 м2) [IIa/A]
2) можна зважити у хворих, які мають проміжний ризик ішемічних подій (≥1 із наступних факторів: КХ із множинним/дисемінованим ураженням артерій, ЦД, що вимагає фармакологічного лікування, черговий інфаркт міокарда, ЗПА, СН, ХХН із рШКФ 15–59 мл/хв/1,73 м2) [IIb/A].
Антитромбоцитарна терапія після черезшкірного коронарного втручання (ЧКВ) у хворих із синусовим ритмом
Рекомендується застосування АСК у дозі 75–100 мг/добу після імплантації стента [I/A].
Застосування клопідогрелю в дозі 75 мг/добу після прийому дози насичення (напр. 600 мг або застосування підтримуючої дози впродовж >5-ти днів) додатково окрім АСК:
1) рекомендують впродовж 6-ти місяців після імплантації стента до коронарної артерії, незалежно від різновиду стента, хіба що показане коротше застосування (1–3 міс.) у зв'язку з ризиком кровотечі, що загрожує життю, або розвитком такої кровотечі [I/A]
2) слід зважити впродовж 3-х місяців у хворих, які мають вищий ризик кровотечі, що загрожує життю [IIa/A]
3) можна зважити впродовж 1-го місяця у хворих із дуже високим ризиком кровотечі, що загрожує життю [IIb/C].
Можна зважити застосування прасугрелю або тікагрелору, принаймні у рамах початкового лікування, в особливих випадках планової імплантації стента, пов'язаної з високим ризиком ускладнень (напр. субоптимальна імплантація стента або інші ситуації під час процедури, пов'язані з високим ризиком тромбозу в стенті, складний стеноз стовбура лівої коронарної артерії або імплантація стентів у декілька судин), a також у тому разі, коли з приводу непереносимості АСК не можна застосувати подвійну антитромбоцитарну терапію (DAPT) [IIb/C].
У хворих із фібриляцією передсердь (ФП), яким призначається антикоагулянтна терапія, та які мають відповідність критеріям для застосування нових оральних антикоагулянтів не антагоністів вітаміну К (НОАК; інформація щодо показань до зниження дози або протипоказань до кожного НОАК у хворих із ХХН, масою тіла <60 кг, віком >75–80 років та взаємодією ЛЗ розміщена в інструкції для медичного застосування лікарського засобу), рекомендують надавати перевагу застосуванню НОАК, a не антагоністів вітаміну К (АВК) [I/A].
Довготермінову пероральну антикоагулянтну терапію (з допомогою НОАК або АВК зі збереженням МНВ в терапевтичному діапазоні впродовж >70 % часу):
1) рекомендують у хворих із ФП i кількістю балів за шкалою CHA2DS2‑VASc ≥2 у чоловіків i ≥3 у жінок [I/A]
2) слід зважити у хворих із ФП i кількістю балів за шкалою CHA2DS2‑VASc ≥1 у чоловіків i ≥2 у жінок [IIa/B].
Можна зважити додавання АСК у дозі 75–100 мг/добу (або клопідогрелю 75 мг/добу) до довготривалої пероральної антикоагулянтної терапії у хворих з ФП, інфарктом міокарда в анамнезі i з високим ризиком ішемічних подій (див. вище), які не мають високого ризику кровотечі (див. вище) [IIb/B].
У хворих, яким імплантують стент у коронарну артерію, у перипроцедурному періоді рекомендують застосування АСК і клопідогрелю [I/C].
У хворих, які мають відповідність критеріям для застосування НОАК, надається перевага застосуванню комбінації антитромбоцитарної терапії з НОАК (апіксабан 5 мг 2 × на день, дабігатран 150 мг 2 × на день, едоксабан 60 мг 1 × на день або ривароксабан 20 мг 1 × на день) на противагу АВК [I/A].
Під час антитромбоцитарної монотерапії або DAPT, якщо занепокоєння щодо кровотечі (ознаки високого ризику — див. вище) домінує над занепокоєнням щодо розвитку тромботичних ускладнень (тромбозу стента; ризик тромбозу i смерті в результаті його розвитку залежить від анатомічних, процедурних і клінічних факторів — у випадку хворих із ХКС це: імплантація стента у стовбур лівої коронарної артерії, проксимальний сегмент лівої передньої низхідної коронарної артерії [LAD] або останньої прохідної коронарної артерії, субоптимальне розміщення стента, довжина стента >60 мм; ЦД, ХХН, імплантація 2-х стентів у розгалуження коронарної артерії, стентування тривало оклюзованої коронарної артерії, перенесений тромбоз стента попри відповідне антитромботичне лікування) або занепокоєння щодо розвитку ішемічного інсульту — слід зважити застосування нижчої дози НОАК:
1) ривароксабану — 15 мг 1 × на день замість 20 мг 1 × на день [IIa/B]
2) дабігатрану — 110 мг 2 × на день замість 150 мг 2 × на день [IIa/B].
Після неускладненого ЧКВ слід зважити ранню відміну АСК (≤1-го тиж.) i продовження подвійної антитромботичної терапії оральним антикоагулянтом і клопідогрелем, якщо ризик тромбозу стента низький, або якщо занепокоєння щодо розвитку кровотечі домінує над занепокоєнням щодо тромбозу стента, незалежно від різновиду імплантованого стента [IIa/B].
Слід зважити потрійну антитромботичну терапію АСК, клопідогрелем та оральним антикоагулянтом впродовж ≥1-го місяця, якщо ризик тромбозу стента домінує над ризиком кровотечі. Загальна тривалість такого лікування (≤6-ти міс.) визначається на основі оцінки ризику тромбозу i ризику кровотечі, що слід чітко задокументувати під час виписки з лікарні [IIa/C].
У хворих із показаннями до лікування із застосуванням АВК у комбінації з АСК і/або клопідогрелем слід обережно коригувати дозу АВК таким чином, щоб МНВ зберігався у діапазоні 2,0–2,5 впродовж >70 % часу лікування [IIa/B].
Можна зважити подвійну антитромботичну терапію оральним антикоагулянтом у комбінації з тікагрелором або прасугрелем (досвід із застосуванням прасугрелю дуже малий) як альтернативу до потрійної антитромботичної терапії (оральний антикоагулянт + АСК + клопідогрель) у хворих із проміжним або високим ризиком тромбозу стента, незалежно від різновиду імплантованого стента [IIb/C]; не рекомендують застосування тікагрелору ані прасугрелю у рамах такого потрійного лікування [III/C].
Рекомендується застосування інгібітора протонної помпи у хворих, які вживають АСК у монотерапії, DAPT або оральний антикоагулянт у монотерапії, та мають високий ризик кровотечі з ШКТ [I/A].
Рекомендується застосовувати:
1) статини у всіх хворих на ХКС [I/A], a якщо у хворого не вдалося досягти мету лікування (зниження стартової концентрації ХС ЛПНЩ на ≥50% i концентрація ХС ЛПНЩ <1,4 ммоль/л [55 мг/добу]) за допомогою статину у максимальній дозі, яка переноситься хворим — додавання езетимібу [I/B], натомість якщо мета не була досягнута попри застосування статинy i езетимібу у максимальних дозах, які переносяться хворим — додавання інгібітора PCSK9 [I/A]
2) інгібітор ангіотензинперетворюючого ферменту (іАПФ) або блокатор рецептора ангіотензину (БРА) у хворих із супровідними захворюваннями (напр. СН, артеріальною гіпертензією або ЦД) [I/A], причому застосування іАПФ слід зважити у всіх хворих із ХКС та дуже високим ризиком СС подій [IIa/A]
3) β‑блокатора у хворих із дисфункцією лівого шлуночка або систолічною СН [I/A]; слід зважити довготривале застосування β‑блокатора у хворих після інфаркту міокарда з елевацією сегмента ST (STEMI) [IIa/B].
Оптимальне фармакологічне лікування — основа терапії ХКС, оскільки дозволяє призупинити прогресування атеросклерозу i попереджує розвиток тромботичних подій. Реваскуляризація міокарда також є важливою, однак її завжди слід оцінювати, як лікування, що доповнює адекватну фармакотерапію. Метою реваскуляризації є зниження вираженості стенокардіальних симптомів і/або покращення прогнозу.
Показання до реваскуляризації при ХКС залежать від наявності стенокардіальних симптомів та ішемії під час неінвазивних досліджень (рис. 2). Однак кожного разу слід ретельно оцінити співвідношення потенційної користі та шкідливих наслідків реваскуляризації у конкретного хворого. Хворому слід надати повну інформацію про переваги та недоліки обидвох стратегій, із врахуванням ризику кровотечі, пов'язаного із DAPT у випадку реваскуляризації з допомогою ЧКВ. Вибір методу реваскуляризації (ЧКВ чи аортокоронарне шунтування [АКШ]) обговорено у клінічних настановах ESC щодо реваскуляризації міокарда.
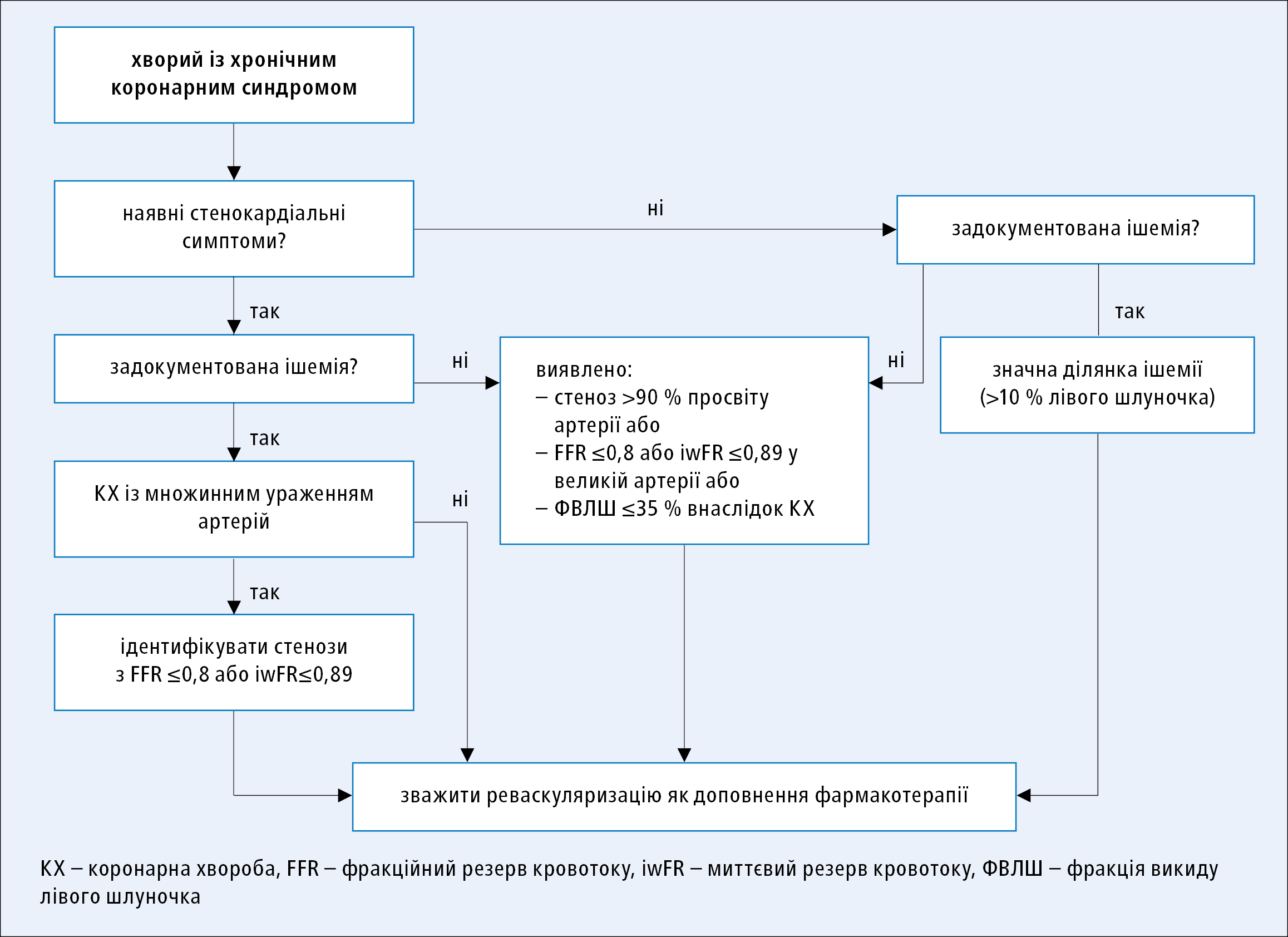
Рисунок 2. Показання до реваскуляризації у хворих із хронічними коронарними синдромами, у яких проводять коронарографію
Рекомендується детальне визначення профілю ризику i мульвекторна тактика дій, яка включає лікування серйозних супровідних захворювань, таких як артеріальна гіпертензія, гіперліпідемія, ЦД, анемія i ожиріння, із врахуванням відмови від тютюнопаління та змін стилю життя [I/A].
У симптомних хворих із ознаками застою у великому та малому колі кровообігу рекомендують застосувати сечогінну терапію з метою зменшення симптомів СН [I/B].
З метою зниження ризику ускладнень i смерті при СН, а також зменшення симптомів, рекомендують застосувати:
1) β‑блокатор (принципова складова фармакотерапії СН) [I/A]
2) іАПФ у хворих із симптомною СН або асимптомною систолічною дисфункцією лівого шлуночка після інфаркту міокарда [I/A], БРА як альтернативний варіант у хворих із непереносимістю іАПФ, або інгібітор рецептора ангіотензину-неприлізину (ARNI) у хворих, у яких симптоми СН зберігаються попри оптимальне лікування [I/B]
3) антагоніст мінералокортикоїдного рецептора (АМР) у хворих, у яких симптоми зберігаються попри оптимальне лікування з допомогою іАПФ i β‑блокатора [I/A].
Слід зважити застосування:
1) нітрату короткої дії, який призначають перорально або трансдермально (ефективне антиангінальне лікування, безпечне при СН) [IIa/A]
2) івабрадину у хворих із синусовим ритмом, ФВЛШ ≤35 % i частотою ритму серця у спокої >70/хв, у яких симптоми зберігаються попри відповідне лікування з застосуванням β‑блокатора, іАПФ i АМР, з метою зменшення ризику ускладнень i смерті [IIa/B].
Можна зважити застосування амлодипіну з метою зменшення вираженості стенокардії у хворих із СН, які мають непереносимість β‑блокаторів; даний ЛЗ вважається безпечним при СН [IIb/B].
У хворих із СН i брадикардією внаслідок атріовентрикулярної блокади високого ступеня, які вимагають електростимуляції серця, рекомендують імплантацію кардіоресинхронізуючого пристрою напротивагу системі правошлуночкової стимуляції [I/A].
У хворих із задокументованою шлуночковою аритмією, яка викликає нестабільність гемодинаміки (вторинна профілактика) та у хворих із симптомною СН i ФВЛШ ≤35 % рекомендують імплантацію кардіовертера-дефібрилятора з метою зменшення ризику раптової серцевої смерті i ризику смерті внаслідок будь-якої причини [I/A].
Рекомендується серцева ресинхронізуюча терапія (СРТ) у симптомних хворих із СН, синусовим ритмом, комплексом QRS тривалістю ≥150 мс [I/A] або 130–149 мс [I/B] i морфологією блокади лівої ніжки пучка Гіса (БЛНПГ) та ФВЛШ ≤35%, попри оптимальне лікування, з метою зменшення симптомів та ризику ускладнень i смерті.
Коронарна реваскуляризація рекомендується, якщо стенокардія зберігається попри лікування антиангінальними ЛЗ [I/A].
Хворі з давно діагностованим ХКС вимагають пожиттєвого лікування та спостереження.
За хворими після коронарної реваскуляризації і/або після ГКС, перенесеного впродовж останнього року, слід особливо ретельно спостерігати, оскільки вони мають підвищений ризик ускладнень i вимагають модифікації фармакологічного лікування. Рекомендується ≥2-х контрольних оглядів під час 1-го року спостереження. У разі систолічної дисфункції лівого шлуночка, діагностованої до реваскуляризації або після ГКС, контрольну оцінку функції лівого шлуночка слід зважити через 8–12 тижнів після втручання.
Через >1 рік від постановки діагнозу ХКС або коронарної реваскуляризації у кожного хворого, навіть асимптомного, лікар, який має відповідний досвід лікування ССЗ, повинен щороку оцінити СС ризик, загальний клінічний стан пацієнта i дотримання рекомендацій. Під час кожного огляду слід виконати ЕКГ із 12-ти відведень. Кожних 2 роки необхідно проводити лабораторні дослідження (ліпідний профіль, показники функції нирок, загальний аналіз периферичної крові i можл. біомаркери). У хворих, які, здавалося б, є асимптомними, корисним вважається кожних 3–5 років оцінити функцію лівого шлуночка (систолічну і діастолічну), клапанний апарат i розміри серця, a окрім того шукати "німу" ішемію із використанням неінвазивних методів, особливо за допомогою візуалізаційних досліджень із навантаженням. У разі нез'ясованого погіршення систолічної функції лівого шлуночка, особливо, якщо виявлено сегментарні порушення скоротливості, рекомендуються візуалізаційні дослідження коронарних артерій. Ліпідний профіль i глікемію слід визначати систематично — пропонується проводити ці дослідження щороку.
У асимптомних хворих:
1) рекомендуються систематичні огляди у лікаря, який має відповідний досвід лікування ССЗ, з метою оцінки потенційних змін у профілі ризику, можливості змін стилю життя, дотримання рекомендацій щодо факторів ризику та наявності супровідних захворювань, які можуть впливати na лікування i прогноз [I/C]
2) або зі слабко-вираженими симптомами, які отримують фармакологічне лікування, у яких неінвазивна стратифікація ризику вказує на високий ризик i у яких розглядається питання про реваскуляризацію з метою покращення прогнозу, рекомендується проведення коронарографії (із вимірюванням FFR, якщо це необхідно) [I/C]
3) із діагностованою КХ рутинне проведення КТ-ангіографії артерій коронарних в якості контрольного дослідження не рекомендується [III/C]
4) проведення коронарографії лише з метою стратифікації ризику не рекомендується [III/C].
У симптомних хворих рекомендують:
1) повторну оцінку щодо КХ у разі погіршення систолічної функції лівого шлуночка, яку не можна пояснити зворотною причиною (напр. довготривалою тахікардією чи міокардитом) [I/C]
2) стратифікацію ризику у разі появи нових або погіршення вже наявних симптомів, найкраще з допомогою візуалізаційного функціонального дослідження, у разі необхідності з допомогою електрокардіографічного тесту з фізичним навантаженням [I/B]
3) швидке скерування на дослідження у разі значної вираженості симптомів [I/C]
4) проведення коронарографії (з FFR/iwFR, якщо це необхідно) з метою стратифікації ризику у разі тяжкої КХ, особливо якщо симптоми зберігаються попри фармакологічне лікування або хворий має високий ризик [I/C].
У хворих із мікросудинною стенокардією зазвичай спостерігаються симптоми, пов'язані з навантаженням, i ознаки ішемії міокарда при неінвазивних дослідженнях, а також не виявлено стенозів під час коронарографії або КТ-ангіографії коронарних артерій, або ж вони легкі чи помірні та визнані функціонально незначущими.
Виявлення порушень мікроциркуляції у хворих із ХКС означає гірший прогноз, ніж досі вважалося, ймовірно тому, що найновіші наукові дані походять зі спостереження за хворими, у яких порушення мікроциркуляції були об'єктивно підтвердженими за допомогою як інвазивних, так і неінвазивних технологій.
У хворих, у яких симптоми зберігаються, a ангіографічна картина коронарних артерій є нормальною або виявлено лише помірні стенози, а iwFR/FFR є збереженим, слід зважити інвазивне вимірювання коронарного резерву і/або мікроциркуляторної резистентності [IIa/B]. При такому стані коронарних артерій можна зважити інтракоронарне введення ацетилхоліну з моніторингом ЕКГ під час ангіографії, щоб оцінити вазоспастичну реакцію мікроциркуляторного русла [IIb/B].
Можна зважити проведення трансторакального доплерівського дослідження LAD, МРТ серця i ПЕТ з метою неінвазивної оцінки коронарного резерву [IIb/B].
Лікування мікросудинної стенокардії повинно залежати від домінуючого механізму мікроциркуляторних порушень. У хворих із неправильним коронарним резервом або підвищеною мікроциркуляторною резистентністю та з негативним результатом провокаційної проби з ацетилхоліном рекомендують застосування β‑блокатора, іАПФ i статинy, враз зі змінами стилю життя i зниженням маси тіла. Хворих, у яких у відповідь на введення ацетилхоліну виникають зміни на ЕКГ i стенокардія, однак без значущого спазму епікардіальних артерій (така картина вказує на мікросудинний спазм), можна лікувати як хворих із вазоспастичною стенокардією.
Вазоспастичну стенокардію слід підозрювати у хворих із стенокардіальними симптомами, які спостерігаються здебільшого у спокої, зі збереженою переносимістю фізичного навантаження. Ймовірність вазоспастичної стенокардії є вищою, якщо напади болю частіше спостерігаються вночі та у ранкові години. Хворі часто молодшого віку i мають менше факторів СС ризику, порівнюючи з хворими на стенокардію напруги, за винятком тютюнопаління. Спазм коронарних артерій також слід запідозрити у тому разі, якщо у хворого з прохідними коронарними стентами зберігається стенокардія.
У хворих із підозрою на вазоспастичну стенокардію:
1) рекомендують проведення ЕКГ під час стенокардії, якщо це можливо [I/C]
2) рекомендують проведення коронарографії або КТ-ангіографії коронарних артерій, якщо спостерігається характерна епізодична стенокардія спокою i зміни сегмента ST, які нормалізуються після застосування нітрату і/або БКК — з метою оцінки обширності КХ, яка являється причиною симптомів [I/C]
3) слід зважити амбулаторний моніторинг сегмента ST з метою виявлення змін сегмента ST без збільшеної частоти ритму серця [IIa/C]
4) слід зважити інвазивну провокаційну пробу з метою діагностування спазму коронарної артерії у хворих з нормальними коронарними артеріями або незначущими стенозами цих артерій за даними коронарографії та спазмом коронарної артерії за даними клінічної картини — з метою визначення локалізації та різновиду спазму [IIa/B].
У хворих зі спазмом епікардіальних артерій або мікроциркуляторних судин ЛЗ першої лінії являються БКК i нітрати тривалої дії, у комбінації з контролем факторів СС ризику i змінами стилю життя. Виявлено, що ніфедипін ефективно зменшує спазм коронарної артерії, пов'язаний з імплантацією стента.
Скринінгові дослідження для виявлення коронарної хвороби у асимптомних осіб
У асимптомних осіб у віці старше 40-ка років без діагностованої ССЗ, ЦД, ХХН ані сімейної гіперхолестеринемії рекомендують оцінку ризику за допомогою відповідних шкал, зокрема SCORE [I/C].
Оцінка СС ризику повинна враховувати сімейний анамнез щодо передчасного ССЗ (визначеного як фатальна чи нефатальна СС подія і/або діагностоване ССЗ у родичів 1-го ступеня чоловічої статі віком до 55-ти років, a жіночої статі віком до 65-ти років) [I/C].
Рекомендується, щоб у всіх осіб віком до 50-ти років із обтяженим сімейним анамнезом щодо сімейної гіперхолестеринемії або передчасного ССЗ у родичів 1-го ступеня (чоловіків віком до 55-ти років і жінок віком до 65-ти років) виконати скринінгові дослідження, застосовуючи валідизовані клінічні шкали [I/B].
В асимптомних осіб фактором, що модифікує СС ризик (дозволяє краще віднести хворих у групи низького або високого ризику), під час оцінки СС ризику можна вважати:
1) оцінку індексу коронарного кальцію за допомогою КТ [IIb/B]
2) виявлення атеросклеротичної бляшки під час ультразвукового дослідження сонних артерій [IIb/B]
3) вимірювання КПІ [IIb/B].
В асимптомних дорослих осіб із високим СС ризиком (із ЦД, значно обтяженим сімейним анамнезом щодо КХ, або якщо під час попередньої оцінки ризик КХ оцінено як високий) можна зважити проведення функціонального візуалізаційного дослідження або КТ-ангіографії коронарних артерій з метою оцінки СС ризику [IIb/C]. В асимптомних дорослих із низьким ризиком та без ЦД проведення таких дослідження у рамах подальшої діагностики не рекомендується [III/C].
В асимптомних дорослих осіб (зокрема осіб, які ведуть сидячий спосіб життя i розглядають питання про застосування інтенсивного фізичного навантаження) можна зважити проведення електрокардіографічного тесту з фізичним навантаженням з метою оцінки СС ризику, особливо, якщо також необхідно оцінити показники, що не пов'язані з ЕКГ, зокрема фізичну справність [IIb/C].
Для оцінки СС ризику не рекомендуються:
1) ультразвукове вимірювання товщини комплексу інтима-медіа сонних артерій [III/A]
2) рутинне визначення біомаркерів у крові [III/B].
Рекомендується, щоб цільові показники офісного артеріального тиску складали: для систолічного тиску 120–130 мм рт. ст. для загальної популяції i 130–140 мм рт. ст. для осіб віком старше 65-ти років [I/A].
У хворих із артеріальною гіпертензією після нещодавно перенесеного інфаркту міокарда рекомендують вживання β‑блокатора i антагоніста ренін–ангіотензин–альдостеронової системи [I/A].
У хворих зі стенокардією рекомендують вживання β‑блокатора і/або БКК [I/A].
Комбіноване лікування іАПФ i БРА не рекомендується [III/A].
Рекомендується проведення коронарографії:
1) перед операцією на клапанах серця у хворих із будь-яким із наступних факторів: ССЗ в анамнезі, підозра на ішемію міокарда, систолічна дисфункція лівого шлуночка, чоловік у віці >40-ка років, жінка у постменопаузальному періоді, наявність ≥1-го факторa СС ризику [I/C]
2) з метою оцінки помірної або тяжкої функціональної недостатності мітрального клапана [I/C].
У хворих із тяжкою клапанною хворобою серця і малою ймовірністю КХ слід зважити перед втручанням на клапанах проведення КТ-ангіографії коронарних артерій як альтернативи для коронарографії [IIa/C].
У хворих, яким проводять транскатетерну імплантацію аортального клапана, слід зважити проведення ЧКВ у разі стенозу коронарної артерії >70 % у проксимальному сегменті [IIa/C].
Рутинне проведення стрес-тестів із метою діагностування КХ у хворих із тяжкою клапанною вадою не рекомендується, з огляду на низьку діагностичну цінність та ризик ускладнень [III/C].
У хворих на злоякісне новоутворення терапевтичні рішення повинні базуватися на очікуваній виживаності, коморбідності, зокрема тромбоцитопенії та збільшеній схильності до емболії і кровотеч, а такоє потенційній взаємодії між протипухлинними ЛЗ та ЛЗ, що застосовуються при ХКС [I/C].
У хворих зі значно вираженими симптомами ХКС та злоякісним новоутворенням і вираженим синдромом старечої астенії у разі показань до реваскуляризації рекомендують проведення мінімально інвазивних процедур [I/C].
У хворих на КХ із супровідним ЦД рекомендують контроль факторів ризику (артеріального тиску, концентрації ХС ЛПНЩ i відсотка HbA1c) зі збереженням відповідних цільових показників [I/A].
В асимптомних хворих на ЦД рекомендують систематичну оцінку ЕКГ у спокої з метою виявлення порушень провідності, ФП i "німого" інфаркту міокарда [I/C].
Рекомендується застосування іАПФ у хворих із ХКС i ЦД з метою попередження розвитку серцевих подій [I/B].
У хворих na ССЗ i ЦД рекомендують застосування:
1) інгібіторів натрій-глюкозного котранспортера 2-го типу (емпагліфлозину, канагліфлозину або дапагліфлозину) [I/A]
2) агоністів глюкагоноподібного пептиду-1 (ліраглютиду або семаглютиду).
Можна зважити проведення візуалізаційного функціонального дослідження або КТ-ангіографії коронарних артерій в асимптомних хворих на ЦД (віком >40-ка років) у рамах розширеної оцінки СС ризику [IIb/B].
У хворих на ХХН рекомендують:
1) контроль факторів СС ризику зі збереженням відповідних цільових показників [I/A]
2) звертати особливу увагу на модифікацію дозування ЛЗ, що екскретуються нирками та застосовуються при ХКС [I/C]
3) обмежити до необхідного мінімуму застосування йодовмісних контрастних речовин у разі тяжкої ХХН зі збереженим діурезом з метою попередження розвитку погіршення функції нирок [I/B].
У хворих похилого віку рекомендують:
1) звертати особливу увагу на побічні ефекти, непереносимість та ризик передозування ЛЗ [I/C]
2) застосовувати стенти, що вивільнюють ЛЗ [I/A]
3) застосовувати радіальний доступ із метою зменшення частоти кровотеч, пов'язаних із місцем доступу [I/B]
4) базувати діагностичну і терапевтичну тактику на симптомах, обширності ішемії міокарда, синдромі старечої астенії, очікуваній тривалості життя та супровідних захворюваннях [I/C].
Не рекомендують застосування гормональної замісної терапії з метою зменшення СС ризику у жінок у постменопаузальному періоді [III/C].
Рефрактерна стенокардія означає збереження впродовж ≥3-х місяців симптомів, спричинених діагностованою та оборотною ішемією міокарда, у хворих із КХ зі значущим стенозом коронарних артерій. Ці симптоми не вдається контролювати попри інтенсифікацію лікування з використанням ЛЗ другої і третьої лінії, АКШ або ЧКВ, також у разі тривало оклюзованих артерій. Така стенокардія спостерігається все частіше у зв'язку з випадками більш запущеної КХ, наявністю у хворих багатьох супровідних захворювань i старінням популяції.
У хворих із виснажливою стенокардією, рефрактерною до оптимального фармакологічного лікування і різних стратегій реваскуляризації, можна з метою полегшення симптомів зважити:
1) застосування посиленої зовнішньої контрпульсації [IIb/B]
2) імплантацію редуктора коронарного синуса [IIb/B]
3) стимуляцію спинного мозку (виявлено, що це втручання також асоціюється з покращенням якості життя) [IIb/B].
Трансміокардіальна лазерна реваскуляризація у таких хворих не рекомендується [III/A].
Запам'ятайте
Термін „стабільна КХ” замінено терміном „хронічні коронарні синдроми” (ХКС).
Шість найчастіших клінічних ситуацій при ХКС це:
1) хворі зі „стабільними” стенокардіальними симптомами і/або задишкою, у яких підозрюється КХ;
2) хворі з вперше діагностованою серцевою недостатністю (СН) або дисфункцією лівого шлуночка i підозрою на КХ;
3) асимптомні хворі або хворі зі стабільними симптомами, які перенесли ГКС впродовж останнього року, або хворі, яким нещодавно проведено реваскуляризацію;
4) асимптомні або симптомні хворі, у яких діагностовано КХ або проведено реваскуляризацію понад рік тому;
5) хворі зі стенокардією i підозрою на вазоспастичне або мікросудинне захворювання;
6) асимптомні хворі, у яких КХ діагностовано під час скринінгових досліджень.
PTP (ймовірність захворювання перед проведенням тесту) для КХ, що базується на віці, статі i симптомах, знизилась, порівнюючи з попередніми клінічними настановами (табл. 2). Введено новий термін „клінічної ймовірності КХ”, який включає різні фактори ризику КХ, що модифікують PTP.
Клінічна ймовірність КХ є нижчою, ніж PTP, якщо виявлено:
1) нормальний результат електрокардіографічного тесту з фізичним навантаженням;
2) відсутність кальцинатів в коронарних артеріях за результатом КТ (результат 0 за шкалою Agatstona).
Однак вона є вищою, ніж PTP, якщо спостерігаються:
1) фактори СС ризику (дисліпідемія, цукровий діабет, артеріальна гіпертензія, тютюнопаління, позитивний сімейний анамнез щодо ССЗ);
2) зміни на ЕКГ у спокої (зубці Q, зміни сегмента ST або зубця T);
3) дисфункція лівого шлуночка, яка вказує на КХ;
4) патологічний результат електрокардіографічного тесту з фізичним навантаженням;
5) кальцинати в коронарних артеріях за результатом КТ.
У симптомних хворих, у яких не можна виключити КХ зі значущими стенозами коронарних артерій за допомогою самої лише клінічної оцінки, рекомендують проведення неінвазивного функціонального візуалізаційного дослідження для виявлення ішемії міокарда або КТ-ангіографії коронарних артерій як початкового дослідження при діагностиці КХ.
Рекомендується, щоб рішення щодо вибору початкового неінвазивного дослідження приймати на основі клінічної ймовірності КХ та інших характеристик хворого (здатність виконувати фізичне навантаження, ймовірність отримання візуалізації доброї якості, очікуваний ступінь опромінення, ризик, пов'язаний з даним дослідженням i протипоказання до його проведення), які впливають на результат дослідження, та з врахуванням досвіду даного центру i доступностi досліджень.
Якщо КТ-ангіографія не дозволила встановити функціональне значення змін у коронарних артеріях або отримано її недіагностичний результат, рекомендують проведення неінвазивного функціонального візуалізаційного дослідження.
Проведення коронарографії рекомендують у хворих із високою клінічною ймовірністю КХ, суттєвими симптомами, рефрактерними до фармакологічного лікування, або з типовою стенокардією, яка спостерігаються під час невеликого навантаження, a також у яких клінічна оцінка вказує на високий ризик серцевих подій. Перед реваскуляризацією слід оцінити за допомогою функціонального дослідження значущість стенозу (не стосується стенозів >90 % діаметру артерій).
Електрокардіографічний тест з фізичним навантаженням вже не рекомендується як початкове дослідження з метою діагностування ХКС у хворих зі стенокардією i проміжним PTP. На даний момент це дослідження рекомендується з метою оцінки переносимості фізичного навантаження, симптомів, аритмії, відповіді артеріального тиску i ризику подій в окремих хворих, a можна зважити його виконання з метою підтвердження або виключення КХ, коли інші неінвазивні або інвазивні візуалізаційні методи недоступні. Можна зважити їх виконання у лікованих хворих із метою оцінки контролю симптомів i ішемії міокарда (зниження сили рекомендації з IIa до IIb).
Дуже важлива модифікація стилю життя, оскільки знижує ризик серцево-судинних подій i смерті.
Антиішемічну терапію слід персоналізувати відповідно до побажань хворого, його супровідних захворювань, лікування, яке застосовується, очікуваної переносимості ЛЗ i здатності дотримуватись рекомендацій. Вибір ЛЗ слід адаптувати до частоти ритму серця, артеріального тиску та функції лівого шлуночка (рис. 1).
ЛЗ першої лінії при ХКС є β‑блокатори i БКК.
Нітрати тривалої дії викликають толерантність, що знижує їх ефективність; дозування цих ЛЗ повинно враховувати 10–14‑годинну перерву.
Основну роль при вторинній профілактиці у хворих на ХКС відіграє антитромботична терапія. У хворих після інфаркту міокарда із високим ризиком ішемічних подій i низьким ризиком кровотечі слід зважити довготривале застосування АСК з інгібітором P2Y12 або ривароксабаном у дуже низькій дозі (2,5 мг 2 × на день), якщо немає показань до пероральної антикоагуляції.
У всіх хворих на ХКС рекомендують застосування статинy, a якщо цільової концентрації ХС ЛПНЩ не буде досягнуто — додавання у першу чергу езетимібу, а в другу чергу додатково інгібітора PCSK9.
Рекомендується щорічна вакцинація проти грипу, особливо в осіб старшого віку.
ACEI (або БРА) рекомендують у хворих із СН, ЦД або артеріальною гіпертензією, a їх застосування слід зважити у всіх хворих із високим ризиком.
У всіх хворих, які отримують АСК або комбіновану антитромботичну терапію та мають високий ризик кровотечі з ШКТ, рекомендують застосування інгібітора протонної помпи.
Хворі з тривалим ХКС повинні систематично звертатися на контрольні огляди з метою оцінки потенційних змін в їх профілі ризику, дотримання ними рекомендацій та розвитку супровідних захворювань. У разі погіршення симптомів і/або некорисної зміни в профілі ризику рекомендують провести повторний стрес-тест або коронарографію з функціональним дослідженням.
У випадку хворих, які, здавалося б, є асимптомними, вважається корисним, щоб кожних 3–5 років оцінити в них функцію лівого шлуночка (діастолічну і систолічну), клапанний апарат i розміри серця, a додатково провести пошук з метою виявлення „німої” ішемії міокарда за допомогою неінвазивних досліджень.