Скорочення: АГ — артеріальна гіпертензія, АМР — антагоніст мінералокортикоїдних рецепторів, АРС — альдостерон-ренінове співвідношення, КТ — комп'ютерна томографія, ЛЗ — лікарський(і) засіб(оби), ПГА — первинний гіперальдостеронізм, ПКР — пряма концентрація реніну, РАП — ренінова активність плазми, ФП — фібриляція передсердь, ESH — Європейське товариство артеріальної гіпертензії (European Society of Hypertension).
У 2020 році Робоча Група European Society of Hypertension (ESH) з питань гормонально опосередкованої артеріальної гіпертензії опублікувала позицію щодо ведення первинного гіперальдостеронізму (ПГА, синдром Конна; визначення і форми — див. рамку). Передумовою для підготовки цієї позиції був значний прогрес у вивченні походження захворювання, удосконаленні діагностики та подальшому розумінні ролі надлишку альдостерону в багатьох системних ускладненнях. Тактика ведення ПГА, яка досі використовувалась, ґрунтувалася на позиції американського The Endocrine Society, а представлена позиція ESH є першою європейською роботою з цього питання.1-3
| ПГА — це група патологічних клінічних ситуацій, пов'язаних з підвищеною, неадекватною до вживання натрію, секрецією альдостерону, яка є відносно незалежною від активності ренін-ангіотензинової системи і концентрації калію в плазмі.
Найбільш частими формами ПГА є одностороння альдостерон-секретуюча аденома наднирника і двостороння гіперплазія надниркових залоз (двосторонній ідіопатичний гіперальдостеронізм). |
Частота зустрічальності ПГА оцінюється в 3,2–12,7 % серед пацієнтів первинної медико-санітарної допомоги та 1–30 % серед пацієнтів, яким надається спеціалізована допомога. Автори позиції ESH вказують, що існує континуум між т. зв. первинною низькореніновою артеріальною гіпертензією (АГ) і ПГА. ПГА — прогресуюче захворювання, яке починається з фази з нормальним артеріальним тиском, але зі зниженою концентрацією реніну в плазмі та незначно підвищеною концентрацією альдостерону, і поступово прогресує до фази з АГ і більш вираженими змінами гормонального фону.
Резистентна АГ і АГ 3-го ступеня: частота зустрічальності ПГA зростає враз зі збільшенням ступеня тяжкості АГ. Вважається, що до 20% пацієнтів із резистентною АГ страждають ПГА.
АГ в молодому віці: пацієнти в молодому віці (<40 років) можуть мати більш легкі форми ПГА, і іноді у них немає класичних показань до діагностики ПГА. Ця група пацієнтів може отримати значну користь від діагностики і лікування ПГА з точки зору серцево-судинного ризику і якості життя, хоча даних, що підтверджують цю гіпотезу, недостатньо.
Гіпокаліємія: в численних дослідженнях оцінювалася частота зустрічальності гіпокаліємії у пацієнтів із ПГА, проте частота, з якою ПГА спостерігається у пацієнтів з АГ і гіпокаліємією, не досліджувалась. Однак, виявлення гіпокаліємії у пацієнта з АГ (без іншої відомої причини) завжди повинно викликати підозру на ПГА. Це також відноситься до гіпокаліємії, індукованої діуретиками.
Інциденталома наднирника: за оцінками, ПГА зустрічається у 1,6–4,3% пацієнтів із інциденталомами наднирників (в групі пацієнтів з АГ і без неї). У пацієнтів з інциденталомою наднирника і АГ ПГА може зустрічатися частіше.
Первинний гіперальдостеронізм або інсульт в ранньому віці в сімейному анамнезі: сімейні форми ПГА зустрічаються дуже рідко. Їх підозра може виникати в разі інсульту в ранньому віці у родича 1-го ступеня або діагнозу ПГА у родича 1-го ступеня в анамнезі. Сімейну форму ПГА слід підозрювати тільки в тому випадку, якщо ПГА виявлений в сімейному анамнезі у родичів молодого віку. Через відносно часту зустрічальність ПГА, його наявність у родичів похилого віку може бути випадковою і не обов'язково вказувати на генетичну схильність.
Цукровий діабет, метаболічний синдром і синдром обструктивного апное сну: автори позиції ESH підкреслюють, що порушення метаболізму глюкози, зокрема цукровий діабет, частіше зустрічаються у пацієнтів із ПГА, ніж в загальній популяції хворих на АГ. Що стосується синдрому обструктивного апное сну, було зазначено, що переважна більшість пацієнтів із синдромом обструктивного апное сну, які страждають ПГА, мають хоча б одне з перерахованих у позиції показань для діагностики ПГА.
Фібриляція передсердь (ФП) значно частіше зустрічається у пацієнтів із ПГА, ніж в загальній популяції пацієнтів з АГ. Результати дослідження з залученням хворих на ФП, не пов'язану зі структурним захворюванням серця або іншим захворюванням, вказують на відносно високий відсоток пацієнтів із ПГА в цій групі (42%).4 Однак до результатів цього дослідження слід підходити з обережністю, оскільки критерії включення пацієнтів з ФП нез'ясованої етіології викликають деякі сумніви — в дослідження були залучені тільки 18% пацієнтів із популяції хворих на ФП і АГ, хоча в той же час автори зробили висновок, що саме лише співіснування АГ не пояснює виникнення ФП. Нечіткі критерії включення можуть впливати на нерепрезентативність оцінюваної вибірки і утруднену екстраполяцію результатів на всю популяцію пацієнтів із ФП.
В якості скринінгу у пацієнтів з підозрою на ПГА рекомендується визначити концентрацію альдостерону і реніну в плазмі, а потім розрахувати альдостерон-ренінове співвідношення (АРС; співвідношення концентрацій альдостерону і реніну в плазмі), яке досі вважається найбільш вірогідним і доступним скринінговим методом. Існуючі відмінності в методах визначення прямої концентрації реніну (ПКР), ренінової активності плазми (РАП) і альдостерону не дозволяють встановити єдине порогове значення для АРС; якщо концентрація альдостерону виражена в нг/дл і АРС в одиницях нг/мл/год, найбільш часто використовують порогове значення для АРС, яке становить 30 (але також допустимі значення в діапазоні 20–40) — див. табл. Тому окремі лабораторії та центри розробляють власні норми.
|
|
РАП (нг/мл/год) |
ПКР(мМО/л) |
|
концентрація альдостерону (нг/дл) |
20 |
1,3 |
|
30 |
2 | |
|
40 |
2,7 | |
|
концентрація альдостерону (пмоль/л) |
550 |
36 |
|
830 |
55 | |
|
1100 |
74 | |
|
РАП – ренінова активність плазми, ПКР – пряма концентрація реніну на основі позиції ESH1 | ||
Концентрацію альдостерону і реніну в плазмі найкраще визначати після відміни лікарських засобів (ЛЗ), які на них впливають. При необхідності пацієнт може приймати верапаміл, доксазозин і моксонідин. Якщо не можна відмінити ЛЗ, що впливають на рівень альдостерону і реніну (β-блокатори, дигідропіридинові блокатори кальцієвих каналів, діуретики, інгібітори ангіотензинперетворюючого ферменту, антагоністи рецепторів ангіотензину [сартани]), слід оцінити АРС і інтерпретувати результат, враховуючи ефект ЛЗ, що приймаються пацієнтом. Цей тест не слід проводити пацієнтам, які приймають антагоніст альдостерону. Перед визначенням концентрації альдостерону та реніну слід скорегувати гіпокаліємію без обмеження вживання натрію. Забір зразків слід здійснити вранці (не пізніше, ніж опівдні) у пацієнта в сидячому положенні після, як мінімум, 2 годин перебування у вертикальному положенні (у цей час пацієнт може сидіти, але не може лягти).
У центрі, представленому авторами цієї статті, в якості порогового значення для АРС використовується значення 30 для концентрацій альдостерону і реніну, виражених в пг/мл. Якщо лабораторні значення виражені в інших одиницях, їх можна перевести в пг/мл: помноживши значення концентрації альдостерону в нг/дл на 10 і поділивши значення концентрації реніну, вираженої в мМО/л на 1,67. Також слід зазначити, що якщо АРС знаходиться в діапазоні 20–30, аналізується клінічна картина, і на цій основі деякі пацієнти можуть бути відібрані для подальшої діагностики ПГА.
На рисунку 1 представлені приклади інтерпретації результатів визначення АРС. При інтерпретації слід оцінити, чи концентрація альдостерону підвищена. Питання не в тому, чи перевищує вона верхню межу норми, тобто референтний інтервал, прийнятий в даній лабораторії. Вважається, що концентрація альдостерону повинна складати >150 пг/мл (15 нг/дл), хоча деякі автори рекомендують вважати пороговим значенням 100 пг/мл або граничне значення для діагнозу ПГА у підтверджуючому тесті (тобто >100 пг/мл або >60 пг/мл в тесті з натрієвим навантаженням). Концентрація реніну повинна бути низькою, тобто наближеної до нижньої межі референтного діапазону або нижче неї.
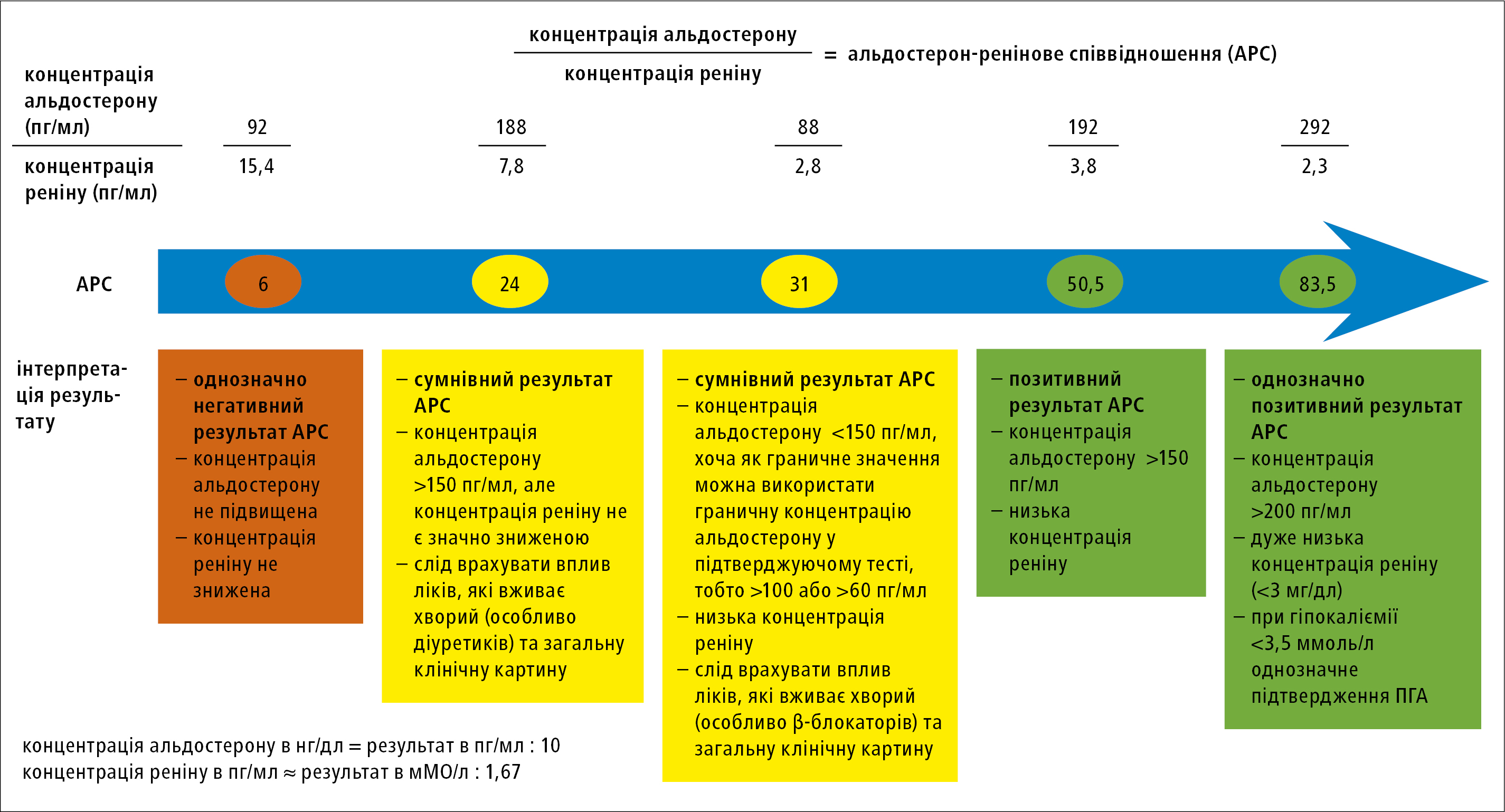
Рисунок 1. Альдостерон-ренінове співвідношення (АРС) — скринінг первинного гіперальдостеронізму (ПГА). Приклад інтерпретації співвідношення на основі позиції ESH з 2020 року і власного досвіду авторів даної роботи
Позитивний результат АРС зобов'язує провести один з визнаних підтверджуючих тестів для ПГА, однак автори позиції ESH пропонують, щоб у пацієнтів із ідіопатичною гіпокаліємією, концентрацією реніну в плазмі дуже низькою або нижче межі виявлення і з концентрацією альдостерону в стані спокою >200 пг/мл (20 нг/дл) ПГА можна діагностувати без необхідності проведення підтверджуючого тесту.
У позиції ESH перераховані 4 найбільш часто використовувані підтверджуючі тести: пероральний і внутрішньовенний тест з натрієвим навантаженням, тест з каптоприлом і тест з флудрокортизоном, при цьому підкреслюється, що вибір методу повинен залежати від доступності даного методу і досвіду конкретного центру. Як і в разі визначення АРС, слід врахувати ЛЗ, що впливають на ренін-ангіотензин-альдостеронову систему, та оцінити протипоказання до проведення дослідження — в разі тесту з натрієвим навантаженням це: значно підвищений артеріальний тиск, тяжка серцева недостатність і ниркова недостатність.
Автори позиції ESH обговорювали можливість рекомендації одного тесту і граничних значень для діагностики ПГА. Через недостатню кількість даних не було прийнято рішення про затвердження конкретних значень. На рисунку 2 запропонований діагностичний алгоритм ПГА, розроблений на основі обговорюваної позиції і досвіду авторів даної статті. На практиці в даний час найбільш часто використовується тест з натрієвим навантаженням в положенні сидячи. Найбільш часто використовуваним пороговим значенням, що дозволяє діагностувати ПГА в цьому випадку, є концентрація альдостерону >60 пг/мл (170 нмоль/л) з концентрацією кортизолу, яка є нижчою після інфузії 0,9% розчину NaCl, порівнюючи з її стартовим значенням. Прийнято також порогові значення для тесту з натрієвим навантаженням в положенні лежачи: >100 пг/мл (точний діагноз) і 50–100 пг/мл (ймовірний діагноз). У позиції ESH зазначено, що тест з натрієвим навантаженням, який виконують в положенні сидячи, може бути методом першої лінії, а в разі протипоказань до його проведення можна виконати тест з каптоприлом.
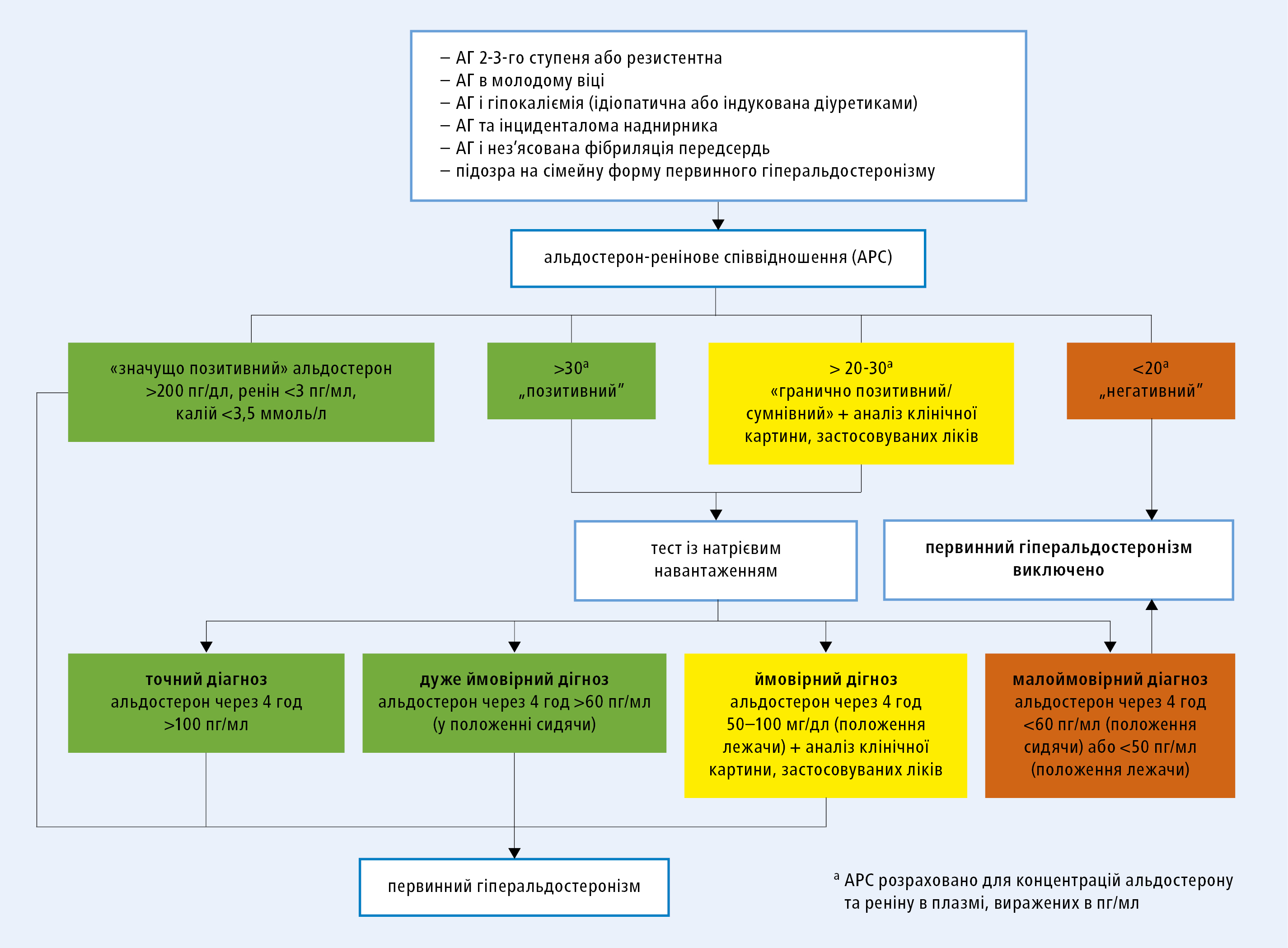
Рисунок 2. Алгоритм діагностичної тактики в осіб із підозрою на первинний гіперальдостеронізм. Наведені граничні значення на окремих етапах діагностики були запропоновані на підставі позиції ESH і досвіду авторів даної роботи. Їх слід розглядати як приклади і враховувати використовувану методологію і досвід даного центру
Всім пацієнтам з ПГА слід проводити комп'ютерну томографію (КТ) черевної порожнини з контрастуванням для виключення раку наднирника і оцінки венозного відтоку перед катетеризацією надниркових вен, а у пацієнтів, відібраних до операції, — анатомічну оцінку перед адреналектомією.
Автори позиції ESH підкреслюють, що відповідність результатів КТ результатам, отриманим на підставі катетеризації надниркових вен, не є задовільною. Найбільший проведений на сьогоднішній день метааналіз, що включає 38 досліджень із залученням в сумі 950 пацієнтів із ПГА, показав, що результат візуалізаційного дослідження (КТ або МРТ) майже в 38% випадків відрізнявся від результату катетеризації надниркових вен. Принагідно слід зазначити, що анатомічне зображення наднирників не може бути визначальним для діагнозу ПГА і диференціювання його форми. Наявність двосторонньої гіперплазії кори надниркових залоз за результатами візуалізаційного дослідження не вказує на наявність ПГА. Необхідно провести гормональні дослідження. Аналогічно, виявлення аденоми у пацієнта із ПГА (на КТ-картині) не є вирішальним для діагностування односторонньої форми (за винятком специфічної клінічної картини, описаної нижче).
Правильне визначення форми ПГА має ключове значення при виборі методу лікування. У всіх пацієнтів з односторонньої формою захворювання, відповідним чином відібраних до операції, адреналектомія нормалізує рівень калію в сироватці крові, у 30–60 % пацієнтів викликає нормотензію без необхідності прийому гіпотензивних ЛЗ, а у решти пацієнтів поліпшує контроль артеріального тиску. З іншого боку, пацієнтам із двосторонньою формою ПГА адреналектомія не приносить такої користі, і їх слід лікувати фармакологічно.
У позиції ESH як і раніше підкреслюється важливість катетеризації надниркових вен як «золотого стандарту» визначення форми ПГА. Автори детально обговорюють принципи виконання цієї процедури і інтерпретації результатів — зацікавленим ми рекомендуємо ознайомитися з цим документом.2
Молоді пацієнти (<35 років) з ідіопатичною гіпокаліємією, значно збільшеною секрецією альдостерону (концентрація альдостерону в плазмі >300 пг/мл), типовою картиною односторонньої аденоми (>10 мм) при КТ і нормальною морфологічною картиною другого наднирника, можуть не вимагати катетеризації надниркових вен перед адреналектомією.
Пацієнти з ПГА характеризуються підвищеним ризиком ускладнень з боку серцево-судинної системи в порівнянні з пацієнтами з ідіопатичною АГ, що пов'язано не лише з тривалими ефектами підвищеного артеріального тиску, а й зі шкідливою дією самого надлишку альдостерону. Як адреналектомія, так і медикаментозна терапія антагоністами мінералокортикоїдних рецепторів (АМР) знижують цей ризик.
У позиції ESH рекомендується виконувати односторонню лапароскопічну адреналектомію хворим із документально підтвердженою односторонньою формою захворювання. Іншим пацієнтам слід проводити тривале фармакологічне лікування за допомогою АМР. Це лікування також слід призначити пацієнтам із позитивним результатом скринінгу (АРС), які не дають згоду на продовження діагностики або яким вона протипоказана.
У пацієнтів із двосторонньою формою ПГА лікуванням вибору є спіронолактон, а в разі його непереносимості — еплеренон. Дозу ЛЗ слід поступово збільшувати. Вважається, що оптимальна доза АМР повинна забезпечити нормокаліємію без необхідності поповнення калію. Також встановлено, що зниження частоти серцево-судинних ускладнень в ході ПГА досягається тільки при наявності повної блокади мінералокортикоїдних рецепторів, про яку свідчить відсутність зниженої концентрації реніну.5 За наявності сумнівів щодо застосовуваної дози, слід виміряти концентрацію реніну — якщо вона все ще низька, це означає, що повна блокада рецепторів не відбулася і дозу слід збільшити.
Використання еплеренону обмежене відсутністю реєстрації для використання при АГ і ПГА в Європі. Слід пам'ятати, що еплеренон застосовується в дозі приблизно в 2 рази вищій, ніж доза спіронолактону, і розділений на 2 прийоми.
Незважаючи на прогрес, досягнутий в останні роки у визначенні патогенезу і принципів діагностики та лікування ПГА, діагностика цієї вторинної форми АГ як і раніше є багатоетапною та вимагає високоспеціалізованих досліджень. З огляду на свою поширеність ПГА слід підозрювати частіше, ніж це робилося раніше, і більш широко виконувати скринінгові тести, тобто оцінку АРС, яку можна проводити в амбулаторних умовах. Підставляючи результати отриманих визначень концентрації альдостерону в плазмі і РАП або ПКР в формулу, використовувану для розрахунку АРС, слід звернути увагу на одиниці, в яких вони виражені, для визначення відповідних порогових значень (див. табл.). При позитивному результаті пацієнтів слід направляти в спеціалізовані центри для виконання підтверджуючих тестів і визначення форми ПГА.
Запам'ятайте
Первинний гіперальдостеронізм (ПГА; синдром Конна) — це група патологічних клінічних ситуацій, пов'язаних із підвищеною, неадекватною до вживання натрію секрецією альдостерону, яка є відносно незалежною від активності ренін-ангіотензинової системи і концентрації калію в плазмі.
Найбільш частими формами ПГА є одностороння альдостерон-секретуюча аденома наднирника і двостороння гіперплазія надниркових залоз (двосторонній ідіопатичний гіперальдостеронізм).
ПГА слід підозрювати в наступних клінічних ситуаціях:
1) резистентна АГ і АГ 3-го ступеня;
2) АГ в молодому віці;
3) АГ з гіпокаліємією (також такою, що індукована діуретиками);
4) інциденталома надниркової залози;
5) інсульт у молодому віці у родича 1-го ступеня або діагноз ПГА у родича 1-го ступеня.
У пацієнтів із ПГА порушення метаболізму глюкози та фібриляція передсердь зустрічаються частіше, ніж у загальній популяції пацієнтів із АГ.
В якості скринінгу у пацієнтів із підозрою на ПГА рекомендується визначення концентрації альдостерону та реніну в плазмі, а потім розрахунок альдостерон-ренінового співвідношення (АРС).
Відмінності в методах визначення концентрації реніну, ренінової активності плазми (РАП) і альдостерону не дозволяють встановити єдине порогове значення для АРС; для концентрації альдостерону, вираженої в нг/дл, і РАП в одиницях нг/мл/год, найбільш часто використовуване порогове значення АРС становить 30.
Концентрації альдостерону та реніну в плазмі найкраще оцінювати після відміни ЛЗ, які на них впливають (β-блокатори, дигідропіридинові блокатори кальцієвих каналів, діуретики, інгібітори ангіотензинперетворюючого ферменту, антагоністи рецепторів ангіотензину [сартани]). При необхідності пацієнт може приймати верапаміл, доксазозин і моксонідин. Якщо не можна відмінити ЛЗ, що впливають на результат дослідження, слід оцінювати АРС і інтерпретувати його з врахуванням їх впливу. Це дослідження не слід проводити пацієнтам, які приймають антагоністи альдостерону. Перед визначенням концентрації альдостерону та реніну слід скорегувати гіпокаліємію, не обмежуючи вживання натрію. Забір зразків слід здійснити вранці (не пізніше, ніж опівдні) у пацієнта в сидячому положенні після, як мінімум, 2 годин перебування у вертикальному положенні.
При інтерпретації АРС слід оцінити, чи концентрація альдостерону є підвищеною (тобто >150 пг/мл; на думку деяких авторів >100 пг/мл або >60 пг/мл в тесті з натрієвим навантаженням). Концентрація реніну повинна бути низькою.
Позитивний результат АРС вимагає проведення одного з визнаних підтверджуючих тестів ПГА (найбільш часто використовувані: пероральний і внутрішньовенний тест із натрієвим навантаженням, тест з каптоприлом, тест з флудрокортизоном). У пацієнтів з ідіопатичною гіпокаліємією, рівнем реніну в плазмі нижче межі виявлення або в діапазоні дуже низьких значень і з концентрацією альдостерону в спокої >200 пг/мл (20 нг/дл), ПГА може бути діагностований без необхідності проведення підтверджуючого тесту.
Всім пацієнтам з ПГА слід виконати комп'ютерну томографію черевної порожнини з контрастуванням.
Пацієнтам з односторонньою формою захворювання рекомендується одностороння лапароскопічна адреналектомія. У пацієнтів, яким не проводиться хірургічне лікування (а також хворі з позитивним результатом АРС, які не дають згоду на продовження діагностики або яким це протипоказано), необхідно застосувати тривалу медикаментозну терапію антагоністом мінералокортикоїдного рецептора (АМР).
У пацієнтів із двосторонньою формою ПГА лікуванням вибору є спіронолактон, а в разі його непереносимості — еплеренон (в Європі немає реєстрації для цього показання). Дозу АМР слід поступово збільшувати; оптимальна повинна забезпечити нормокаліємію без необхідності поповнення калію. У разі сумнівів слід визначити концентрацію реніну і, якщо вона все ще низька, збільшити дозу ЛЗ.
1. Mulatero P., Monticone S., Deinum J. і співавт.: Genetics, prevalence, screening and confirmation of primary aldosteronism: a position statement and consensus of the Working Group on Endocrine Hypertension of The European Society of Hypertension. J. Hypertens., 2020; 38: 1919–1928
2. Mulatero P., Sechi L.A., Williams T.A. і співавт.: Subtype diagnosis, treatment, complications and outcomes of primary aldosteronism and future direction of research: a position statement and consensus of the Working Group on Endocrine Hypertension of the European Society of Hypertension. J. Hypertens., 2020; 38: 1929–1936
3. Funder J.W., Carey R.M., Mantero F. і співавт.: The management of primary aldosteronism: case detection, diagnosis, and treatment: an Endocrine Society clinical practice guideline. J. Clin. Endocrinol. Metab., 2016; 101: 1889–1916
4. Seccia T.M., Letizia C., Muiesan M.L. і співавт.: Atrial fibrillation as presenting sign of primary aldosteronism: results of the Prospective Appraisal on the Prevalence of Primary Aldosteronism in Hypertensive (PAPPHY) Study. J. Hypertens., 2020; 38: 332–339
5. Hundemer G.L., Curhan G.C., Yozamp N. і співавт.: Cardiometabolic outcomes and mortality in medically treated primary aldosteronism: a retrospective cohort study. Lancet Diabetes Endocrinol., 2018; 6: 51–59
