Ми прагнемо й надалі безкоштовно надавати цей тип контенту. На жаль, коштів на це більше немає.
Без Вашої допомоги нам доведеться закрити проект до кінця 2024 року.
Зробіть пожертвуВИЗНАЧЕННЯ ТА ЕТІОПАТОГЕНЕЗвгору
Найчастіша аденома гіпофіза, яка розвивається з лактотропних клітин, автономно продукує пролактин (ПРЛ), надмірна кількість якого призводить до гіперпролактинового гіпогонадизму, а у жінок проявляється синдромом аменореї та галактореї (amenorrhoea galactorrhoea), у чоловіків — еректильною дисфункцією; концентрація ПРЛ значно підвищується, добовий ритм коливань відсутній.
Патогенез пролактином не з’ясований, але існує морфологічна та ультраструктурна схожість між аденомами гіпофіза та NET, що стало основою для зміни класифікації пухлин гіпофіза (PitNET за ВООЗ 2022).
Патомеханізм розвитку гіпогонадизму: гіперпролактинемія пригнічує пульсове виділення виділення ГнРГ з гіпоталамуса, і, як наслідок, гіпофізарних гонадотропінів (ЛГ та ФСГ); також блокує гонадотропні рецептори в статевих залозах → пригнічення дозрівання Граафового фолікулу та ендокринної функції яєчників (недостатність естрадіолу та прогестерону у жінок), а також пригнічення сперматогенезу та ендокринної функції яєчок (дефіцит тестостерону у чоловіків). Прямий вплив підвищеного рівня ПРЛ на молочні залози → галакторея. Гінекомастія у чоловіків пов’язана з гіпогонадизмом та зменшенням співвідношення рівня тестостерону до рівня естрогенів.
КЛІНІЧНА КАРТИНА ТА ТИПОВИЙ ПЕРЕБІГвгору
Клінічні симптоми залежать від розміру пухлини («мас-ефект»), тривалості впливу та ступеню тяжкості гіперпролактинемії, яка призводить до гіпогонадизму. У випадку мікропролактиноми рідко спостерігається гіперплазія, тоді як макропролактинома, особливо у чоловіків, має інший перебіг і вимагає більш ретельного спостереження та відповідного лікування. Концентрація ПРЛ прямо пропорційна до розміру пухлини (крім пролактинових кістозних пухлин). Мікропролактиноми (microprolactinoma), як правило, не дають неврологічної симптоматики, на відміну від макропролактином, які часто супроводжуються порушенням поля зору, головним болем, інколи — гіпофункцією аденогіпофіза. У чоловіків та жінок гіпогонадизм супроводжується зниженням мінеральної щільності кісткової тканини (залежить від тривалості та ступеню тяжкості гіпогонадизму) і може мати етіологічний зв’язок з ожирінням (частіше при пролактиномі, ніж при гормонально-неактивних пухлинах гіпофіза).
Симптоми у жінок у пременопаузі залежать від концентрації ПРЛ у сироватці:
1) помірно підвищена, однак <2,3 нмоль/л (<50 мкг/л; норма <1,1 нмоль/л [25 мкг/л]) → порушення менструального циклу, недостатність жовтого тіла, непліддя, можлива галакторея, зниження лібідо;
2) 2,3–4,5 нмоль/л (50–100 мкг/л) → олігоменорея або аменорея, часто галакторея, зниження лібідо;
3) >4,5 нмоль/л (>100 мкг/л) → аменорея, галакторея і гіпогонадизм.
Симптоми у чоловіків: зниження лібідо, еректильна дисфункція, непліддя, гінекомастія та гіпогонадизм (зменшення оволосіння на обличчі та статевого оволосіння, зменшення м’язової маси).
ДІАГНОСТИКАвгору
Діагностичний алгоритм →рис. 8.4-2.
Показання для визначення концентрації ПРЛ:
1) клінічні — погіршення або втрата лібідо, безпліддя, галакторея, порушення менструального циклу, еректильна дисфункція;
2) лабораторні — гіпогонадотропний гіпогонадизм;
3) візуалізаційні — будь-яка аномальна масова пухлина в турецькому сідлі (інтраселлярна пухлина).
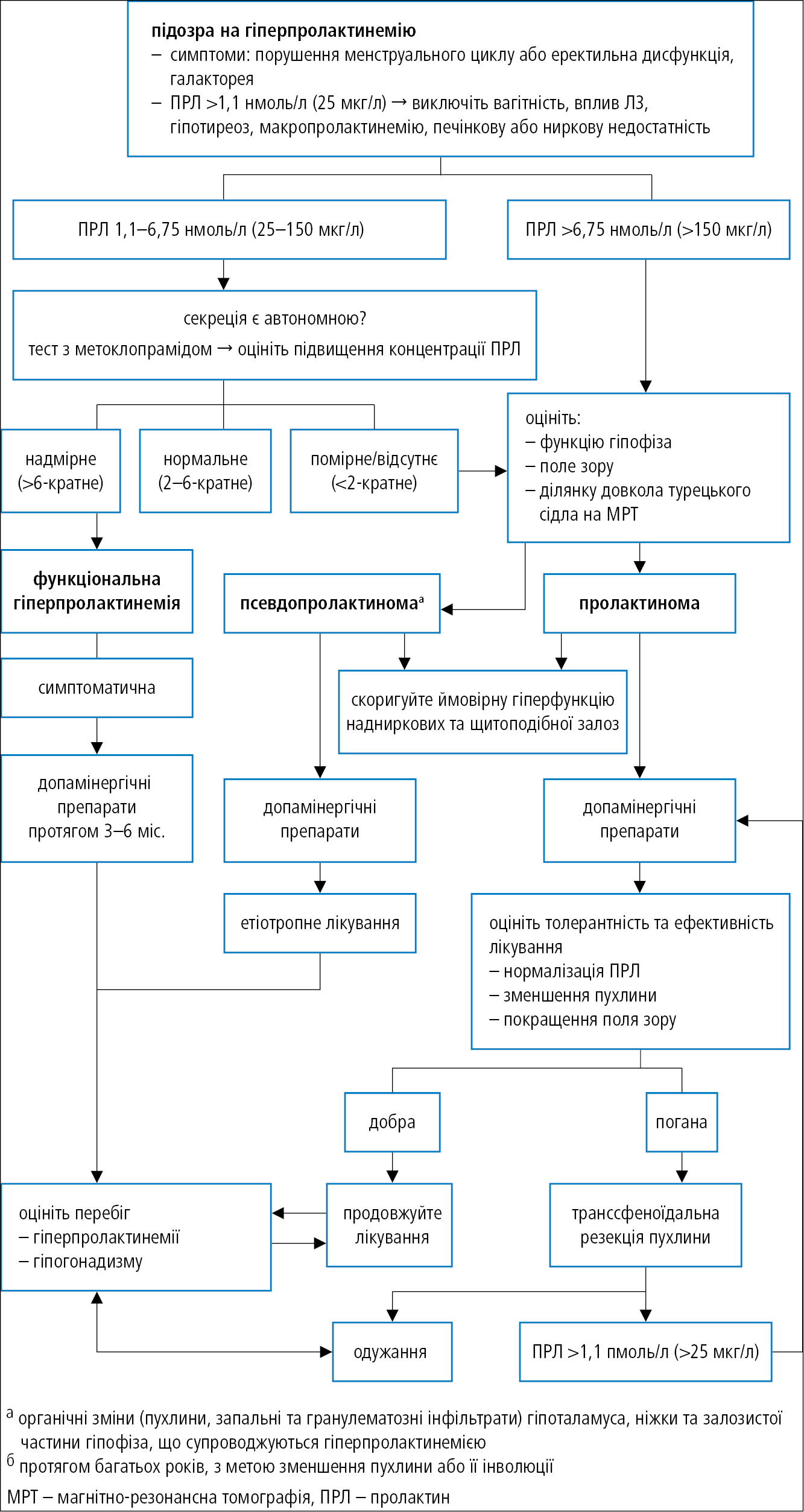
Рисунок 2. Алгоритм дій при гіперпролактинемії
1. Лабораторні дослідження: підвищення концентрації ПРЛ у сироватці:
1) >9 нмоль/л (200 мкг/л) — висока ймовірність наявності пухлини (рівень пролактину зазвичай корелює з розміром пухлини);
2) 6,75–9 нмоль/л (150–200 мкг/л) — доволі ймовірна наявність пухлини;
3) 1,12–6,75 нмоль/л (25–150 мкг/л) — діагноз сумнівний, можливий діагноз гормонально неактивної аденоми, що стискає ніжку гіпофіза. Якщо симптоми вказують на пролактинову пухлину або візуалізовано макроаденому гіпофіза → визначте концентрацію пролактину в зразку, розведеному 1:10 і 1:100, щоб виключити потенційну лабораторну помилку, т. зв. ефект гачка, тобто хибнонегативний результат через насичення антитілами, що використовуються в рутинних методах імунологічної діагностики (у тестах, що актуально виконуються, ефект гачка рідко зустрічається, але його слід враховувати, якщо підозрюється макропролактинома, а рівень пролактину <6,75 нмоль/л [150 мкг/л]); слід визначити концентрацію ПРЛ декілька разів, з інтервалами, напр., кожні 30 хв, або потрібно виконати тест з метоклопрамідом: дати 10 мг п/о та визначити початкову вихідну концентрацію ПРЛ, а потім ще через 60 та 120 хв — інтерпретація тесту →рис. 8.4-2.
Секреція ПРЛ має пульсовий характер (змінюється щогодини), характеризується добовим ритмом із підвищеною продукцією під час сну, зростає в умовах стресу та залежить від якості харчування та шкідливих звичок.
2. МРТ ділянки турецького сідла: проводиться обов’язково при наявності підвищеної концентрації ПРЛ та виключенні інших причин гіперпролактинемії (особливо, якщо у тесті з метоклопрамідом немає подальшого підвищення ПРЛ або воно є незначним [<2-разове], чи якщо у повторних дослідженнях підтверджується підвищена концентрація ПРЛ, яка зберігається на постійному рівні).
Вимагається:
1) виключення інших причин гіперпролактинемії (→нижче);
2) виявлення типової клінічної картини (у жінок зазвичай синдром аменореї і галактореї, ау чоловіків еректильна дисфункція);
3) у лабораторних дослідженнях значно підвищена і відносно постійний концентрація ПРЛ у сироватці та ознаки гіпогонадотропного гіпогонадизму;
4) підтвердження аденоми гіпофіза на МРТ.
1. Інші причини гіперпролактинемії:
1) вагітність;
2) підвищена секреція ПРЛ внаслідок відсутності гальмівного впливу гіпоталамічного допаміну на незмінені лактотропні клітини гіпофіза, що спричинене зменшенням його синтезу або транспорту з гіпоталамуса до гіпофіза через:
а) пухлини, інфільтративно-запальні процеси або травми гіпоталамуса чи гіпофізарної ніжки, які порушують допамінергічний шлях — псевдопролактинома (disconnection hyperprolactinemia) з помірно підвищеною концентрацією ПРЛ (при пролактиномі розмір пухлини корелює з концентрацією ПРЛ у сироватці крові, зазвичай >9 нмоль/л [200 мкг/л]);
б) ЛЗ, які впливають на гіпоталамічно-гіпофізарну регуляцію секреції ПРЛ — нейролептики (промазин, сульпірид, галоперидол, рисперидон), антидепресанти (іміпрамін, амітриптилін), блокатори допамінових рецепторів (метоклопрамід), антигіпертензивні препарати (верапаміл, спіронолактон, метилдопа), Н2-блокатори гістамінових рецепторів (циметидин, ранітидин), естрогени, опіоїди;
3) періодична гіперсекреція ПРЛ у відповідь на різноманітні подразники (у пацієнтів без органічних захворювань гіпоталамічно-гіпофізарної системи) — функціональна гіперпролактинемія;
4) гіперпролактинемія, супутня до некомпенсованого гіпотиреозу (підвищення секреції ТРГ активує секрецію ПРЛ);
5) підвищення рівня ПРЛ, що пов’язане з печінковою недостатністю (порушений метаболізм ПРЛ) або ниркової недостатності (зменшений кліренс);
6) змішані пухлини гіпофіза, які продукують одночасно ПРЛ та інші гормони (напр., СТГ).
2. Макропролактинемія — наявність високомолекулярного ПРЛ, зв’язаного з анти-ПРЛ-IgG, яка біологічно неактивна, проте високу імуногенність — високий рівень ПРЛ у сироватці крові супроводжується неадекватними або слабко вираженими клінічними симптомами (правильний діагноз дозволяє уникнути непотрібного лікування); при додаванні 25 % поліетиленгліколю (ПЕГ) до зразка сироватки крові, взятої на аналіз, макропролактин випаде в осад.
ЛІКУВАННЯвгору
Алгоритм лікування гіперпролактинемії →рис. 8.4-2.
1. Фармакотерапія є кращим методом лікування 1-ї лінії, хоча у окремих пацієнтів з неоднозначною гіперпролактинемією та високими шансами на ремісію може бути розглянуто хірургічне втручання (→нижче).
2. Ризик перетворення мікроаденоми у макроаденому впродовж 10 років становить ≈7 %, тому вважається, що не всі пацієнти потребують лікування. Лікування потрібно розпочати тоді, коли відновлення функції гонад є важливим для хворого. Дофамінергічні ЛЗ ефективні у >90 % випадків.
3. Ефективність фармакотерапії при макроаденомі та мікроаденомі є подібною, однак у випадку макроаденоми хірургічне лікування має обмежену ефективність, оскільки супроводжується великою кількістю рецидивів та післяопераційних ускладнень, тому використовується лише в особливих випадках.
Допамінергічні ЛЗ (агоністи допамінових рецепторів D2):
1) бромокриптин п/о 2,5–30 мг/добу; при резистентності до бромокриптину (відсутність нормалізації рівня ПРЛ або суттєвого зменшення аденоми гіпофіза після 3 міс. лікування максимально переносимою дозою ЛЗ) або поганій переносимості ЛЗ — змінити на каберголін;
2) каберголін п/о у початковій дозі 0,5 мг 1 раз на тиж., при необхідності поступово збільшують дозу аж до нормалізації рівня ПРЛ у сироватці; зазвичай 0,5–2,0 мг/тиж., які приймають 1–2 рази на тиж. (>1 мг/тиж., рекомендується розділити на 2 прийоми) — найкраще переноситься та найефективніший препарат для зменшення рівня ПРЛ та розмірів пролактиноми і з найдовшим періодом напіврозпаду;
3) хінаголід п/о 75–600 мкг/добу 1 × на день перед сном.
У більшості хворих можна досягти нормалізації рівня ПРЛ, запобігти подальшому розростанню аденоми, досягти зменшення пухлини (після року на >50 % у 90 % хворих), і навіть її зникнення. Лікування багаторічне, у деяких пацієнтів — пожиттєве. Припинення лікування часто призводить до рецидиву захворювання. Вважається, що <10 % пацієнтів після 2–4 років лікування можуть досягти ремісії та завершити терапію (більший шанс мають пацієнти з пухлинами, які спочатку не виявляли екстраселярного поширення та дуже добре реагували на лікування зі швидкою нормалізацією концентрації ПРЛ).
При застосуванні вищих доз, ніж стандартні (>2 мг/тиж.), каберголіну рекомендуються періодичні ехокардіографічні дослідження через ризик фіброзу та уражень клапанів серця. У 15 % пацієнтів, які отримували високі дози допамінергічних препаратів, спостерігалася компульсивна поведінка (гіперсексуальність, компульсивне переїдання, патологічна схильність до азартних ігор або покупок). Пацієнта слід попередити про ризик такої поведінки і, якщо вона виникає, можливо зменшити дозу препарату.
Застосовується у рідкісних випадках резистентності до допамінергічних ЛЗ або дуже вираженої їх непереносимості, якщо пухлина викликає компресію перехресту зорових нервів, що призводить до обмеження поля зору, яке зберігається після призначення допамінергічних препаратів у високих дозах. Згідно з рекомендаціями PS (2023), хірургічне лікування також може розглядатися (в рамках мультидисциплінарного консиліуму за участю досвідчених спеціалістів: ендокринолога, нейрохірурга та радіолога) як лікування 1-ї лінії в деяких випадках неінвазивної пролактиноми з прогнозом повної резекції пухлини (стадії 0 та 1 за класифікацією Кноспа). Ефективне лікування дозволяє пацієнту уникнути тривалої медикаментозної терапії; однак слід враховувати ризики, пов'язані з хірургічним втручанням, та ризик рецидиву гіперпролактинемії, незважаючи на початкову нормалізацію рівня ПРЛ в сироватці крові. Результати операції залежать від розміру пухлини; операцію повинен виконувати нейрохірург з відповідним досвідом проведення транссфеноїдальних процедур. У найкращих медичних центрах транссфеноїдальне видалення пухлини ефективне у 70 % мікропролактином, але в ≈20 % випадків розвиваються рецидиви. У випадку макропролактином відсоток одужань досягає ≈30 %, а частота рецидивів >50 %.
1. З метою уникнення неврологічних порушень, пов’язаних зі збільшенням розмірів пухлини гіпофіза під час вагітності внаслідок підвищеної концентрації плацентарного естрадіолу, ще до настання вагітності призначте фармакологічне лікування і намагайтеся досягти максимального зменшення розміру пухлини. Якщо протягом 3–6 міс. підтверджено зменшення пухлини та стабільні розміри при повторних МРТ, обмежені турецьким сідлом, вагітність буде безпечною навіть для жінок із макропролактиномою.
2. Під час вагітності медикаментозне лікування потрібно припинити, оскільки у жінок з мікропролактиномою вагітність зазвичай протікає без ускладнень, проте клінічний моніторинг потрібен кожні 3 місяці. У випадку макропролактиноми існує ризик збільшення аденоми, тому клінічний моніторинг потрібен щомісяця та додатково необхідно контролювати поля зору у кожному триместрі вагітності. Якщо з’являються симптоми «ефекту маси» (сильний головний біль або обмеження поля зору) → слід відновити прийом допамінергічних препаратів. Дозволяється проведення МРТ, але без гадолінієвого контрасту. Не існує доказів підвищеного ризику викидня або вроджених вад розвитку у зв’язку з застосуванням бромокриптину або каберголіну під час вагітності. Не рекомендують визначати концентрації ПРЛ у сироватці крові у вагітних з пролактиномою через його фізіологічне підвищення, однак дуже значне підвищення концентрації ПЛР (>22,5 нмоль/л [500 мкг/л]), зазвичай свідчить про ріст пролактиноми, та після виключення макропролактинемії може бути також показом для призначення допамінергічного препарату.
3. У перинатальному періоді може виникнути інсульт пухлини, що часто призводить до самовиліковування аденоми.