Ми прагнемо й надалі безкоштовно надавати цей тип контенту. На жаль, коштів на це більше немає.
Без Вашої допомоги нам доведеться закрити проект до кінця 2024 року.
Зробіть пожертвуКоментар: Piotr Grzanka
Скорочення: АБЛА — алергічний бронхолегеневий аспергільоз, АЦТД — активний цикл техніки дихання, БЕ — бронхоектази, ВІЛ — вірус імунодефіциту людини, КТ — комп’ютерна томографія, КТВР — комп’ютерна томографія високої роздільної здатності, ЛЗ — лікарський засіб, НТМБ (non‑tuberculous mycobacteria) — нетуберкульозні мікобактерії, ОФВ1 — об’єм форсованого видиху за першу секунду, РА — ревматоїдний артрит, РГ — рентгенограма, ХОЗЛ — хронічне обструктивне захворювання легень, 6MWT (six minutes walking test) — тест з 6-хвилинною ходьбою, BSI (Bronchiestasis Severity Index) — індекс тяжкості бронхоектазів, BTS — British Thoracic Society, ISWT (incremental shutle walking test) — ступінчастий тест човникової ходьби (шатл-тест), mMRC (modified Medical Research Council) — модифікована шкала для оцінки тяжкості задишки Medical Research Council, OPEP (oscillating positive expiratory pressure) — вібраційний позитивний тиск на видиху
Клінічні настанови British Thoracic Society (BTS), представлені у даній статті, стосуються тактики дій у дорослих пацієнтів із бронхоектазами (БЕ), які проявляються хронічним кашлем або рецидивуючою респіраторною інфекцією та пов’язані з незворотним руйнуванням та розширенням бронхів. Клінічні настанови не стосуються хворих із БЕ, пов’язаними з муковісцидозом, дітей у віці менше 15-ти років ані хворих із БЕ, які утворилися в ході інших легеневих захворювань, особливо інтерстиціальних, оскільки вони найчастіше є безсимптомними. Клінічні настанови розроблено відповідно до методології AGREE II (www.agreetrust.org/resource‑centre/agree‑ii/). Після кожної рекомендації у квадратних дужках наведено її силу за класифікацією SIGN — від A (найсильніша) до D (найслабша).
У клінічних настановах BTS вказано захворюваність БЕ у Великобританії, яку у 2013 році оцінено на 566/100 000 жінок та 486/100 000 чоловіків. Оцінки з різних регіонів світу значно відрізняються. Частота захворюваності БЕ зростає враз із віком.1
Немає рандомізованих досліджень, які б порівнювали ефективність різних методів візуалізації в діагностиці БЕ. Рентгенограма (РГ) грудної клітки має обмежену чутливість та специфічність, методики використання інгаляційних індикаторів не є корисними, тоді як комп'ютерна томографія (КТ) характеризується високою діагностичною ефективністю. КТ також може допомогти у визначенні етіології БЕ. Зазвичай використовується КТ високої роздільної здатності (КТВР), проте конусно-променева КТ, мабуть, є більш точним дослідженням.
Рекомендації
1. У хворих із підозрою на БЕ слід виконати стартову РГ грудної клітки [D].
2. У хворих з їх клінічною підозрою на БЕ для їх підтвердження слід провести КТВР [D].
3. Стартові візуалізаційні дослідження слід виконувати в стабільній фазі захворювання, оскільки отримані на цьому етапі зображення є оптимальними як для потреб діагностики, так і для подальшої порівняльної оцінки [C].
Практичні вказівки
БЕ — це розширення просвіту бронха, яке визначається як ≥1 із нижче наведених ознак:
1) бронхо-судинне співвідношення >1 (внутрішній просвіт дихальних шляхів порівнюючи з відповідним йому просвітом легеневої судини)
2) відсутність поступового зменшення діаметра бронхів у напрямку до периферії
3) бронхи візуалізуються на відстані <1 см від ребрової частини парієтальної плеври або прилягають до середостінної частини парієтальної плеври.
Непрямими ознаками БЕ є:
1) потовщення бронхіальних стінок
2) накопичення слизу в бронхах
3) мозаїчна перфузія/повітряна пастка, що візуалізуються на КТ під час видиху.
КТ показує розширення просвіту бронхів у порівнянні з діаметром супутньої артерії. Розширення може супроводжуватися потовщенням бронхіальної стінки, а також затримкою секрету в просвіті бронхів. Ступінь бронхіальної деформації може бути різним. Невеликі розширення просвіту нормального бронха — це циліндричні БЕ (рис. 1). Вони можуть зустрічатися у здорових людей віком >65-ти років. Співвідношення діаметра просвіту бронха до діаметра просвіту артерії також може збільшуватися при легеневій гіпертензії, коли розвивається артеріоспазм. У такій ситуації симптом недостатнього звуження просвіту бронха в міру його віддалення від воріт легені (рис. 2) є більш специфічним. У разі прогресування змін розвиваються варикозні БЕ (рис. 3), просвіт яких нерегулярно розширений, у зв'язку з чим іноді вони нагадують нитку перлин. У результаті подальшого руйнування утворюються кістозні БЕ діаметром навіть до декількох сантиметрів. У разі інфекції/колонізації в них може накопичуватися рідина (рис. 4). У деяких випадках КТ-картина вказує на ймовірну причину або наслідки БЕ, наприклад, алергічний бронхолегеневий аспергільоз (рис. 5), мікобактеріоз (рис. 6), первинну циліарну дискінезію, дефіцит α1-антитрипсину, синдром Вільямса-Кемпбелла (рис. 7), наявність стороннього тіла в бронхіальному дереві або фіброз легень (рис. 8). Іноді підозра на захворювання може спиратись на непрямі симптоми, видимі на КТ легенів (рис. 9).
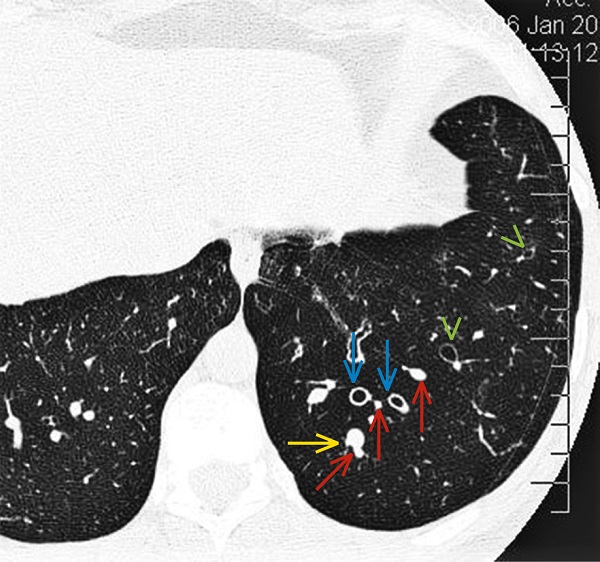
Рисунок 1. Циліндричний бронхоектаз. Просвіт розширеного бронха (зелені стрілки) ширший від супровідної артерії (червона стрілка). Стінки деяких змінених бронхів потовщені (сині стрілки); в поодинокому бронху розширений просвіт заповнений секретом (жовта стрілка)
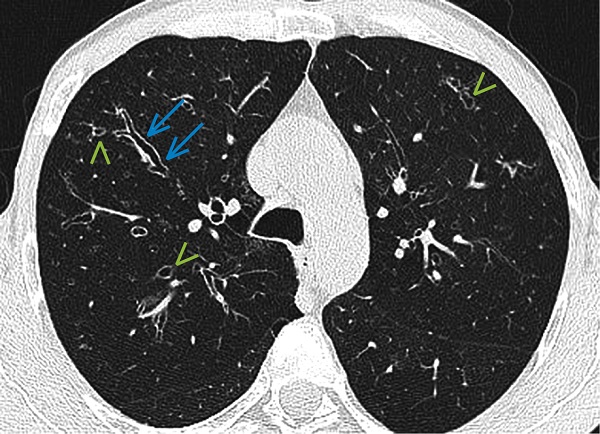
Рисунок 2. Циліндричний бронхоектаз. КТ візуалізує недостатнє звуження просвіту бронха у дистальному напрямку (сині стрілки); зелені стрілки показують бронхоектази в інших ділянках
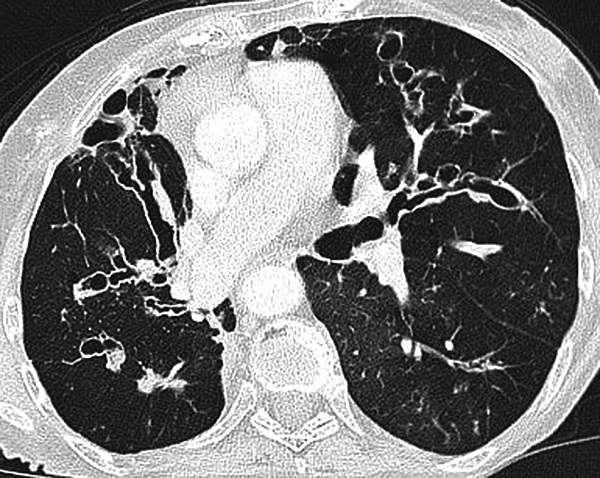
Рисунок 3. Варикозний бронхоектаз
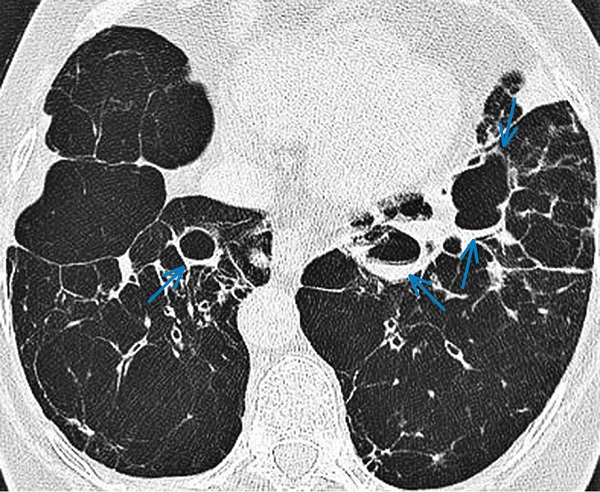
Рисунок 4. Кістозний бронхоектаз. Кістозно розширені бронхи (сині стрілки) у VII сегменті правої легені та в ділянці язичка лівої легені
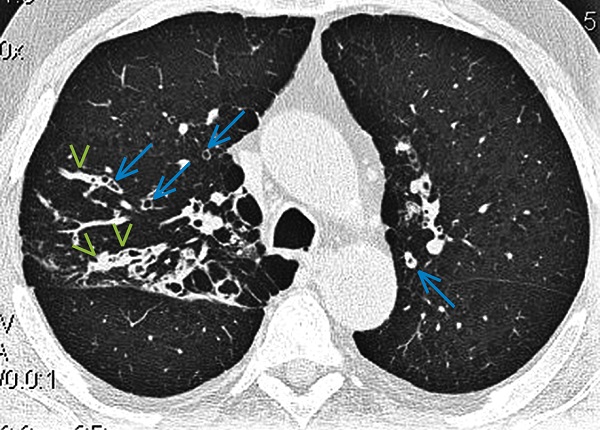
Рисунок 5. Алергічний бронхолегеневий аспергільоз. КТ у хворого на ХОЗЛ і астму, з еозинофілією периферичної крові, візуалізує у верхніх частках обох легень сегментарні бронхоектази (сині стрілки) i сегментарне ураження просвіту бронхів (зелені стрілки)
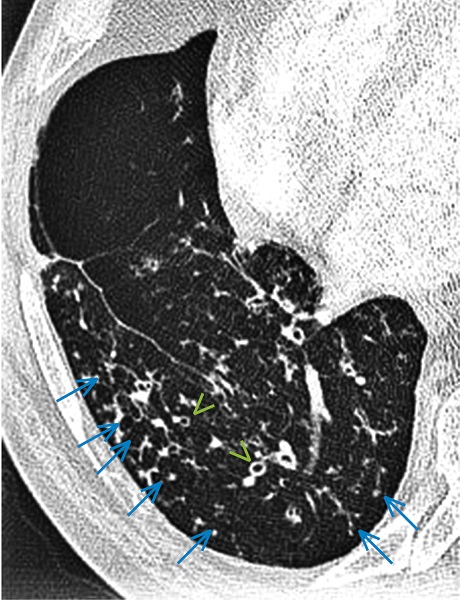 Рисунок 6. Мікобактеріоз легень. КТ у хворого з загостренням ХОЗЛ візуалізує сегментарні бронхоектази (зелені стрілки) та інтралобулярні вузлики, розміщені по ходу дрібних бронхів – симптом "дерева в бруньках" (сині стрілки)
Рисунок 6. Мікобактеріоз легень. КТ у хворого з загостренням ХОЗЛ візуалізує сегментарні бронхоектази (зелені стрілки) та інтралобулярні вузлики, розміщені по ходу дрібних бронхів – симптом "дерева в бруньках" (сині стрілки)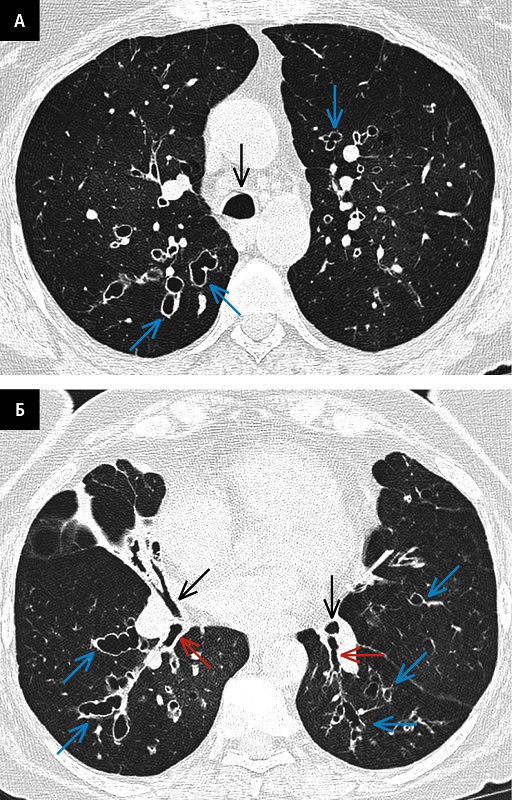
Рисунок 7. У хворої з синдромом Вільямса-Кемпбелла КТ візуалізує нормальну картину трахеї та лобарних (чорні стрілки) i сегментарних (червоні стрілки) бронхів. Дефект хрящового шару в стінці субсегментальних бронхів, що призводить до розширення їх просвіту
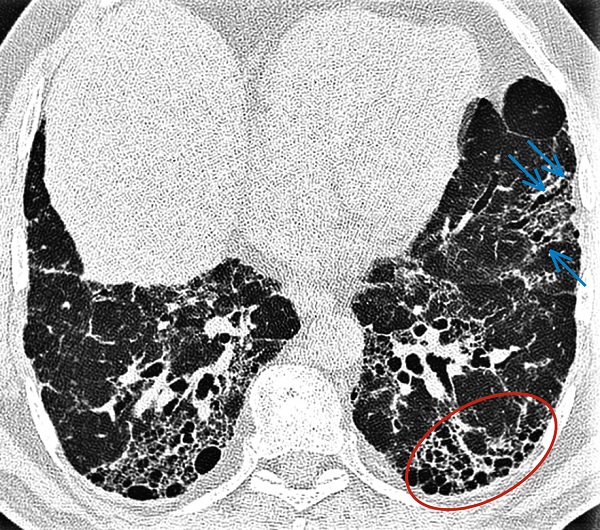
Рисунок 8. Інтерстиціальна пневмонія з ознаками фіброзу у хворого на ідіопатичний фіброз легень. Візуалізуються ділянки завершеного фіброзу (ділянки "стільникової легені"; овал) та ділянки менш поширеного фіброзу, на яких наявні тракційні бронхіолоектази (сині стрілки)
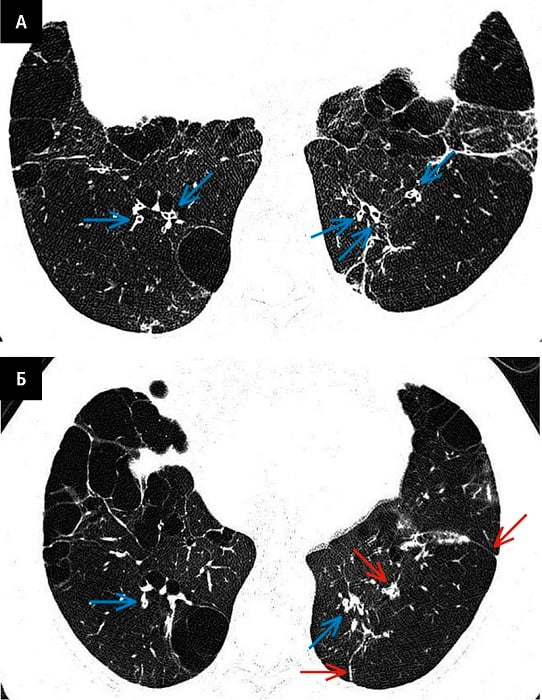
Рисунок 9. Непрямі ознаки бронхоектазів на КТ-картині у 78–річної хворої на ХОЗЛ з деструктивною бульозною емфіземою і дихальною недостатністю. A — КТ-картина на вдиху візуалізує потовщення стінок незначно розширених бронхів (сині стрілки). Б — КТ-картина у кінці фази видиху вказує на дифузні ділянки повітряної пастки (червоні стрілки)
Найчастіший симптом БЕ — продуктивний кашель.
До причин БЕ належать:
1) хронічне обструктивне захворювання легень (ХОЗЛ) — у хворих на ХОЗЛ, яке співіснує з БЕ, спостерігається відкашлювання мокротиння у більшій кількості, частіші і тяжчі загострення, гірша функція легень, вища концентрація маркерів запалення в плазмі крові та частіша колонізація потенційно патогенними мікроорганізмами і Pseudomonas aeruginosa
2) дефіцит α1‑антитрипсину (особливо фенотип PiZZ)
3) астма (особливо астма, яка важко піддається лікуванню)
4) зараження вірусом імунодефіциту людини (ВІЛ) або HTLV‑1
5) ревматоїдний артрит (РА); БЕ можуть розвинутись раніше, ніж симптоми артриту
6) інші захворювання сполучної тканини (синдром Шегрена, синдром Марфана, анкілозуючий спондиліт, системний червоний вовчак), запальні захворювання кишківника, інфекційні захворювання (кір, кашлюк, туберкульоз, пневмонія; особливо, якщо симптоми виникли невдовзі після зараження).
Питання про доцільність проведення діагностики БЕ слід розглядати у пацієнтів із:
1) хронічним відкашлюванням слизисто-гнійного або гнійного секрету, особливо якщо є інші суттєві фактори ризику [D]
2) РА і з хронічним, продуктивним кашлем або рецидивуючими інфекціями [C]
3) ХОЗЛ (в стабільному періоді захворювання) з частими загостреннями (≥2/рік) і позитивним результатом посіву мокротиння на наявність P. aeruginosa [B]
4) запальними захворюваннями кишечника і з хронічним продуктивним кашлем [C].
Якщо є підозра на БЕ, діагностику в цьому напрямку слід також розглянути у пацієнтів із груп ризику:
1) хворих на ХОЗЛ (в стабільному періоді захворювання), у разі хронічного продуктивного кашлю з наявністю потенційно патогенних мікроорганізмів у мокротинні або з ≥2-ма загостреннями протягом 12-ти місяців
2) хворих на тяжку або погано контрольовану астму
3) хворих з ВІЛ-інфекцією в анамнезі, після трансплантації органа чи кісткового мозку, або після імуносупресивного лікування з приводу лімфоми чи васкуліту, у яких спостерігається хронічний продуктивний кашель або рецидивні респіраторні інфекції
4) хворих на хронічний синусит, у яких спостерігається хронічний продуктивний кашель або рецидивні респіраторні інфекції
5) хворих на системне захворювання сполучної тканини, у яких спостерігається хронічний продуктивний кашель або рецидивні респіраторні інфекції
6) у здорових осіб із кашлем, що зберігається >8-ми тижнів, особливо з відкашлюванням секрету або з факторами ризику БЕ в анамнезі.
Дані, що підтверджують доцільність діагностики з метою визначення етіології БЕ, надходять з досліджень низької або середньої якості. Припускається, що у пацієнтів із вперше діагностованими БЕ слід провести діагностику щодо наявності імунодефіциту гуморальної ланки та алергічного бронхолегеневого аспергільозу (АБЛА). Проведення діагностики щодо причин БЕ і діагностування первинної циліарної дискінезії, AБЛА або муковісцидозу впливає на подальшу тактику ведення пацієнта.
1. Щоб визначити причину БЕ, необхідно виконати наступні дослідження:
1) зібрати анамнез щодо супутніх (таких як РА, ХОЗЛ, астма, гастроезофагеальна рефлюксна хвороба і запальні захворювання кишечника) або перенесених захворювань, які можуть сприяти розвитку БЕ [C]
2) загальний аналіз крові з мікроскопією мазка, загальний IgE в сироватці крові, специфічні IgE до Aspergillus fumigatus (або шкірні прик-тести на гіперчутливість до антигенів A. fumigatus) [D]
3) визначення в сироватці крові концентрації імуноглобуліну G (IgG), імуноглобуліну A (IgA) і імуноглобуліну M (IgM) [C].
2. У всіх пацієнтів слід розглянути необхідність визначення титру антитіл до капсульних полісахаридів Streptococcus pneumoniae у рамах діагностики імунодефіциту гуморальної ланки. У пацієнтів із низьким титром антитіл слід застосувати 23-валентну вакцину проти пневмококової інфекції, а потім через 4–8 тижнів провести його повторну оцінку [D].
3. У пацієнтів із раннім дебютом БЕ, чоловічим безпліддям, мальабсорбцією або панкреатитом нез'ясованої етіології слід виконати дослідження з метою виключення муковісцидозу [B].
4. Пацієнти з порушеннями функції дихальної системи в неонатальному періоді, симптомами з боку дихальної системи, що виникають з дитинства, рецидивуючим середнім отитом, хронічним синуситом або чоловічим безпліддям, повинні бути обстежені на предмет первинної циліарної дискінезії [A].
5. У всіх пацієнтів з БЕ слід провести бактеріологічне та мікологічне дослідження мокротиння [D].
1. У пацієнтів із ідіопатичними БЕ цей діагноз повинен бути верифікований за допомогою проведення діагностики з метою виявлення етіології бронхоектазів, особливо, якщо перебіг захворювання погіршується або у разі його раннього дебюту (у віці <50-ти років).
2. Визначення ревматоїдного фактора, антитіл до циклічних цитрулінованих пептидів (АЦЦП), антинуклеарних антитіл (ANA) і антитіл до цитоплазми нейтрофілів (ANCA) слід розглядати у пацієнтів із супутніми проявами артриту, захворювання сполучної тканини і/або васкуліту.
3. У пацієнтів із супутньою емфіземою цілої часточки в нижніх частках легень слід розглянути питання про діагностику з метою виключення дефіциту α1-антитрипсину.
4. Дослідження для виявлення гастроезофагеального рефлюксу і аспірації шлунково-кишкового вмісту показані лише у пацієнтів із симптомами або іншими ознаками, що викликають таку підозру.
5. Бронхоскопію слід розглядати у пацієнтів із обмеженою формою захворювання (із залученням частки або сегмента легені), щоб виключити інтрабронхіальне ураження або присутність чужорідного тіла в дихальних шляхах.
6. У пацієнтів із БЕ і накопиченням секрету слід розглянути необхідність бронхоскопії з аспірацією секрету.
7. У всіх пацієнтів із БЕ і підвищеною концентрацією імуноглобулінів у плазмі крові слід виконати електрофорез білків плазми.
8. У пацієнтів із БЕ і клінічними ознаками, на основі яких можна запідозрити ретровірусне захворювання, слід зважити проведення дослідження на наявність ВІЛ-інфекції.
Доступні два інструменти для оцінки тяжкості перебігу БЕ: BSI (Bronchiestasis Severity Index — табл. 1) і FACED (табл. 2).2,3 Вони допомагають оцінити ризик смерті, а BSI також надає інформацію про захворюваність, ризик госпіталізації та виникнення загострень. Обидві шкали не враховують супутні захворювання, проте вони можуть бути корисні при прийнятті терапевтичних рішень.
|
|
Категорії |
Бали |
|
вік, роки |
<50 50–69 70–79 >80 |
0 2 4 6 |
|
індекс маси тіла (ІМТ), кг/м2 |
<18,5 ≥18,5 |
2 0 |
|
об’єм форсованого видиху за першу секунду (ОФВ1), % належного |
>80 50–80 30–49 <30 |
0 1 2 3 |
|
госпіталізація впродовж останніх 2 років |
ні так |
0 5 |
|
кількість загострень впродовж останніх 12 місяців |
0 1–2 ≥3 |
0 0 2 |
|
модифікована шкала для оцінки тяжкості задишки Medical Research Council (mMRC) |
1–3 4 5 |
0 2 3 |
|
колонізація P. aeruginosa |
ні так |
0 3 |
|
колонізація іншими патогенами, ніж P. aeruginosa |
ні так |
0 1 |
|
радіологічні зміни |
уражені <3 частки уражені ≥3 частки або кістозні бронхоектази в будь-якій з часток |
0 1 |
|
0–4 бали — легке захворювання (ризик смерті 2,8 %/рік) 5–8 балів — середньотяжке захворювання (ризик смерті 4,8 %/рік) >9 балів — тяжке захворювання (ризик смерті 10,5 %/рік) | ||
|
|
Категорія |
Бали |
|
об’єм форсованого видиху за першу секунду (ОФВ1), % належного |
<50 ≥50 |
2 0 |
|
вік, роки |
≤70 років >70 років |
0 2 |
|
колонізація P. aeruginosa |
ні так |
0 1 |
|
радіологічні зміни |
1–2 частки >2 часток |
0 1 |
|
модифікована шкала для оцінки тяжкості задишки Medical Research Council (mMRC) |
1–2 3–4 |
0 1 |
|
0–2 бали — легке захворювання 3–4 бали — середньотяжке захворювання 5–7 балів — тяжке захворювання | ||
1. Chandrasekaran R., Aogáin M.M., Chalmers J.D. і співавт. Geographic variation in the aetiology, epidemiology and microbiology of bronchiectasis. BMC Pulm. Med., 2018; 18: 83
2. https://www.bronchiectasis.eu/severity‑assessment (доступ: 22.10.2019)
3. https://bronchiectasis.com.au/assessment/medical/faced‑score (доступ: 22.10.2019)