Ми прагнемо й надалі безкоштовно надавати цей тип контенту. На жаль, коштів на це більше немає.
Без Вашої допомоги нам доведеться закрити проект до кінця 2024 року.
Зробіть пожертвуКонсультація: Maciej Kupczyk
Скорочення: АСІТ — алерген-специфічна імунотерапія, ГК — глюкокортикоїд(и), іГК — інгаляційний глюкокортикоїд, ЛЗ — лікарський(і) засіб(оби), ОФВ1 (FEV1) — об’єм форсованого видиху за першу секунду (forced expiratory volume in 1st second), ATS (American Thoracic Society) — Американське торакальне товариство, ERS (European Respiratory Society) — Європейське респіраторне товариство, FENO (fractional exhaled nitric oxide) — концентрація оксиду азоту у видихуваному повітрі, GINA (Global Initiative for Asthma) — Глобальна Ініціатива щодо ведення астми, LABA (long‑acting beta‑agonist) — β2-агоніст тривалої дії, LAMA (long‑acting muscarinic antagonist) — антихолінергічний ЛЗ тривалої дії, NAEPP — National Asthma Education and Prevention Program, SABA (short‑acting β2‑agonist) — β2-агоніст короткої дії.
У цій статті представлена обрана, суттєва для клінічної практики інформація з авторитетних діючих клінічних настанов щодо цього захворювання, розроблених Глобальною ініціативою щодо ведення астми (GINA)1, Національною програмою з навчання та профілактики астми (NAEPP)2, а також Європейським респіраторним товариством і Американським торакальним товариством (ERS/ATS)3.
Для рекомендацій, для яких такі дані були доступні, в квадратних дужках вказані сила (С — сильна, Сл — слабка) і якість даних (В — висока, Ср — середня, Н — низька), на яких вони засновані.
Принципи діагностики астми в клінічних настановах GINA залишаються незмінними. Для діагностування захворювання, крім наявності його клінічних симптомів, необхідно виявити бронхообструкцію при спірометрії (≥1-й в процесі діагностики) та підтвердити її варіабельність. Виняток становлять випадки, коли показане термінове лікування, а діагноз, відмінний від астми, малоймовірний; в такій ситуації діагностичні дослідження слід провести через 1–3 місяці від початку лікування.
У клінічних настановах NAEPP є рекомендації щодо використання визначення концентрації оксиду азоту в видихуваному повітрі (FENO). Пацієнтам, у яких дані з суб'єктивного та об’єктивного обстеження і спірометрії не дозволяють поставити точний діагноз астми (а також тим, хто не може виконати спірометрію), пропонується враховувати визначення FENO в діагностичному процесі [Сл/Ср]. Підвищена концентрація FENO збільшує, а низька — знижує ймовірність астми, проте це дослідження неспецифічне — воно не дозволяє підтвердити або виключити дане захворювання. Згідно з клінічними настановами NAEPP, у пацієнтів, які не приймають глюкокортикостероїди (ГК) з FENO >50 ppm, ймовірно спостерігається еозинофільне запалення дихальних шляхів, а ймовірність діагностування астми і доброї відповіді на лікування інгаляційними глюкокортикостероїдами (іГК) вища. У пацієнтів з FENO <25 ppm ймовірність астми нижча (це може бути астма без еозинофільного запалення або астма, лікована ГК), а специфічність дослідження для значень <20 ppm оцінюється в 77 %. Результат в діапазоні 25–50 ppm зазвичай мало допомагає в діагностиці. Дослідження завжди слід інтерпретувати разом з клінічною оцінкою і результатами інших додаткових досліджень. У деяких клінічних ситуаціях визначення FENO також може використовуватися в якості маркера дотримання пацієнтом рекомендацій лікаря (тобто підтвердження того, чи приймає пацієнт призначені іГК).
Пацієнтам з алергічною астмою, щодо яких є сумніви у зв’язку з вибором лікування, моніторингом або підбором протизапального лікування на підставі даних суб'єктивного та об’єктивного обстеження і спірометрії, пропонується включити визначення FENO як складову моніторингу та стратегії підбору лікування, що включає часту оцінку пацієнтів [Сл/Н]. Використання FENO не рекомендується в якості єдиного інструменту для оцінки контролю захворювання, прогнозування ризику загострень або оцінки ступеня їх тяжкості [С/Н]. Визначення FENO може використовуватися як доповнення до інших методів моніторингу астми (оцінка симптомів, функціональні дослідження і оцінка дотримання рекомендацій); у деяких пацієнтів це може знизити ризик загострень без значного впливу на інші показники контролю захворювання. Однак необхідний частий клінічний контроль з оцінкою FENO (кожні 2–3 міс.). У клінічних настановах NAEPP перераховано кілька клінічних ситуацій, в яких це може бути корисно; перш за все, слід пам'ятати про пацієнтів з недостатньо контрольованою астмою, які приймають іГК (у монотерапії або з β2-агоністом тривалої дії [LABA], монтелукастом або омалізумабом), а також про пацієнтів із алергічною астмою.
Слід пам'ятати, що вимірювання FENO не є клінічно корисним у пацієнтів із астмою без Th2-залежного запалення.
У клінічні настанови GINA була внесена суттєва зміна, згідно з якою схема лікування астми розділяється на 2 напрямки, що базуються на:
1) прийомі препарату, який містить іГК і формотерол, тільки «за потребою» або регулярно та «за потребою» (тактика, якій надається перевага)
2) регулярному застосуванні іГК (в режимі «за потребою» лише на 1-й сходинці), при необхідності з LABA і/або іншими ЛЗ. Перед тим, як вибрати цей напрямок лікування, слід оцінити ймовірність того, що пацієнт буде дотримуватися рекомендацій щодо регулярного щоденного застосування контролюючого захворювання ЛЗ.
В обох випадках при необхідності можна додавати інші ЛЗ: антилейкотрієновий ЛЗ, антихолінергічний ЛЗ тривалої дії (LAMA) або застосувати алерген-специфічну імунотерапію (АСІТ) сублінгвальним препаратом (рис. 1). Також варто відзначити, що ця зміна є результатом не нових наукових даних, а повторної інтерпретації раніше доступних результатів клінічних досліджень.

Рисунок 1. Сходинковий підхід до лікування астми у хворих віком 12 років і старших відповідно до клінічних настанов GINA
У клінічних настановах NAEPP концепція сходинкового підходу до лікування астми є подібною (рис. 2), проте є деякі відмінності. В якості лікування в режимі «за потребою» на всіх сходинках пацієнти повинні приймати β2-агоніст короткої дії (SABA), якщо не вказано інше (пацієнтам, які приймають тільки «за потребою» або регулярно і «за потребою» препарат, що містить формотерол та іГК). Альтернативне лікування відповідно до NAEPP можна вибрати тоді, коли пацієнт вже приймає його і його астма контролюється, а лікування, якому надається перевага, недоступне або занадто дороге, а також у тому разі, якщо пацієнт віддає перевагу альтернативному лікуванню.
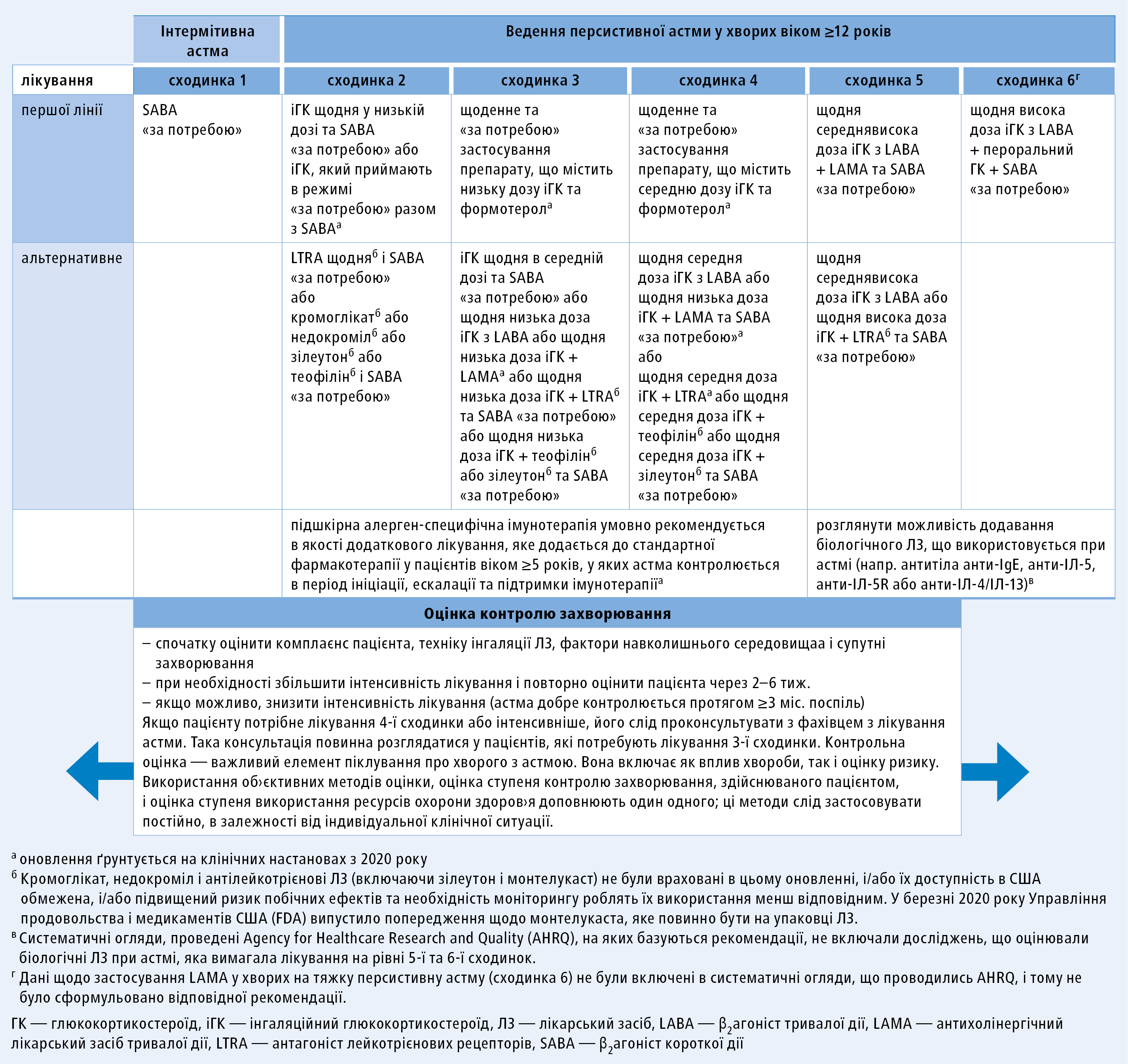
Рисунок 2. Сходинковий підхід до лікування астми у хворих віком 12 років і старших відповідно до клінічних настанов National Asthma Education and Prevention Program (джерело: National Heart, Lung, and Blood Institute; National Institutes of Health; U.S. Department of Health and Human Services)
У пацієнтів, яким потрібне лікування 5-ї або 6-ї сходинки, можна розглянути можливість застосування біологічних ЛЗ.
Як і в клінічних настановах GINA, перед збільшенням інтенсивності лікування слід оцінити комплаєнс пацієнта, техніку інгаляції, вплив шкідливих факторів навколишнього середовища та супутні захворювання.
Варто відзначити кілька важливих відмінностей. У клінічних настановах GINA зазначено, що всі хворі на астму повинні отримувати протизапальний ЛЗ, навіть якщо симптоми захворювання виникають дуже рідко. Ця рекомендація заснована, зокрема, на результатах досліджень, які показують, що навіть у цих пацієнтів спостерігаються загострення хвороби, яким можна запобігти, застосовуючи протизапальний ЛЗ; тому з 2019 року GINA не рекомендує використовувати SABA як ЛЗ «за потребою» в монотерапії. Крім того, протизапальне лікування у цих пацієнтів пов'язано зі зниженням симптомів, порівнюючи з застосуванням одного тільки SABA. Клінічні настанови NAEPP як і раніше допускають лікування найлегших форм інтермітивної астми тільки за допомогою застосування SABA «за потребою».
Інша відмінність стосується ведення пацієнтів, у яких регулярного прийому та застосування «за потребою» препарату, що містить формотерол та низьку дозу іГК, недостатньо: в клінічних настановах GINA рекомендується регулярне застосування препарату, що містить формотерол та середню дозу іГК, а також застосування «за потребою» подібного комбінованого препарату, але який містить низьку дозу іГК. У той же час клінічні настанови NAEPP рекомендують як регулярне, так і в режимі «за потребою» застосування препарату, що містить формотерол та іГК в середній дозі. Відмінності щодо АСІТ обговорюються нижче.
У клінічних настановах NAEPP підкреслюється, що схема лікування не повинна замінювати прийняття клінічних рішень (це скоріше вказівка, а не абсолютна рекомендація) для окремих пацієнтів, а також врахування уподобань пацієна при виборі лікування. Незалежно від рекомендованої схеми лікування, догляд за пацієнтом вимагає регулярного контролю (симптомів, факторів, що впливають на ефективність лікування, техніки інгаляції ЛЗ, дотримання рекомендацій), коригування тактики дій (оптимізація модифікувальних факторів ризику, навчання пацієнтів, зміна фармакотерапії) і контролю відповіді на лікування (вираженість симптомів, виникнення загострень, побічні ефекти ЛЗ, функціональні дослідження легень, задоволеність пацієнта).
Нижче наведені окремі рекомендації з клінічних настанов NAEPP для конкретних варіантів фармакологічного лікування.
Пацієнтам з легкою або помірно тяжкою формою астми, які, ймовірно, дотримуються рекомендацій по лікуванню, пропонується не збільшувати дозу іГК «за потребою» у відповідь на посилення симптомів або погіршення ПШВ [Сл/Н].
У пацієнтів з помірно тяжкою або тяжкою астмою перевагу віддають застосуванню препарату, що містить формотерол та іГКС, регулярно та «за потребою», аніж регулярному лікуванню:
1) іГК в більш високих дозах [С/В]2) іГК в тій же дозі в комбінації з LABA [С/В]
3) іГК у вищій дозі в комбінації з LABA [Сл/В].
Принципи застосування LAMA:
1) LAMA може бути доданий до іГК, якщо LABA не застосовується [Сл/Ср]
2) віддають перевагу додаванню до іГК LABA , а не LAMA [Сл/Ср]
3) LAMA може бути доданий до іГК і LABA (в порівнянні з продовженням лікування іГК і LABA) [Сл/Ср].
Нижче наведено рекомендації з клінічних настанов NAEPP щодо окремих немедикаментозних методів лікування.
У клінічних настановах NAEPP допускається використання підшкірної АСІТ у пацієнтів із алергічної астмою легкою або середньої тяжкості, за умови, що захворювання є контрольованим під час ініціації і продовження АСІТ [Сл/Ср]. АСІТ — цінний метод впливу на природний перебіг атопічних захворювань, але пропонується застосовувати його з обережністю у пацієнтів з астмою через ризик серйозних побічних ефектів. АCІТ може розглядатися у пацієнтів, у яких астма недостатньо контролюється, а ймовірною причиною є алергія на інгаляційні алергени (рекомендується збільшити інтенсивність лікування перед початком АСІТ, щоб досягти контролю над астмою і знизити ризик побічних ефектів АСІТ), а також у пацієнтів, y яких астма знаходиться під контролем, але бажано зменшити інтенсивність лікування. АСІТ не можна застосовувати у пацієнтів із тяжкою астмою.
У клінічних настановах GINA згадуються переваги АСІТ (зменшення вираженості симптомів та інтенсивності лікування), але підкреслюється ризик побічних ефектів і необхідність спостереження за пацієнтом після введення кожної дози препарату алергену, тому підшкірна АСІТ чітко не рекомендується (пропонується враховувати баланс переваг та ризику і незручностей для пацієнта).
Клінічні настанови NAEPP і клінічні настанови GINA значно відрізняються щодо підходу до сублінгвальної АСІТ. У клінічних настановах GINA це метод, який можна розглядати у пацієнтів із алергією на кліщів домашнього пилу зі стійкими симптомами, незважаючи на застосування низьких або середніх доз іГК (лікування 2-ї або 3-ї сходинки) і ОФВ1 >70 % належного значення. Було відзначено, що переваги сублінгвальної АСІТ, ймовірно, помірні (невелике зниження дози іГК), але це безпечний метод, оскільки побічні ефекти обмежуються в основному ротовою порожниною та дистальнішими відділами шлунково-кишкового тракту. У свою чергу, в клінічних настановах NAEPP експерти виступають проти використання цього методу у пацієнтів з астмою, але це слабка рекомендація, заснована на даних середньої якості. У такому разі, якщо розглядається питання про застосування АСІТ, який шлях введення препарату алергену слід вибрати? Безсумнівно, підшкірна АСІТ має більш сприятливий вплив на симптоми і використання ЛЗ, а також може полегшити перебіг захворювання, проте менш зручна для пацієнтів і пов'язана з ризиком серйозних побічних ефектів. Сублінгвальна АСІТ, ймовірно, має незначний позитивний вплив на симптоми захворювання, але є набагато безпечнішою. При виборі різновиду АСІТ у пацієнта з астмою слід враховувати клінічну ситуацію і уподобання пацієнта.
Бронхіальна термопластика може бути розглянута у пацієнтів, яким залежить на потенційних перевагах (поліпшення якості життя, невелике зниження ризику загострень) і в яких не викликає занепокоєння короткострокове погіршення симптомів і невідомий ризик віддалених ускладнень [Сл/Н]. Подібна позиція була описана в клінічних настановах GINA, які допускають розгляд цього методу у пацієнтів із тяжкою астмою, але також підкреслюють, що віддалені наслідки бронхіальної термопластики невідомі. Після публікації цих клінічних настанов були опубліковані результати дослідження, яке показало, що позитивні ефекти процедури зберігалися протягом як мінімум 10 років при прийнятному профілі безпеки.4
Пропонується не використовувати методи зниження впливу алергенів у людей, які не сенсибілізовані або не мають симптомів після експозиції до алергену [Сл/Н].
Пацієнтам, у яких розвиваються симптоми астми після впливу певних алергенів в закритому приміщенні, пропонується впровадження комплексної програми зниження впливу алергенів [Сл/Н].
Пацієнтам, у яких розвиваються симптоми астми після впливу алергенів тарганів або гризунів, пропонуються багатокомпонентні методи зниження впливу алергенів (можл. в якості елемента багатокомпонентних програм) [Сл/Н].
Пацієнтам з алергією на кліщів домашнього пилу пропонується використовувати непроникні для алергенів кліщів чохли для матраців і подушок тільки як частину комплексної програми, а не як єдине втручання [Сл/Ср].
Обидва документи (NAEPP і GINA) підкреслюють, що використання деяких методів зниження експозиції до алергенів може бути важким для пацієнтів, тому рішення щодо їх рекомендації слід приймати індивідуально з урахуванням думки пацієнта. Принагідно слід пам'ятати, що більшість втручань, використовуваних окремо, неефективні.
Астма, яка важко піддається лікуванню, визначається як захворювання, яке не контролюється попри використання LABA і середніх або високих доз іГК, або вимагає LABA та високих доз іГК для підтримки контролю. Тяжка астма — це астма, яка залишається неконтрольованою, незважаючи на використання LABA і високих доз іГК (або другого контролюючого захворювання ЛЗ або перорального ГК відповідно до клінічних настанов ERS/ATS) пацієнтом, що виконує рекомендації лікаря, або контроль якої погіршується при спробі зниження інтенсивності такого лікування.
Перед інтенсифікацією лікування у пацієнтів, яким важко досягти контролю над астмою, слід:
1) підтвердити діагноз астми; диференційна діагностика повинна включати хронічне обструктивне захворювання легенів, захворювання серця, низьку фізичну витривалість, індуковану обструкцію гортані, хронічний риносинусит зі стіканням секрету по задній стінці глотки, гастроезофагеальний рефлюкс, бронхоектази, кашель, спричинений застосуванням інгібіторів ангіотензинперетворюючого ферменту, та інші більш рідкісні захворювання (напр. трахеобронхомаляцію)
2) оцінити фактори, які можуть погіршити симптоми і/або збільшити ризик загострень або погіршити якість життя пацієнта, такі як:
а) техніка інгаляції інгаляційних препаратів (до 80 % пацієнтів припускаються помилок); при кожному відвідуванні перевіряти, чи правильно пацієнт здійснює інгаляцію ЛЗ
б) дотримання пацієнтом рекомендованого лікування (більшість пацієнтів не дотримуються рекомендацій)
в) супутні захворювання, в т. ч. гастроезофагеальна рефлюксна хвороба, ожиріння, хронічний риносинусит, обструктивне апное сну
г) модифікувальні фактори ризику і тригери симптомів — тютюнопаління, вплив навколишнього середовища, контакт з алергенами в осіб, які страждають на алергію (алергію слід оцінювати за допомогою шкірних тестів або визначення специфічних IgE), застосування таких ЛЗ, як β-блокатори або нестероїдні протизапальні препарати
д) зловживання SABA — використання ≥3-х упаковок на рік пов'язано з підвищеним ризиком відвідування відділення невідкладної допомоги або госпіталізації (незалежно від виникнення симптомів), а використання ≥12-ти упаковок на рік — з підвищеним ризиком смерті
е) побічні ефекти застосовуваних ЛЗ, особливо пероральних ГК та іГК, виникнення яких погіршує комплаєнс пацієнта
є) тривога, пригнічений настрій, соціальні проблеми.
Нижче наведені рекомендації з клінічних настанов ERS/ATS щодо лікування тяжкої астми.3
У пацієнтів із тяжкою астмою, недостатньо контрольованою, або яка вимагає застосування пероральних ГК, пропонується використовувати лікування, спрямоване проти інтерлейкіну 5 (ІЛ-5) (бенралізумаб, меполізумаб, реслізумаб) [Сл/Н]. Було виявлено, що ці ЛЗ знижують ризик загострень астми, використання меполізумабу або бенралізумабу дозволило знизити дозу перорального ГК. Однак вплив кожного з трьох ЛЗ на контроль астми, функцію легенів і якість життя був невеликим і не перевищував мінімальної клінічно значущої різниці.
У пацієнтів із тяжкою астмою та загостреннями в анамнезі пропонується розглянути можливість лікування анти-ІЛ-5, якщо кількість еозинофілів в крові складає ≥150/мкл [Сл/Н].
У пацієнтів із тяжкою астмою у віці ≥12 років, відібраних для лікування моноклональним антитілом проти IgE (омалізумабом), для виявлення пацієнтів з більшою ймовірністю клінічної відповіді на лікування пропонуються наступні граничні значення: кількість еозинофілів ≥260/мкл [Сл/Н], FENO ≥19,5 ppb [Сл/Н]. Оскільки ці порогові значення не оцінювалися в рандомізованих дослідженнях, до них слід підходити з обережністю, оскільки не можна виключити, що лікування омалізумабом також принесе користь пацієнтам з більш низькими значеннями цих параметрів.
Пацієнтам з астмою та загостреннями, незважаючи на застосування іГК і LABA, рекомендується додати тіотропій [С/Ср]. Таке лікування поліпшує контроль астми, збільшує час до наступного загострення астми і може поліпшити функцію легенів. У клінічних настановах ERS/ATS згадується тільки тіотропій, але тепер уже для лікування астми зареєстровано більшу кількість ЛЗ з групи LAMA (доступних у вигляді комбінованих препаратів), що зазначено в оновлених клінічних настановах GINA.
У пацієнтів із тяжкою астмою, яка залишається неконтрольованою, незважаючи на застосування лікування 5-ї сходинки згідно GINA, пропонується спроба тривалого використання макроліду для зниження частоти загострень [Сл/Н]. Тривале лікування макролідом знижує частоту загострень, і ефект, ймовірно, буде подібним у пацієнтів з еозинофілією і у пацієнтів без еозинофілії. Однак клінічно значимого впливу на контроль астми або якість життя пацієнтів не спостерігалося. Можливим побічним ефектом є діарея. Незважаючи на побоювання з приводу подовження інтервалу QT і розвитку порушень слуху, ці побічні ефекти не спостерігалися в клінічних дослідженнях. В клінічних настановах GINA рекомендація щодо макроліду була сформована в 2021 році, обмежуючись азитроміцином (через наявних даних клінічних досліджень), який рекомендується використовувати в дозі 500 мг 3 рази на тиждень. Таке лікування можна розглянути у пацієнтів з рецидивуючими загостреннями, незважаючи на застосування LABA та високих доз іГК. Перед початком лікування макролідом і через місяць його застосування рекомендується виконувати ЕКГ.
У хворих на тяжку форму астми з еозинофілією і тяжку стероїдозалежну астму (незалежно від кількості еозинофілів в крові) рекомендується додати до лікування дупілумаб [Сл]. Це ЛЗ, який є моноклональним анти-ІЛ-4/ІЛ-13 антитілом, знижує частоту загострень у пацієнтів із помірно тяжкою і тяжкою астмою, а також дозволяє знизити дозу перорального ГК у стероїдозалежних пацієнтів. Також було виявлено, що ЛЗ має позитивний вплив на контроль захворювання, функцію легенів і якість життя пацієнтів.
1. Global Initiative for Asthma: Global strategy for asthma management and prevention, 2021. www.ginasthma.org (доступ: 9.07.2021)
2. Expert Panel Working Group of the National Heart, Lung, and Blood Institute (NHLBI) administered and coordinated National Asthma Education and Prevention Program Coordinating Committee (NAEPPCC) i wsp.: 2020 focused updates to the asthma management guidelines: a report from the National Asthma Education and Prevention Program Coordinating Committee Expert Panel Working Group. J. Allergy Clin. Immunol., 2020; 146: 1217–1270
3. Holguin F., Cardet J.C., Chung K.F. i співавт.: Management of severe asthma: a European Respiratory Society/American Thoracic Society guideline. Eur. Respir. J., 2020; 55: 1900588
4. Chaudhuri R., Rubin A., Sumino K. i співавт.: Safety and effectiveness of bronchial thermoplasty after 10 years in patients with persistent asthma (BT10+): a follow‑up of three randomised controlled trials. Lancet Respir. Med., 202 1; 9: 457–466