Introducción
El plasma convaleciente es uno de los tratamientos de la COVID-19 que más se dieron a conocer al principio de la pandemia. La mayoría de las opciones terapéuticas propuestas al principio resultaron ineficaces, p. ej. la cloroquina, el ritonavir/lopinavir o la azitromicina. El uso de remdesivir sigue siendo polémico, puesto que no influye en la mortalidad. Los únicos fármacos que han conseguido reducir la mortalidad son los glucocorticoides, unos fármacos de uso generalizado, verificados y baratos.
El plasma convaleciente ha generado debates acalorados, en parte debido a la información sobre su eficacia transmitida por los grandes medios de comunicación.
Sin embargo, ¿existen pruebas científicas reales de que el plasma convaleciente sea eficaz? Intentaremos responder a esta pregunta en este artículo breve acerca de los ensayos clínicos aleatorizados que han evaluado la eficacia del plasma convaleciente en los pacientes con COVID-19.
Ensayos
| Tabla. Características generales de los 6 ensayos aleatorizados considerados en el artículo | |||||
|---|---|---|---|---|---|
| Ensayo | Población | Intervención | Control | Criterio de valoración principal | Observaciones |
| Agarwal, 2020 (India) | Pacientes con COVID-19 moderada (PaO2/FiO2 = 200-300 mm Hg o RR >24/min con una SpO2 ≤93 % durante la respiración de aire atmosférico (N=235) |
2 dosis de plasma convaleciente de 200 ml cada una con 24 h de separación + SOC (N=229) |
SOC | Criterio de valoración compuesto (progresión a enfermedad grave o mortalidad en 28 días) (N=228) 19 % vs. 18 % RR 1,04, IC 95 % 0,71-1,54 |
Mayor riesgo de error debido a la falta de carácter ciego de la intervención |
| Avendaño-Solá, 2020 (España) | Pacientes hospitalizados por COVID-19 (N=43) |
Plasma convaleciente administrado inmediatamente después de la aleatorización + SOC (N=38) |
SOC | Porcentaje de pacientes que fallecieron o necesitaron hospitalización y VNI, ONAF, VMI u OMEC al día 15 del ensayo. 0 % vs. 14,0 %, p=0,57 |
1) Mayor riesgo de error debido a la falta de carácter ciego de la intervención 2) Prepublicación: la publicación no se ha revisado 3) La falta de eventos en el grupo de intervención a causa de la conclusión prematura del ensayo dificulta sacar conclusiones |
| Gharbharan, 2020 (Países Bajos) | Pacientes hospitalizados con COVID-19 confirmado en <96 h desde la aleatorización (N=43) |
Plasma convaleciente administrado el día de la aleatorización (existía la posibilidad de administrar una segunda unidad en caso de que no hubiera respuesta clínica y se mantuviera el resultado positivo de la RT-PCR 5 días después de la aleatorización) + SOC (N=43) |
SOC | Mortalidad hasta el alta hospitalaria o hasta el día 60 desde la aleatorización 14 % vs. 26 % OR 0,95, IC de 95 % 0,20-4,67 |
1) Mayor riesgo de error debido a la falta de carácter ciego de la intervención 2) El ensayo se interrumpió de forma prematura porque la mayoría de pacientes ya tenía una alta concentración inicial de anticuerpos anti-SARS. Por lo tanto, la prevalencia de la mortalidad puede haberse subestimado (solo 32 pacientes estuvieron sometidos a una observación de 60 días). 3) Prepublicación: la publicación no se ha revisado. |
| Al Qahtani, 2020 (Baréin) | Pacientes hospitalizados con COVID-19, hipoxemia (SpO2 ≤92 % durante la respiración de aire atmosférico, PaO2 <60 mm Hg en la gasometría de sangre arterial o PaO2/FiO2 ≤300) y necesidad de oxigenoterapia
y neumonía confirmada por pruebas radiológicas (N=20) |
2 dosis de plasma convaleciente de 200 ml administradas con intervalo de 24 h + SOC (N=20) |
SOC | Necesidad de administrar ventilación invasiva 20 % vs. 30 % RR 0,67, IC de 95 % 0,22-2,0 |
1) Mayor riesgo de error debido a la falta de carácter ciego de la intervención 2) Prepublicación: la publicación no se ha revisado |
| Li, 2020 (China) | Pacientes hospitalizados con COVID-19 grave o potencialmente mortal* y neumonía confirmada por pruebas radiológicas (N=52) |
Plasma convaleciente en dosis de 4-13 ml/kg de la masa corporal del paciente + SOC (N=51) |
SOC | Tiempo hasta la mejoría clínica en 28 días (alta hospitalaria o descenso de 2 puntos en una escala del 1 [alta] al 6 [muerte]) 51,9 % vs. 43,1 % HR 1,40, IC de 95 % 0,79-2,49 |
Mayor riesgo de error debido a la falta de carácter ciego de la intervención |
| Simonovich, 2020 (Argentina) | Pacientes hospitalizados con COVID-19 grave (SpO2 <93 % en reposo durante la respiración de aire atmosférico, PaO2/FiO2 <300 mm Hg o aumento de 2 puntos con respecto al valor inicial en las escalas SOFA o SOFA modificada) y neumonía confirmada por pruebas radiológicas (N=228) |
Plasma convaleciente (N=105) |
Placebo | Estado clínico 30 días después de la intervención en una escala del 1 (muerte) al 6 (alta con recuperación completa del estado de salud original) OR 0,83, IC 95 % 0,52-1,35 |
)¡Único ensayo con carácter ciego de la intervención! |
* Forma grave: ≥30 respiraciones/min; SpO2 en reposo ≤93 % durante la respiración de aire atmosférico; o Pao2/Fio2 ≤300. Forma potencialmente mortal: insuficiencia respiratoria que precise de ventilación mecánica, shock u otro fallo orgánico que requiera seguimiento en la UCI. Abreviaturas: ONAF — oxigenoterapia nasal de alto flujo, OR — odds ratio, RR — riesgo relativo, SOC — estándar de atención, VMI — ventilación mecánica invasiva, VNI — ventilación no invasiva | |||||
Observaciones
1) Grupos pequeños de pacientes en la mayoría de ensayos
2) Solo el ensayo de Simonovich tenía un carácter ciego
3) Alta variabilidad de los criterios de valoración principales
4) La mitad de los ensayos aún no se han publicado, por lo que los informes presentados por los autores no se han revisado
Valoración de la eficacia del plasma convaleciente en criterios de valoración seleccionados
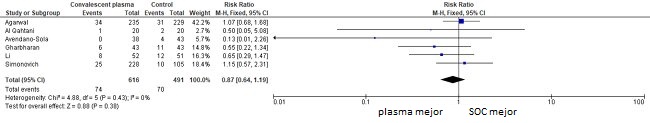
1) Mortalidad a 28-30 días
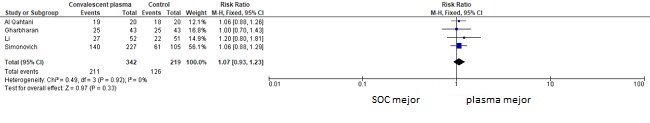
2) Mejoría del estado clínico a 28-30 días
Comentario
El análisis de los resultados conjuntos de los 6 ensayos aleatorizados disponibles deja bastante claro que el uso de plasma de convalecientes en el tratamiento de los pacientes con COVID-19 no produce beneficios. No ha sido posible demostrar que reduzca la mortalidad ni aumente la frecuencia de mejoría clínica en una observación de 28-30 días. Cabe destacar que esto se ha observado tanto en los estudios con pacientes graves tratados fuera de la UCI como con enfermos críticos. No obstante, antes de sacar conclusiones debemos considerar las limitaciones de los ensayos de tales características (grupos reducidos, falta de ciego en 5 de 6 ensayos, conclusión prematura en 2 de 6 ensayos y el hecho de que la mitad de los estudios citados no se han revisado y se han publicado como prepublicación). La eficacia del plasma convaleciente en el tratamiento de los pacientes con COVID-19 debería quedar aclarada una vez se publiquen los resultados de dos grandes ensayos aleatorizados, el RECOVERY (administración programada de plasma convaleciente a 2500 pacientes) y el REMAP-CAP (a 1000 pacientes).
Así pues, teniendo en cuenta el riesgo de complicaciones postransfusionales y los datos científicos disponibles, ¿merece la pena administrar plasma convaleciente a los pacientes con COVID-19? Parece que, actualmente, la administración de plasma convaleciente debería limitarse únicamente a los ensayos clínicos.
Bibliografía:
1. Agarwal A, Aparna M, Gunjan K, et al., Convalescent plasma in the management of moderate covid-19 in adults in India: open label phase II multicentre randomised controlled trial (PLACID Trial), BMJ, 2020; 371 :m39392. Li L, Zhang W, Hu Y, et al., Effect of Convalescent Plasma Therapy on Time to Clinical Improvement in Patients With Severe and Life-threatening COVID-19: A Randomized Clinical Trial, JAMA, 2020;324:460-470.
3. Simonovich VA, Burgos Pratx LD, Scibona P, et al., A Randomized Trial of Convalescent Plasma in Covid-19 Severe Pneumonia, N Engl J Med., 2020. Online ahead of print.
4. Gharbharan A, Jordans CCE, Geurts van Kessel C, et al., Convalescent plasma for COVID-19: a randomized clinical trial. (https://www.medrxiv.org/content/10.1101/2020.07.01.20139857v1).Preprint.
5. Avendaño-Solá C, Ramos-Martinez A, Muñez-Rubio E, et al., Convalescent plasma for COVID-19: a multicenter, randomized clinical trial. https://www.medrxiv.org/content/10.1101/2020.08.26.20182444v3).Preprint.
6. AlQahtani M, Abdulrahman A, Almadani A, et al., Randomized controlled trial of convalescent plasma therapy against standard therapy in patients with severe COVID-19 disease. https://www.medrxiv.org/content/10.1101/2020.11.02.20224303). Preprint.
 Español
Español
 English
English
 українська
українська