Siglas y abreviaturas: AINE — antinflamatorios no esteroideos, EPOC — enfermedad pulmonar obstructiva crónica, LABA (longacting betaagonist) — agonista β2 de acción prolongada, LAMA (longacting muscarinic antagonist) — fármaco anticolinérgico de acción prolongada, SABA (shortacting β2-agonist) — agonista de acción corta, TC — tomografía computarizada
Introducción
En las guías de la Global Initiative for Asthma (GINA) 2019 se utilizan las siguientes definiciones
1) asma no controlada: asma que cumple ≥1 de los siguientes criterios:
a) mal control sintomático (síntomas frecuentes o necesidad de administración frecuente de fármacos inhalados a demanda, limitación de la actividad vital por causa del asma, despertares nocturnos debidos al asma)
b) exacerbaciones frecuentes (≥2/año) que requieren el uso de glucocorticoides orales o exacerbaciones graves que requieren hospitalización (≥1/año)
2) asma difícil de tratar: asma no controlada a pesar de un tratamiento de 4 o 5 grado según la GINA (dosis moderada o alta de glucocorticoide inhalado y otro fármaco controlador o glucocorticoide oral: véase fig. 1) o que requiere dicho tratamiento con el fin de controlar bien los síntomas y reducir el riesgo de exacerbaciones
3) asma grave (subcategoría de asma difícil): asma que permanece descontrolada a pesar de que el paciente cumpla el tratamiento optimizado de máxima intensidad y a pesar de que estén controlados los factores concomitantes que puedan agravar la enfermedad, o que se intensifica tras la reducción de dosis altas de fármacos.
El asma difícil y el asma grave constituyen respectivamente un 17 % y un 3,7 % de los casos de asma en adultos. El asma difícil empeora considerablemente la calidad de vida de los enfermos, debido a una mayor intensidad de los síntomas, así como de exacerbaciones frecuentes, impredecibles y graves. No menos importantes son los efectos adversos derivados del uso de los fármacos para el asma, sobre todo de los glucocorticoides orales, cuya administración se asocia p. ej. con una ganancia ponderal y con un aumento del riesgo para el desarrollo de diabetes mellitus, osteoporosis y catarata.
Actuación en enfermos con sospecha de asma grave
1. Confirmación del diagnóstico del asma: una anamnesis detallada y la exploración física son básicos para determinar si los síntomas presentes son típicos del asma. En función de la situación clínica y de los síntomas predominantes, al realizar el diagnóstico diferencial, hay que tener en cuenta
1) en pacientes con disnea: enfermedad pulmonar obstructiva crónica (EPOC), obesidad, enfermedades cardíacas, bajo rendimiento físico
2) en pacientes con tos: obstrucción laríngea inducida, rinosinusitis crónica con caída de moco por la pared posterior de la faringe, reflujo gastroesofágico, bronquiectasia, tos causada por la toma de un inhibidor de la enzima convertidora de la angiotensina
3) en pacientes que refieren sibilancias: obesidad, EPOC, traqueobroncomalacia y obstrucción laríngea inducible.
Hay que realizar una espirometría con prueba de reversibilidad, con el fin de confirmar la variabilidad de la obstrucción bronquial. Si el resultado es negativo, hay que considerar repetir la prueba durante la presentación de los síntomas. Si el resultado de la espitometría es normal, se puede valorar la evaluación de la variabilidad del flujo espiratorio máximo, y si el enfermo puede interrumpir los broncodilatadores se puede valorar realizar un test de provocación.
2. Valoración de los factores que pueden intensificar los síntomas, aumentar el riesgo de exacerbaciones o empeorar la calidad de vida. Entre tales factores se encuentran
1) Técnica de inhalación de fármacos (un 80 % comete errores). Durante casa visita hay que pedir al paciente que demuestre cómo se administra el fármaco por vía inhalatoria.
2) Cumplimiento del tratamiento recomendado (subóptimo en 2 de cada 3 enfermos). Se puede preguntar al paciente con qué frecuencia toma el fármaco (p. ej. cuántas veces a la semana), así como identificar los eventuales problemas que puedan dificultar el tratamiento, p. ej. precio elevado del fármaco o temor a la aparición de efectos adversos.
3) Enfermedades concomitantes, p. ej. reflujo gastroesofágico, obesidad, rinosinusitis crónica, apnea obstructiva del sueño.
4) Factores de riesgo y factores desencadenantes de los síntomas que pueden modificarse: tabaquismo, exposición ambiental, contacto con alérgenos en alérgicos (la presencia de alergia debe confirmarse mediante pruebas cutáneas o examen de IgE específicas), uso de fármacos, tales como β-bloqueantes o antinflamatorios no esteroideos (AINE).
5) Abuso de agonistas β2 de acción corta (SABA): la toma de ≥3 envases anuales se asocia a un aumento del riesgo de visitas a urgencias o de hospitalización (independientemente de la presentación de síntomas), mientras que la toma de ≥12 envases/año se asocia a un riesgo elevado de muerte.
6) Efectos adversos de los fármacos administrados (sobre todo de glucocorticoides orales e inhalados), cuya aparición empeora el cumplimiento de las recomendaciones del médico.
7) Inquietud, depresión del estado anímico, problemas sociales.
3. Optimización del tratamiento del asma
1) Educar al enfermo y elaborar junto con él un plan de actuación en asma.
2) Optimizar el tratamiento farmacológico: evaluar la técnica de inhalación de fármacos, valorar los fármacos adicionales, p. ej. agonista β2 de acción prolongada (LABA), tiotropio, fármaco antileucotrieno (si no han sido utilizados hasta el momento). En los enfermos con exacerbaciones del asma hay que utilizar un glucocorticoide inhalado con formoterol en un inhalador que contenga los dos fármacos, tanto en el tratamiento regular, como a demanda; dicho tratamiento reduce el riesgo de exacerbaciones.
3) Valorar el uso de métodos no farmacológicos, p. ej. abandono del hábito tabáquico (necesario en todos los enfermos), actividad física, reducción del peso corporal en pacientes con sobrepeso/obesidad, vacunación contra la gripe, limpieza de las secreciones retenidas en las vías respiratorias.
4) Tratar las enfermedades concomitantes que tienen influencia negativa en el asma y en el control/eliminación de los factores de riesgo modificables.
5) Considerar un tratamiento inicial con una alta dosis de glucocorticoide inhalado, si no se ha hecho antes.
4. Si después de 3-6 meses de optimizar el tratamiento sigue con criterios de asma no controlada, hay que diagnosticar un asma grave y remitir al enfermo a un especialista.
5. Si después de 3-6 meses de optimizar el tratamiento el asma está completamente controlada, hay que intentar reducir la intensidad del tratamiento. En primer lugar hay que reducir la dosis del glucocorticoide oral o suspenderlo, a continuación suspender los demás fármacos adicionales, y al final reducir la dosis del glucocorticoide inhalado (¡sin suspenderlo!). Si después de desescalar el tratamiento de manera adecuada se observa pérdida del control del asma o exacerbación de la enfermedad, hay que diagnosticar asma grave, remitir al enfermo al especialista y restituir el tratamiento anterior eficaz.
Actuación en enfermos con asma grave
La actuación en enfermos con asma grave depende sobre todo del fenotipo de la enfermedad, que debe evaluarse durante el tratamiento con alta dosis del glucocorticoide inhalado o la dosis efectiva menor de glucocorticoide oral (preferiblemente antes de introducir el glucocorticoide oral), ya que estos fármacos rápidamente eliminan los rasgos de inflamación tipo 2. En la inflamación tipo 2 participan p. ej. IL-4, IL-5 e IL-13, secretadas a consecuencia del contacto con un alérgeno, o inducido por virus, bacterias o agentes irritativos, estimulantes de la producción de IL-25, IL-33 y linfoproteínas del estroma tímico por las células epiteliales de las vías respiratorias. Se presenta en un 50 % de los enfermos con asma grave, y en los demás en el proceso inflamatorio predominan p. ej. neutrofilias. Hay que determinar si el enfermo cumple los criterios de la inflamación respiratoria resistente al tratamiento tipo 2 (tabla 1). Algunas de las siguientes etapas consisten en
1) Volver a realizar un diagnóstico detallado de las enfermedades concomitantes y considerar diagnósticos alternativos. En función de la situación clínica debería valorarse la realización de las siguientes pruebas
a) de imagen: p. ej. radiografía de tórax, tomografía computarizada (TC) de alta resolución, tomografía de los senos paranasales, ecocardiograma
b) de laboratorio: hemograma de sangre periférica, proteína C-reactiva, IgG, IgA, IgM, IgE, anticuerpos precipitantes contra Aspergillus, anticuerpos contra el citoplasma de neutrófilos (ANCA), NT-proBNP
c) orientadas hacia enfermedades alérgicas: pruebas cutáneas, IgE sérica específica
d) pruebas respiratorias funcionales, p. ej. determinación de la capacidad de difusión pulmonar (DLCO).
2) Valorar las indicaciones para el apoyo psicosocial e introducirlo en caso de necesidad.
3) Considerar la introducción de cuidados multidisciplinares.
4) Incentivar al paciente a participar en un registro de enfermos o en ensayos clínicos.
Si el enfermo no cumple los criterios de la infección tipo 2, hay que volver a considerar las cuestiones básicas en el tratamiento de asma grave:
1) considerar el tratamiento alternativo
2) evaluar la técnica inhalatoria
3) evaluar la eficacia del tratamiento de enfermedades concomitantes significativas, y presentación de efectos adversos de fármacos
4) recomendar evitar los factores desencadenantes del asma, tales como humo de tabaco, alérgenos, sustancias irritativas.
Además deberíamos
1) considerar un diagnóstico adicional: examen de esputo inducido, TC de alta resolución, broncoscopia
2) volver a optimizar el tratamiento adicional: considerar la administración de un fármaco anticolinérgico de acción prolongada (LAMA), antibiótico macrólido, glucocorticoide oral a dosis baja, así como suspender los fármacos que no conllevan una mejoría
3) valorar la realización de termoplastia bronquial.
Si el enfermo cumple los criterios de inflamación respiratoria tipo 2 a pesar de la administración de glucocorticoide inhalado a dosis alta, hay que:
1) evaluar de manera objetiva el cumplimiento de las recomendaciones, p. ej. sobre la base de la información que nos aportan las recetas médicas realizadas o a través del uso de inhalador con contador electrónico de dosis, o determinar la concentración sanguínea de prednisona
2) en la evaluación clínica/diagnóstico diferencial tener en cuenta sobre todo la aspergilosis broncopulmonar alérgica, enfermedad respiratoria alta agudizada por los antinflamatorios no esteroideos (asma inducida por ácido acetilsalicílico), rinosinusitis crónica, y dermatitis atópica
3) considerar aumentar la dosis de glucocorticoide inhalado durante 3-6 meses
4) determinar la posibilidad de realizar una terapia biológica dirigida.
Si la terapia biológica dirigida no está disponible, hay que:
1) considerar aumentar la dosis de glucocorticoide inhalado, si no se ha hecho antes
2) considerar añadir fármacos adicionales no biológicos (LABA, tiotropio, fármaco antileucotrieno, antibiótico macrólido)
3) considerar añadir un glucocorticoide oral (hay que recordar la profilaxis de los efectos adversos de la corticoterapia oral)
4) suspender los fármacos adicionales ineficaces.
El tratamiento biológico se debe tener en consideración en enfermos en los que, a pesar de la administración de glucocorticoide inhalado a dosis alta y/o glucocorticoide oral se presentan exacerbaciones del asma, así como ante la presencia de biomarcadores de alergia (en tales situaciones se puede utilizar el omalizumab) o infección eosinofílica (indicación para la administración de mepolizumab, benralizumab, reslizumab o dupilumab). Hay que evaluar si el enfermo cumple los criterios de inclusión al programa farmacológico, así como elegir un fármaco óptimo, incluyendo los factores predictivos de buena respuesta al tratamiento, su coste, frecuencia y vía de administración, además de tener en cuenta las preferencias del enfermo (tabla 2). La terapia biológica debe administrarse durante 4 meses, y a continuación hay que evaluar la respuesta. En caso de dudas en cuanto a la eficacia de este tratamiento, hay que prolongar el período de prueba hasta 6-12 meses.
En ausencia de eficacia del tratamiento biológico hay que suspenderlo y eventualmente considerar la administración de otro fármaco biológico (si el enfermo cumple los criterios básicos), y volver a evaluar la respuesta al tratamiento pasados 4 meses. Si el enfermo sigue sin responder al tratamiento biológico, hay que suspender el segundo fármaco biológico, así como volver a:
1) realizar el diagnóstico diferencial, evaluar la técnica inhalatoria, el cumplimiento de las recomendaciones, enfermedades concomitantes, efectos adversos de los fármacos administrados, así como ofrecer apoyo psicológico (en caso de indicaciones)
2) evaluar el fenotipo de la enfermedad, y según los resultados de la prueba de esputo inducido, realizar pruebas de apoyo apropiadas (hay que valorar la broncoscopia), así como considerar la inclusión de métodos adicionales de tratamiento (antibiótico macrólido, glucocorticoide oral a dosis baja, termoplastia bronquial
3) suspender todos los fármacos ineficaces (¡no se deben suspender los glucocorticoides inhalados!).
Si se observa buena respuesta al tratamiento biológico, hay que:
1) regularmente cada 3-6 meses controlar la respuesta al tratamiento, incluyendo los síntomas de la enfermedad, la presencia de exacerbaciones, la actividad respiratoria, los efectos adversos de los fármacos utilizados, el coste del tratamiento y la satisfacción del paciente
2) considerar la modificación de la farmacoterapia oral: reducción de la dosis/suspensión del glucocorticoide oral, y a continuación suspensión de otros fármacos adicionales
3) considerar la modificación de la farmacoterapia inhalatoria: reducción de la dosis pasados 3-6 meses de su administración (sin embargo, hay que mantener una dosis por lo menos moderada del glucocorticoide inhalado)
4) evaluar con regularidad las indicaciones para continuar el tratamiento biológico.
Tras llegar al control del asma hay que continuamente buscar la optimización del tratamiento, evaluando con regularidad la técnica inhalatoria, el cumplimiento de las recomendaciones médicas, el control de las comorbilidades significativas, las necesidades socioemocionales, así como manteniendo el contacto entre el especialista neumólogo y el médico de familia que cuida del enfermo.
A recordar
El asma grave constituye un 4 % de todos los casos del asma.
Pasos iniciales en caso de problemas con el control del asma:
1) confirmación del control del asma
2) evaluación del cumplimiento de las recomendaciones, incluida la técnica inhalatoria correcta
3) diagnóstico y tratamiento de las enfermedades concomitantes
4) reducción de la exposición a factores de riesgo.
- La actuación en el asma grave depende de la aparición de rasgos de inflamación tipo 2 a pesar del tratamiento con glucocorticoides inhalados.
- En enfermos con inflamación tipo 2 puede considerarse un tratamiento biológico.
|
Recuento de eosinófilos en sangre periférica ≥150/µl FeNO ≥20 ppb Recuento de eosinófilos en el esputo después del contacto con un alérgeno Características clínicas de la intensificación del asma después del contacto con un alérgeno Necesidad de utilizar glucocorticoides oralesb |
|
a Basta con cumplir 1 criterio. |
|
Grupos de fármacos |
Fármacos disponibles |
Dosificación |
Criterios de inclusión |
Factores predictores de buena respuesta |
Efectos adversos |
|
Anticuerpos anti-IgE |
Omalizumab |
VSc cada 2-4 semanas |
Alergia a alérgenos inhalatorios confirmada por pruebas cutáneas o detección de IgE específicos Concentración sérica de IgE y peso corporal lo suficientemente altos (dependiendo de los criterios locales) Número determinado de exacerbaciones del asma (dependiendo de los criterios locales) |
Recuento de eosinófilos en sangre ≥260/µl FeNO ≥20 ppb Presentación de los síntomas del asma después de la exposición a alérgenos Inicio de la enfermedad en la infancia |
Reacción en el lugar de la inyección Anafilaxia en ~0,2 % de los enfermos |
|
Anticuerpos anti-IL-5 o contra receptor de la IL-5 |
Mepolizumab Benralizumab
|
100 mg VSc cada 4 semanas 30 mg VSc cada 4 semanas, después de 3 dosis cada 8 semanas 3 mg/kg iv. cada 4 semanas |
Número adecuado de exacerbaciones del asma (en función de criterios locales) Recuento de eosinófilos en sangre por encima de un determinado nivel |
Alto recuento de eosinófilos en sangre Numerosas exacerbaciones en el último año Inicio de la enfermedad a edad adulta Pólipos nasales Uso de glucocorticoides orales |
Reacción en el lugar de la inyección Con poca frecuencia anafilaxia Riesgo de efectos adversos en general similar que en enfermos que reciben placebo |
|
Anticuerpos contra el receptor de la IL-4 |
Dupilumab |
200 o 300 mg VSc cada 2 semanas (300 mg en caso de coexistencia de dermatitis atópica moderada o grave) |
Número adecuado de exacerbaciones del asma (en función de criterios locales) Recuento de eosinófilos en sangre y concentración de FeNO por encima de un determinado nivel o Necesidad de utilizar glucocorticoides orales |
Alto recuento de eosinófilos en sangre Alta concentración de FeNO |
Reacción en el lugar de la inyección Eosinofilia transitoria en la sangre periférica |
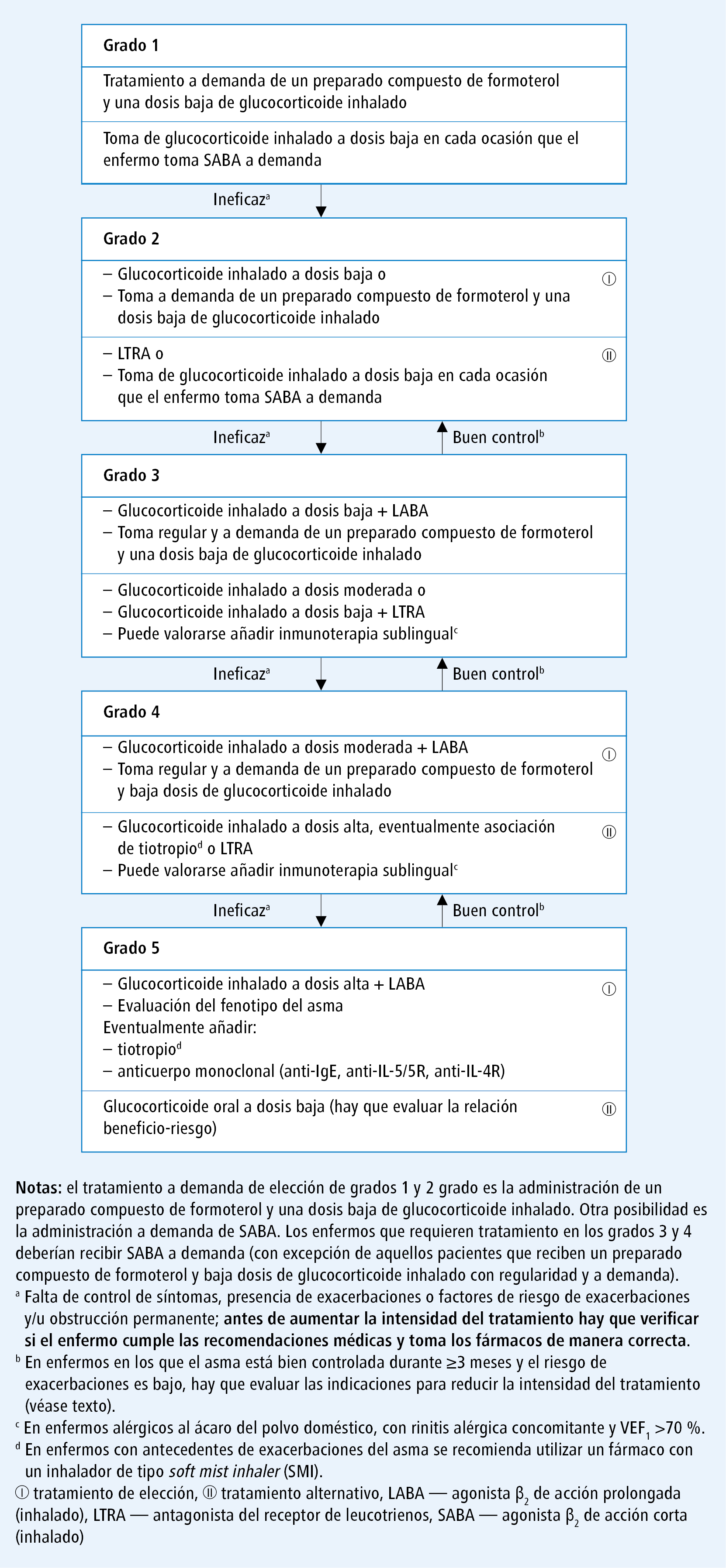
Fig. 1. Grados de tratamiento del asma según GINA 2019
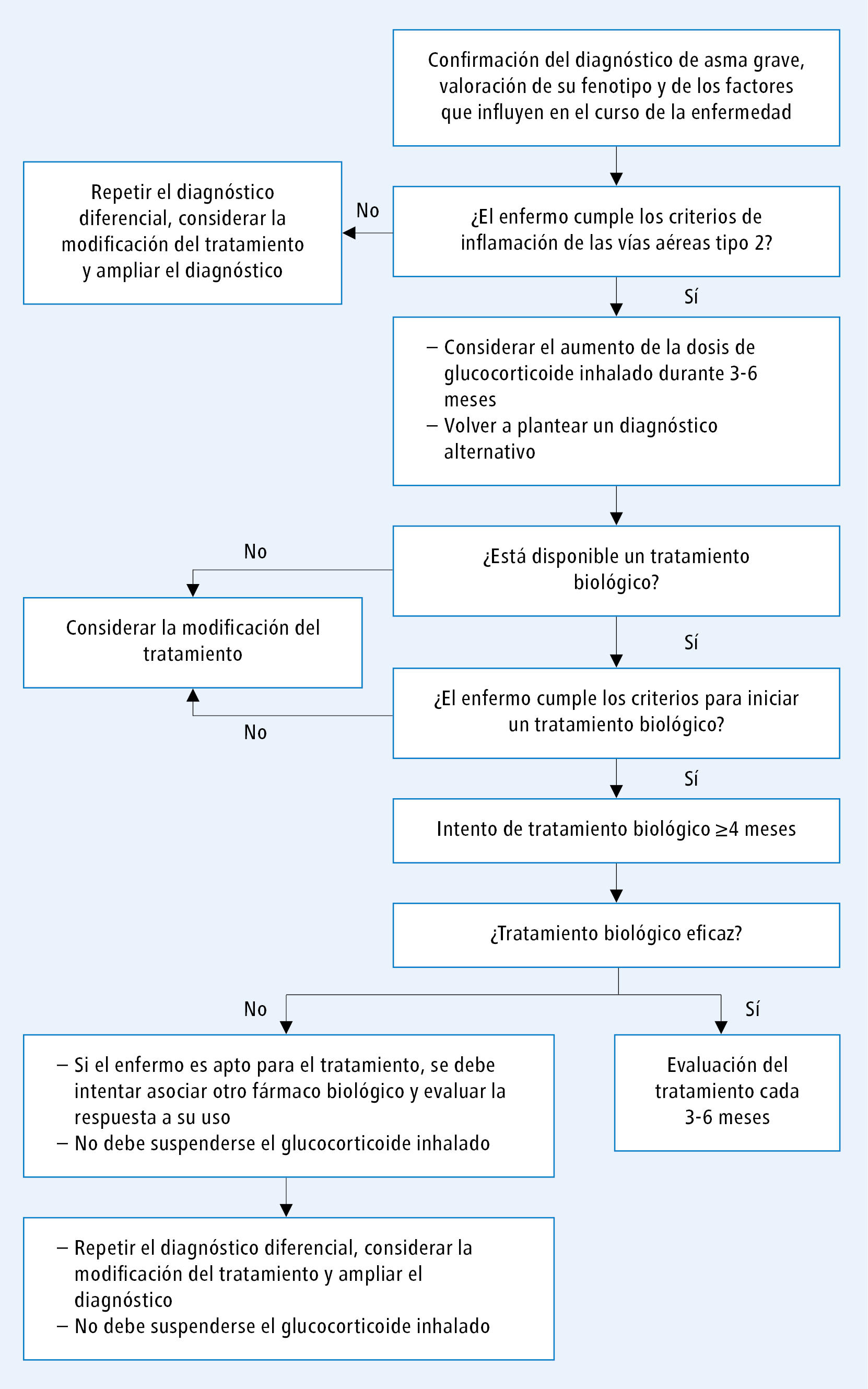
Fig. 2. Algoritmo de actuación en asma grave según la guía GINA 2019
Bibliografía:
1. Hekking P.P., Wener R.R., Amelink M. y cols., The prevalence of severe refractory asthma, J. Allergy Clin. Immunol., 2015, 135: 896-902.2. Difficult-to-treat & severe asthma in adolescent and adult patients. Diagnosis and management. A GINA Pocket Guide for Health Professionals. Global Initiative for Asthma, 2019.
 Español
Español
 English
English
 українська
українська




