Ми прагнемо й надалі безкоштовно надавати цей тип контенту. На жаль, коштів на це більше немає.
Без Вашої допомоги нам доведеться закрити проект до кінця 2024 року.
Зробіть пожертвуВИЗНАЧЕННЯ ТА ЕТІОПАТОГЕНЕЗ вгору
Дифузний токсичний зоб (ДТЗ) — аутоімунне захворювання, при якому аутоантигеном є рецептор до ТТГ (рТТГ). Його активація антитілами АТ-рТТГ призводить до збільшення синтезу та секреції ГЩЗ, що призводить до появи симптомів гіпертиреозу, стимулює ріст щитоподібної залози і розвиток її системи кровопостачання (судинний зоб). Запуск механізмів клітинної відповіді проти даного антигену, що наявний у фібробластах може призводить до посилення секреції прозапальних цитокінів, аутоімунного запалення і розвитку екстратиреоїдних проявів захворювання. Тиреоїдна орбітопатія — група очних симптомів, індукованих імунним запаленням м’яких тканин очниць у перебігу ДТЗ, що призводить до транзиторного або стійкого пошкодження органу зору. Характеризується інтерстиціальним набряком екстраокулярних м’язів, що супроводжується проліферацією фібробластів — це спричиняє періорбітальний набряк, ретракцію повік та екзофтальм, диплопію, пошкодження рогівки та (рідше) компресію зорового нерва. Злоякісний екзофтальм — тяжка форма прогресуючої інфільтраційно-набрякової офтальмопатії з особливо високим ризиком стійких ускладнень.
КЛІНІЧНА КАРТИНАвгору
1. Маніфестна або помірно виражена картина гіпертиреозу розвивається переважно у хворих у віці 20–50 років →розд. 9.2; в осіб літнього віку можуть проявлятися лише симптоми з боку серця; найчастіше у вигляді пароксизмальної або постійної фібриляції передсердь, іноді загострення наявної ішемічної хвороби або серцевої недостатності. У дітей та підлітків симптоми також можуть бути нетиповими, часто спостерігаються розлади поведінки та концентрації, а надмірна нервозність або психотичні розлади можуть бути єдиним проявом захворювання.
Як правило, ДТЗ має перебіг з періодами загострення і ремісії, з наявністю судинного або паренхіматозно-судинного зобу і характерним судинним посиленим шумом при аускультації та характерним зображенням на УЗД →нижче. Може зустрічатися екзофтальм (явна орбітопатія не є обов’язковою умовою для постановки діагнозу ДТЗ), рідше виявляється симптоми аутоімунного запалення шкіри — претібіальна мікседема (тиреоїдна дермопатія розвивається в результаті аутоімунного дерматиту і стимуляції фібробластів, патогномонічний симптом, але рідкісний) і тиреоїдна акропахія (безболісний набряк пальців рук, рідше стоп у поєднанні з піднадкостничним потовщенням кістки; дуже рідкісний симптом).
2. Тиреоїдна орбітопатія: проявляється одночасно з гіпертиреозом, чи пізніше протягом 18 міс., може випереджувати інші симптоми гіпертиреозу, рідко є єдиним симптомом ДТЗ; як виключення, може супроводжувати гіпотиреоз. Хворі скаржаться на біль в очних яблуках, печіння, сльозотечу, зниження гостроти зору, відчуття піску під повіками, світлобоязнь і диплопію; при об’єктивному обстежені виявляються екзофтальм, набряк повік і періорбітальних тканин, гіперемія кон’юнктиви і обмеження рухливості очних яблук. Загроза втрати зору з’являється, коли розвиваються виразки рогівки внаслідок неповного заплющення повік та компресії зорового нерву (спочатку погіршення кольорового зору). Стеатоз періорбітальних тканин і фіброз при запущеному захворюванні призводять до постійних змін зовнішнього вигляду пацієнта.
ДІАГНОСТИКАвгору
ДТЗ може перебігати як явний або субклінічний первинний гіпертиреоз →розд. 9.2, що супроводжується ознаками аутоімунного запалення, які проявляються клінічно, або виявляються допоміжними методами дослідження.
1. Лабораторні дослідження:
1) знижений рівень ТТГ у сироватці і підвищений (рідше — нормальний) рівень вільних ГЩЗ (зазвичай, досить визначення FT4; якщо знаходиться у межах норми — слід визначити FT3). При явному гіпертиреозі значне переважання зростання FT3 над зростанням FT4 є несприятливою прогностичною ознакою — відповідь на антитиреоїдне лікування є гіршою. У фазі ремісії результати гормональних досліджень знаходяться у межах норми;
2) підвищення рівня антитіл до рецепторів ТТГ — підтверджує діагноз (визначте до початку або протягом перших 3 міс. антитиреоїдного лікування), нормалізація свідчить про імунологічну ремісію захворювання;
3) інші лабораторні дослідження — як при гіпертиреозі →розд. 9.2.
2. Візуалізаційні дослідження:
УЗД щитоподібної залози — гіпоехогенність паренхіми, щитоподібна залоза найчастіше збільшена, особливо в передньо-задньому вимірі, з посиленням судинного кровотоку; наявність вогнищевих уражень щитоподібної залози не виключає ДТЗ. У період ремісії захворювання можливий регрес змін і повернення нормального зображення УЗД щитовидної залози.
Сцинтиграфія щитоподібної залози — особливо корисна при наявності вузлів і під час відбору для лікування радіойодом.
КТ очниць (не потребує введення контрастної речовини): оцінка м’яких тканин очниці, її кісткових стінок (що важливо при плануванні декомпресійної операції) і потовщення зовнішніх м’язів очних яблук.
МРТ очниць: оцінка набряку або фіброзу м’язів очного яблука.
1. Діагноз ДТЗ достовірний у наступних випадках:
1) явний або субклінічний гіпертиреоз і підвищення антитіл до рецепторів ТТГ;
2) гіпертиреоз, що супроводжується тиреоїдною орбітопатією з вираженими змінами у м’яких тканинах очниць і/або тиреоїдною дермопатією;
3) гіпертиреоз із судинним зобом, підтвердженим при УЗД (дифузна гіпоехогенність паренхіми, посилений кровотік при кольоровому доплерівському дослідженні) — корисно, якщо ще недоступний результат тесту антитіл до рецепторів ТТГ;
4) ізольована тиреоїдна орбітопатія і підвищення рівня антитіл до рецепторів ТТГ.
2. Діагноз ДТЗ ймовірний, якщо:
1) виникають рецидиви гіпертиреозу, розділені періодами еутиреозу, що тривали >6 міс. без прийому анититиреоїдних ЛЗ;
2) у родині пацієнта з гіпертиреозом зустрічаються випадки ДТЗ, тиреоїдиту Хашимото, або пацієнт має інше аутоімунне захворювання.
Ізольованого підвищення рівня антитіл до рецепторів ТТГ недостатньо для постановки діагнозу ДТЗ (можуть визначатися у родичів пацієнтів з ДТЗ, у яких не розвиваються симптоми захворювання).
Має значення не тільки саме виявлення запалення тканин очниць і встановлення діагнозу «тиреоїдна орбітопатія» (ТO), але, передусім, оцінка, чи тяжкість симптомів вимагає застосування лікування (потребує повного офтальмологічного обстеження і, часто, КТ орбіт).
Класифікація тиреоїдної офтальмопатії бере до уваги активність імунного запалення (за EUGOGO, 2021):
1) легка ТO (з невеликим впливом на щоденне функціонування) — присутні ≥1 з наступних симптомів:
а) незначна ретракція повік <2 мм;
б) незначне ураження періорбітальних м’яких тканин;
в) екзофтальм <3 мм вище норми з урахуванням раси та статі;
г) без диплопії (при втомі або після пробудження), ураження рогівки, що минають під впливом зволожувальних засобів;
2) ТO від середньої до тяжкої, без ризику втрати зору (зі значним впливом на щоденне функціонування) — присутні ≥2 з наступних симптомів:
а) ретракція повік ≥2 мм;
б) помірне або тяжке ураження м’яких тканин орбіти;
в) екзофтальм ≥3 мм вище норми з урахуванням раси та статі;
г) диплопія: непостійна (у крайніх областях поля зору) або постійна (у центрі поля зору або в положенні до читання);
3) ТO дуже тяжкого ступеня з ризиком втрати зору — порушення зору та/або дуже виражені симптоми — спостерігається нейропатія зорового нерва та/або пошкодження рогівки.
Оцінка активності тиреоїдної орбітопатії на підставі вираженості ознак запалення: кількість балів за шкалою Clinical Activity Score (CAS) відповідає сумі виявлених симптомів (симптом наявний — 1 бал; симптом відсутній — 0 балів):
1) спонтанний ретробульбарний біль;
2) біль при погляді вгору або вниз;
3) гіперемія повік;
4) гіперемія кон’юнктив;
5) запалення слізного м’ясця та/або півмісяцевої складки кон’юнктиви;
6) набряк повік;
7) набряк кон’юнктив (хемоз).
На активну ТО вказує значення CAS ≥3/7. Неактивна ТO діагностується при CAS <3.
Три додаткові критерії дозволяють використовувати 10-бальну шкалу в оцінці прогресування захворювання після першого візиту:
8) збільшення екзофтальму на ≥2 мм;
9) зменшення рухливості ока на ≥8°;
10) погіршення гостроти зору за останні 1–3 місяці.
Диференційна діагностика ДТЗ з іншими причинами гіпертиреозу →рис. 9.2-1, табл. 9.2-1. Підвищення рівня антитіл до рецепторів ТТГ підтверджує активність аутоімунного процесу при ДТЗ.
Очні симптоми, що супроводжують неаутоімунний тяжкий гіпертиреоз (визначальне значення має концентрація антитіл до рецепторів ТТГ); якщо екзофтальм однобічний — лімфома очниці, метастази пухлин, гранульома (псевдотумор очниці).
ЛІКУВАННЯвгору
Не існує ефективного етіотропного лікування ДТЗ, застосовується симптоматична терапія гіпертиреозу →рис. 9.2-3 і орбітопатії →розд. 9.2.1.
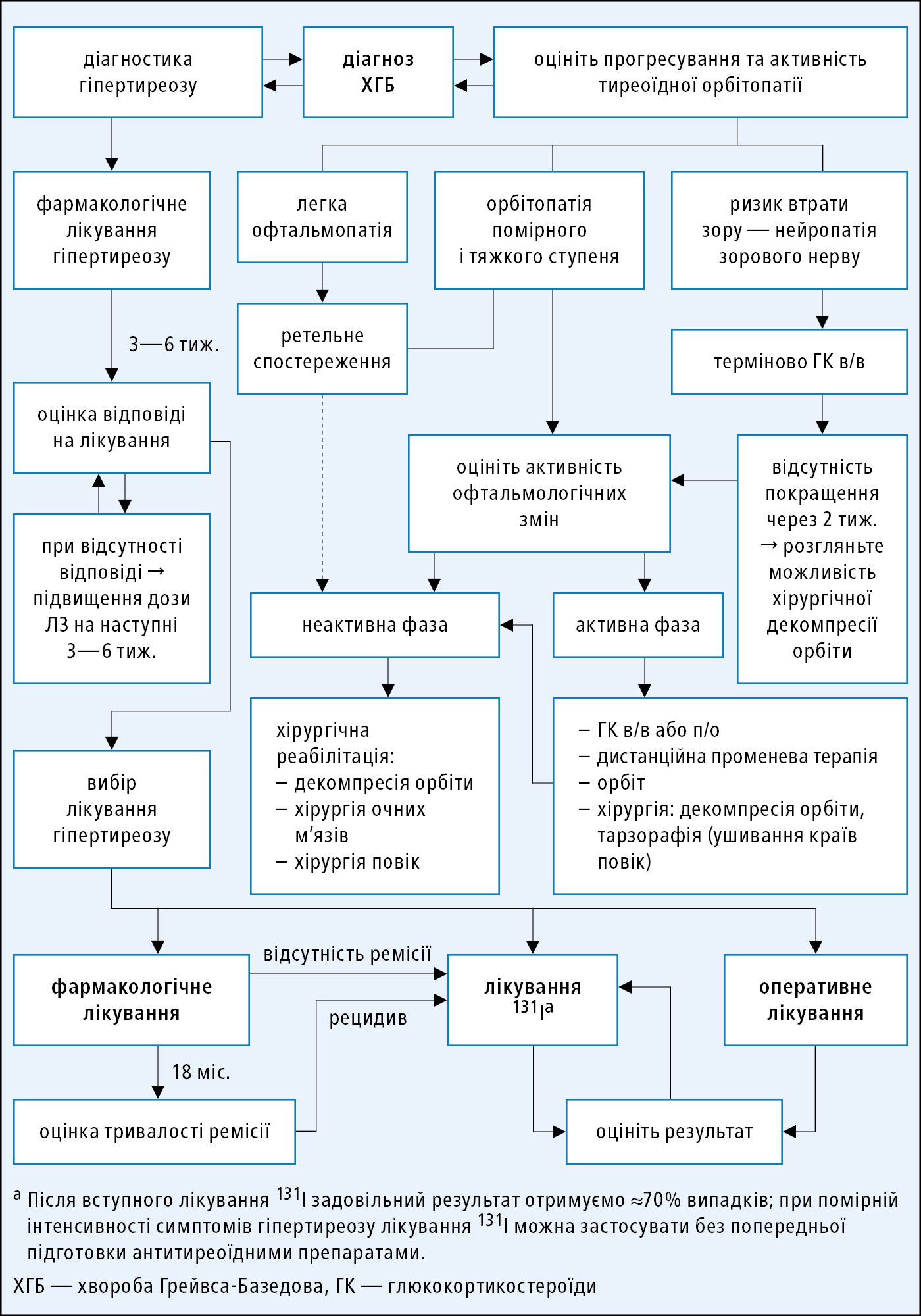
Рисунок 3. Алгоритм лікування дифузного токсичного зобу
Першою метою є якнайшвидше досягнення еутиреозу і визначення разом з пацієнтом подальшої тактики лікування. Якщо основним методом лікування є фармакотерпія, необхідно намагатися досягти стійкої імунологічної ремісії. Позитивною прогностичною ознакою є нормалізація антитіл до рецепторів ТТГ, а також зменшення об’єму зобу та регресія ознак судинного зобу (знижується стимулюючий вплив антитіл АТ-рТТГ і зникає лімфоцитарна інфільтрація) — непрямі ознаки імунологічної ремісії. У випадку рецидиву гіпертиреозу, надається перевага радикальному лікуванню — лікуванню радіоактивним йодом або хірургічному лікуванню, — але допускається тривале лікування низькою дозою тиреостатика, якщо неможливо провести радикального лікування, або якщо воно протипоказано, чи цьому надає перевагу пацієнт. Фармакологічне лікування полегшує симптоми надлишку ГТ і прискорює ремісію, але не запобігає рецидиву, який виникає в ≈50 % випадків, а у чоловіків і хворих <20 р. — навіть в 70–80 %. Важче досягти ремісії у випадках прояви хвороби <15 років, високої концентрації антитіл до рецепторів ТТГ, великий зоб (>30 мл у жінок і >35 мл у чоловіків), Т3-токсикозу, сімейного анамнезу захворювання та куріння.
Загальні принципи антитиреоїдної терапії →розд. 9.2. Оптимальнаий час тривалість фармакологічного лікування — 18 міс., або, принаймні, 12 міс., якщо метою є досягнення стійкої імунологічної ремісії.
1. Схеми антитиреоїдного лікування ДТЗ:
1) монотерапія тіамазолом з поступовим зниженням дози до підтримуючої — класична та схема, якій надається перевага; застосовуйте тіамазол (доза →розд. 9.2) початково до досягнення еутиреозу (≈3–4 тиж.), найчастіше у дозі 20 мг/добу (30–40 мг/добу при тяжкому гіпертиреозі у хворого з великим зобом), а потім — в залежності від результатів гормональних досліджень — поступово знижуйте дозу до підтримуючої (якомога нижчої, що підтримує концентрацію ГЗЩ у межах цільового діапазону): 2,5–10 мг, рідше 10 мг × на день. Застосовуйте протягом 12–18 міс.; якщо після цього часу далі зберігається підвищений рівень АТ-рТТГ, то після консультації з хворим можна прийняти рішення про радикальну терапію (радіойод або тиреоїдектомія) або продовжувати лікування тіамазолом впродовж наступних 12-ти міс. Результати досліджень вказують на ефективність та довготривалу безпеку багаторічного застосування тиреостатику в низькій дозі, що призводить до тривалої ремісії ДТЗ у більшого відсотка хворих ніж стандартна терапія протягом 12–18 міс.; у частини хворих може бути тактикою вибору. Про ефективність фармакотерапії свідчить передусім тривалість ремісії після закінчення лікування (критерій 12-ти міс.). Тільки у випадку алергії на тіамазол, якщо лікування необхідне — пропілтіоурацил (Д →розд. 9.2) — час досягнення еутиреозу, як правило, довший.
2) лікування незмінною, низькою дозою тіамазолу — напр., 10 мг/добу, зазвичай у разі, якщо симптоми гіпертиреозу виражені незначно;
3) застосування тіамазолу разом з L-T4 — модель лікування, що не рекомендується через вищий ризик побічних ефектів, але іноді допускається (схема «блокування та заміна»), напр., тіамазол 30–40 мг/добу та L-T4 у повній замісній дозі (100 мкг/добу).
2. Прояви неефективності фармакотерапії:
1) відсутність гормональної ремісії — незважаючи на застосування антитиреоїдних препаратів рівні ГЩЗ не нормалізуються або підвищуються при спробі знизити дозу ЛЗ;
2) відсутність початкової імунологічної ремісії — концентрація антитіл до рецепторів ТТГ зберігається >10 МЕ/л після 6 міс. фармакотерапії (регресія симптомів гіпертиреозу не гарантує досягнення імунологічної ремісії);
3) відсутність стійкої імунологічної ремісії — підвищений рівень антитіл до рецепторів ТТГ після 12 міс. лікування свідчить про високий ризик рецидиву (75–90 %), незважаючи на еутиреоз;
4) рецидив гіпертиреозу після досягнення гормональної та імунологічної ремісії; якщо період ремісії після закінчення лікування тривав ≥1 року — істинний рецидив.
3. Медикаментозна підготовка (тіамазолом) до радикального лікування:
1) перед оперативним лікуванням — протягом 4–6 тиж. (принаймні 2 тиж.) до досягнення еутиреозу;
2) перед лікуванням 131І — загалом протягом 1–3 міс. прийом антитиреоїдних препаратів слід припинити необхідно вчасно →розд. 9.2; також можливо лікування 131I без попереднього застосування антитиреоїдних ЛЗ.
4. Тактика дій у разі вагітності у жінок, які лікувалися тиреостатиком з приводу ДТЗ: якщо це можливо, не застосовуйте тиреостатичні препарати між 6-м і 10-м тиж. вагітності; у жінки, яка лікувалася низькими дозами тіамазолу (≤5–10 мг/добу) чи пропілтіоурацилу (≤50–200 мг/добу) ризик рецидиву гіпертиреозу після підтвердження вагітності є низьким (на що вказують: невизначена або низька концентрація антитіл до рецепторів ТТГ, нормальна концентрація ТТГ у сироватці крові, використання антитиреоїдних ЛЗ протягом >6 міс. до вагітності та відсутність симптомів тиреоїдної орбітопатії можете відмінити тиреостатик надалі кожні 2 тижні обстежуйте пацієнтку та контролюйте концентрації ТТГ і FT4. Якщо утримується стан клінічного та біохімічного еутиреозу, можна у ІІ та ІІІ триместрах подовжити інтервал між контролями до 4 тиж. При необхідності антитиреоїдного лікування — до вагітності та в I триместрі використовуйте пропілтіоурацил; після 16-го тиж. вагітності перевагу віддають тіамазолу; тиреостатики застосовуйте в якнайнижчих ефективних дозах і контролюйте концентрації ТТГ і FT4 у сироватці, спочатку кожні 2 тиж., а після досягнення еутиреозу — кожні ≈4 тиж. Вагітним жінкам також можна застосовувати пропранолол, однак тільки за необхідності і якомога коротше. При наявності ДТЗ, а також у жінок, які перенесли радикальне лікування гіпертиреозу, слід визначити концентрацію антитіла до рецетпорів ТТГ на початку вагітності або після діагностування гіпертиреозу; у разі підвищеної концентрації — повторити дослідження між 18-м і 22-м тиж. вагітності. Якщо виявлено підвищену концентрацію антитіл до рецепторів ТТГ (особливо >3 × вище верхньої межі норми), рекомендуйте моніторинг плода щодо появи симптоми гіпертиреозу. Якщо рівень антитіл до рецепторів ТТГ підвищений або вагітна приймає антитиреоїдні ЛЗ, повторіть тест в 30–34 тиж. вагітності для оцінки ризику неонатального гіпертиреозу.
Загальні принципи →розд. 9.2. Це метод вибору при радикальному лікуванні гіпертиреозу у перебігу ДТЗ (в дозі ≥10–15 мКі) →табл. 9.2-3, особливо рекомендований у хворих:
1) з протипоказаннями до застосування тиреостатиків;
2) похилого віку, в яких супутні захворювання підвищують операційний ризик;
3) з порушеннями серцевого ритму, які кваліфікуються до лікування аміодароном;
4) жінок, які у майбутньому планують вагітність (не раніше ніж через 6 міс. після введення радіойоду та з застереженням, що підвищена концентрація АТ-рТТГ може зберігатися навіть до 2-х років, а ці антитіла мають здатність стимулювати щитовидну залозу плода.
У ≈3/4 випадків достатньо одноразового прийому 131І, в решті — необхідний прийом другої дози, зазвичай, через 6 міс. При тяжкій активній або помірній орбітопатії терапія 131І протипоказана. При легкій активній орбітопатії лікування 131І проводиться під захистом кортикостероїдами (з огляду на ризик транзиторного загострення) — преднізолон 0,3–0,5 мг/кг/добу з 1–3-го дня після прийому 131І протягом місяця, надалі поступове зниження дози, таким чином, щоб відмінити препарат протягом ≤3 міс. Великий зоб без компресії та стенозу трахеї не є протипоказанням, оскільки об’єм щитоподібної залози на пізніших етапах часто значно зменшується внаслідок лікування, натомість значні компресійні симптоми чи супутні вогнищеві зміни щитоподібної залози з підвищеним ризиком малігнізації є аргументом для хірургічного лікування.
|
Причина гіпертиреозу |
ББ |
T |
131I |
Оп |
|
|
дифузний токсичний зоб (ДТЗ) |
перший епізод |
||||
|
черговий рецидив |
|||||
|
a |
|||||
|
активна тиреоїдна орбітопатія помірного або тяжкого ступеня |
|||||
|
зі встановленим діагнозом або з підозрою на злоякісний вузол |
б |
||||
|
рецидив ДТЗ після оперативного лікування у минулому |
|||||
|
вузловий токсичний зоб |
невеликий зоб без стиснення дихальних шляхів, доброякісний процес |
||||
|
великий зоб, після біопсії вогнищевих уражень — доброякісний процес |
|||||
|
зоб зі встановленим діагнозом або з підозрою на злоякісний вузол |
б |
||||
|
одиничний автономний вузол |
прицільна ТАПБ — доброякісне ураження або підозра на фолікулярну неоплазію без факторів ризику злоякісності |
в |
|||
|
встановлено діагноз раку щитоподібної залози (дуже рідко) |
б |
||||
|
йод-індукований гіпертиреоз
|
аміодарон-індукований гіпертиреоз |
г |
|||
|
інші випадки |
|||||
|
тиреоїдит |
підгострий |
||||
|
тихий або післяпологовий (латентний) |
|||||
|
на початкових стадіях тиреоїдиту Хашімото |
|||||
|
гіпертиреоз у вагітниxґ |
д |
||||
|
субклінічний гіпертиреоз |
е |
||||
|
відсутність показів ад’ювантний метод метод, який застосовується метод, якому надається перевага протипоказаний метод |
|||||
|
a З метою захисту перед збільшенням тяжкості орбітопатії призначають ГК п/о, найчастіше преднізолон у дозі 0,3–0,5 мг/кг м. т./добу (напр., 30 мг/добу) протягом 1 міс., а в подальшому поступово зменшують дозу таким чином, щоб відмінити ЛЗ протягом 3-х міс. б Після оперативного лікування раку в цілому необхідно приймати 131I. в Лікування 131I допускається також у випадку підозри на фолікулярну пухлину щитоподібної залози при прицільній ТАПБ, якщо немає клінічних ознак злоякісності. Ризик раку в істинному одиничному гарячому вузлі становить 2 % (його слід диференціювати від одиничної автономної ділянки при токсичному вузловому зобі). г Залежно від типу; при I типі часто показане додаткове призначення перхлорату натрію, при II типі передусім застосовують ГК. ґ Диференціюйте з тиреотоксикозом вагітних, який рідко потребує лікування. д Використовуйте тільки в тому разі, якщо лікування необхідне, і у значно нижчих дозах; в I триместрі вагітності — бажано застосувати пропілтіоурацил. е Лише, якщо показання до операції виникають через компресію або встановлення діагнозу злоякісного зобу. ББ — β-блокатор, 131I — лікування радіоактивним йодом, Оп — операція на щитоподібній залозі, ТАПБ –тонкоголкова аспіраційна пункційна біопсія, T — тіонаміди (препарат першого ряду — тіамазол) |
|||||
Безсумнівним показанням до операції є супутній вузол з цитологічними або клінічними ознаками злоякісності (ризик раку щитоподібної залози при ДТЗ аналогічний, як при інших формах вузлового зобу, і становить 2–7 %). Перевага оперативному лікуванню надається у випадку супутньої помірної або тяжкої орбітопатії, а також у випадку зобу великих розмірів (>80 мл) чи >50 мл з симптомами компресії (→рис. 9.2-3), або якщо наявні вузлики щитоподібної залози чи у його межах виявляються великі вогнища, що не накопичують йод. Об’єм залишених фрагментів щитоподібної залози суттєво корелює з ризиком рецидиву ДТЗ, тому все частіше виконують тотальну або гранично субтотальну тиреоїдектомію. У випадку одностороннього вогнищевого ураження щитоподібної залози також не рекомендують виконувати щадні операції, тобто видалення однієї частки з перешийком, оскільки залишення тканини щитоподібної залози, яка є чутливою на вплив АТ-рТТГ, наражає хворого на наступні епізоди гіпертиреозу у випадку рецидиву ДТЗ. Хірургічне лікування асоціюється з підвищеним ризиком післяопераційного гіпопаратиреозу, оскільки прищитовидні залози при ДТЗ винятково добре кровопостачаються, а при обширних операціях більш вразливі на післяопераційну ішемію. Сучасні методи інтраопераційного моніторингу знижують ризик ускладнень. Неминучим наслідком операції є гіпотиреоз (принаймні субклінічний), що вимагає замісної терапії.
При лікуванні ДТЗ стандартно протягом 12–18 міс. застосовується спочатку фармакотерапія тіамазолом, тоді як використання радіойоду (або рідше тиреоїдектомія) залишається зазвичай лікуванням другої лінії, якщо фармакотерапія виявляється неефективною. Можна продовжити фармакотерапію ще на 12 міс. (якщо зберігаються підвищені рівні АТ-рТТГ) або обговорити з хворим показання до радикального лікування радіойодом. Рішення про перехід від фармакологічного лікування до радикального (радіойод або хірургічне втручання) завжди потрібно узгоджувати з хворим. Довготривале фармакологічне лікування ДТЗ є безпечним і знижує ризик рецидиву гіпертиреозу більшою мірою (до ≈15 %), ніж лікування тривалістю 12–18 міс., після якого цей ризик оцінюється на ≈45–50 % (дослідження показують, що кожен рік тривалого застосування антитиреоїдних препаратів збільшує шанси на тривалу ремісію ДТЗ). Розгляньте можливість хірургічного лікування в ситуаціях підвищеного ризику раку щитоподібної залози, супутнього вузлового захворювання або великого зобу з компресією. Якщо фармакотерапію не можна продовжувати (напр. виникнули значні побічні ефекти застосування тиреостатика — агранулоцитоз або тяжка печінкова недостатність) або якщо рецидив гіпертиреозу може загострити серцеві захворювання чи планується лікування аміодароном, то у першу чергу розгляньте можливість радикального лікування радіоактивним йодом.
Стійкий ефект неможливий без ефективного лікування гіпертиреозу, однак також слід уникати гіпотиреозу (ТТГ стимулює рецептор TSH-R на орбітальних фібробластах подібно до TRAb, що посилює зміни в очах). Саме лише досягнення ремісії гіпертиреозу може призвести до значного зменшення або ремісії орбітопатії протягом 2–3 міс. Усім курцям із ДТЗ слід рекомендувати повністю припинити палити, оскільки куріння є значним фактором ризику розвитку та більш тяжкого перебігу орбітопатії.
У лікуванні орбітопатії на кожній стадії важливу роль відіграє місцеве лікування, яке запобігає, серед іншого, виразкам рогівки (застосування зволожуючих, антибактеріальних і протизапальних мазей і крапель), а також підтримуюче лікування (вище положення голови для сну, носіння сонцезахисних окулярів, при необхідності застосування сечогінного ЛЗ, що знижує внутрішньоочний тиск). Протизапальне лікування ГК необхідно розпочинати на ранніх стадіях, у фазі активного запалення. Показанням для початку лікування може бути швидке наростання симптомів офтальмопатії. Лікувальна тактика залежить від тяжкості офтальмопатії:
1) ТО з загрозою втрати зору → необхідно негайно рішуче розпочати імуносупресивне, напр., метилпреднізолон (→нижче), і якщо покращення не досягнуто протягом тижня, → хірургічне лікування (термінова орбітальна декомпресія) лікування;
2) ТО від помірної до тяжкої → необхідно розпочати імуносупресивну терапію ГК (якщо хвороба активна — CAS ≥3/7) або розглянути можливість хірургічного лікування (якщо хвороба неактивна);
3) легка ТО → симптоми захворювання не впливають істотно на повсякденне життя і не створюють підстав до застосування імуносупресивного або оперативного лікування, однак швидке погіршення симптомів активної ТО може бути показанням для початку лікування ГК; використовуйте лікування, що полегшує симптоми. Розгляньте поповнювати селен протягом 6-ти міс., (натщесерце), особливо при відносно короткочасному захворюванні, оскільки може знизити ризик прогресування ТО.
При ТО з ризиком втрати зору → негайно напр., метилпреднізолон у дозі 0,5–1 г в/в 1 х в день протягом 3-х наступних днів або кожні 2 дні протягом тижня, із щоденним моніторингом та оцінкою через тиждень. Якщо настає покращення, лікування можна продовжити (сукупна доза метилпреднізолону на цикл <8 г).
При ТО від середньої до тяжкої ГК є препаратами першого ряду, які використовуються тільки при активній хворобі (CAS ≥3/7): EUGOGO (2021) рекомендує кумулятивну дозу 4,5 г метилпреднізолону у 12 інфузіях в/в 1 ×/тиж. (6 інфузій по 0,5 г, потім 6 інфузій по 0,25 г) — добре переносима схема лікування, що значно покращує якість життя хворих. За необхідності можна розглянути вищу кумулятивну дозу — 7,5 г (початкова доза 0,75 г 1 х на тиж. в/в протягом 6 тиж., потім 500 мг в/в щотижня протягом 6 тиж.), яка пов’язана з вищим ризиком небажаних побічних ефектів. ГКС п/о (терапія другого вибору при активній орбітопатії) використовується рідше через меншу ефективність і вищий ризик побічних ефектів — преднізон 1 мг/кг м. т./добу протягом 6–8 тиж., а потім у дозі, яку поступово знижують протягом 3 міс. EUGOGO (2021) також рекомендує використовувати імуносупресивний ЛЗ разом з метилпреднізолоном: мікофенолат натрію (у дозі 0,72 г/день протягом 24 тиж., у т. ч. перші 12 тиж. разом із кортикостероїдами) або мікофенолат мофетил (1,0 г/добу).
Ад’ювантний метод, який для кращого ефекту пропонується використовувати разом з кортикотерапією, оскільки дає кращий і триваліший ефект, ніж використання тільки одного з цих методів. Єдиним протипоказанням (крім вагітності) є діабетична ретинопатія.
Єдиний метод лікування стійких наслідків орбітопатії — після закінчення активної фази захворювання. Часто — багатоетапне, з орбітальною декомпресією та лікуванням косоокості, що виникає у результаті фіброзу окорухових м’язів, та з операціями на повіках. Виконання екстреної орбітальної декомпресію слід зважити при появі симптомів компресії зорового нерву і неефективності інтенсивної імуносупресивної терапії, яка тривала впродовж 1–2 тиж.
Новим препаратом, зареєстрованим FDA у 2020 році (який вже має позитивний відгук EMA і чекає на допущення до реалізації в ЄС) для розгляду у хворих із помірною та важкою активністю ТО (CAS ≥4), є тепротумумаб — моноклональне антитіло проти рецептора інсуліноподібного фактора росту 1 (IGF-1). Зараз триває дискусія щодо місця цього нового ЛЗ в алгоритмі лікування ТО, рекомендації EUGOGO (2021) вказують його як ЛЗ другого вибору, подібно до ритуксимабу та тоцилізумабу (не зареєстрованих EMA для лікування ТО).
ПРОГНОЗвгору
1. Гіпертиреоз: без лікування з часом розвивається спонтанна ремісія, але раніше можуть з’явитися небезпечні для життя ускладнення →розд. 9.2. Фармакологічне лікування усуває симптоми надлишку ГЩЗ і прискорює настання ремісії, але у ≈50 % випадків виникає рецидив захворювання. Концентрація антитіл до рецепторів ТТГ нормалізується у більшості пацієнтів вже після ≈6 міс. лікування, але це не дає впевненості, що досягнена ремісія буде тривалою. Ризик рецидиву — вищий у чоловіків і у осіб у віці <20-ти р., а також у пацієнтів з великим зобом і високим стартовим співвідношенням FT3/FT4. Гіпотиреоз розвивається завжди після оперативного лікування і дуже часто — після успішного лікування радіоактивним йодом; також може розвинутися при ДТЗ після тривалого фармакологічного лікування.
2. Тиреоїдна орбітопатія: без лікування може зникнути без стійких наслідків, особливо при легкій формі, але при активній тяжкій формі ризик незворотного пошкодження тканин очниць (порушення рухливості очних яблук та гостроти зору, і навіть сліпота) — великий, особливо при злоякісному екзофтальмі. Своєчасне лікування (в активній фазі хвороби) часто дозволяє уникнути серйозних наслідків. Якщо екзофтальм, ураження м’яких тканин і м’язів очного яблука значно виражені або, якщо розвивається ураження рогівки або компресія зорового нерву — існує великий ризик стійкого пошкодження органу зору та стійких змін у зовнішньому вигляді пацієнта. Косоокість і екзофтальм корегуються хірургічним шляхом після закінчення активної фази захворювання.