DEFINICIÓNArriba
El melanoma es una neoplasia maligna derivada de los melanocitos de la piel, de las mucosas o de la úvea.
EPIDEMIOLOGÍAArriba
El melanoma constituye un 5-7 % de todas las neoplasias de la piel. La incidencia es mayor en Australia (28,9/100 000 hombres y 25,3/100 000 mujeres). La mediana de edad de aparición es de ~50 años.
PERSPECTIVA LATINOAMERICANA
Se desconocen los datos estadísticos de epidemiología de melanoma en países de Latinoamérica. Con mayor frecuencia, el melanoma se presenta en mujeres con lesión en miembros inferiores, es de tipo histológico lentiginosoacral y suele ser diagnosticado en etapa tardía.
EtiopatogeniaArriba
Los factores que conducen a la transformación neoplásica de los melanocitos no se conocen por completo. La radiación ultravioleta (UV) desempeña un papel importante en este proceso, dado que ejerce una acción mutágena directa en el ADN y, además, estimula las células de la piel a producir factores de crecimiento, debilita los mecanismos de defensa de la piel y, junto con otros factores oxidativos como los radicales libres, favorece la creación de la melanina oxidada, la cual provoca daños en el ADN e inhibe la apoptosis. El efecto nocivo de la radiación UV es favorecido por ciertas características fenotípicas naturales y por estados de inmunodeficiencia. La transformación neoplásica puede tener origen genético (p. ej. mutaciones de los genes CDKN2A y CDK4, diagnosticadas en una parte de los melanomas tanto esporádicos como familiares).
Factores de riesgo:
1) antecedentes familiares: un riesgo desde 3 veces (1 familiar de primer grado enfermo) hasta 70 veces mayor (≥3 familiares); se distingue el síndrome de melanoma y lunares múltiples atípicos familiares (familial atypical mole and melanoma syndrome, FAM-M) en el que el riesgo llega casi al 100 %
2) antecedentes de:
a) melanoma (riesgo 8 veces mayor)
b) otra neoplasia maligna de piel (riesgo 3 veces mayor)
3) nevus melanocíticos: numerosos (>50; con >100 nevus el riesgo es 11 veces mayor), que cambian de aspecto, nevus atípicos (riesgo 11 veces mayor)
4) xeroderma pigmentosum
5) tez pálida, pelo claro o rojo, ojos azules, presencia de pecas (un riesgo 2-3 veces mayor)
6) exposición periódica intensa a la radiación UV (sol, solárium)
7) tendencia a quemaduras solares
8) quemaduras solares graves en la infancia o juventud (riesgo 2-3 veces mayor después de ≥5 episodios de quemaduras)
9) inmunosupresión (p. ej. en trasplantados de órgano, riesgo 3 veces mayor).
Un ~60 % de los melanomas se desarrolla en una piel sin cambios. Entre las lesiones a partir de las cuales se puede desarrollar un melanoma se enumeran:
1) nevus melanocíticos, que se forman a causa de alteraciones prenatales del desarrollo cutáneo y se manifiestan en diferentes periodos de la vida:
a) nevus displásico (atípico)
b) nevus melanocítico congénito
c) nevus de la unión (juntural)
d) nevus azul
2) manchas pigmentarias (muy raras veces).
Cuadro clínicoArriba
Formas clínicas del melanoma de piel:
1) forma superficial (superficial spreading melanoma, SSM; el 40-60 % de los casos) →fig. 24.7-1
2) forma nodular (nodular melanoma, NM; el 30-50 %) →fig. 24.7-2
3) melanoma lentigo maligno (lentigo malignant melanoma, LMM; el 5-10 %) →fig. 24.7-3
4) melanoma lentiginoso acral (acral lentiginous melanoma, ALM; el 5 %)
5) melanoma subungueal (subungual melanoma, SM; el 5 %).
Síntomas y signos
En la forma temprana del melanoma de piel, las lesiones son planas, asimétricas, de bordes irregulares y dentados con la piel sana, multicolores. En la forma avanzada suelen elevarse sobre el nivel de la piel, en algunos casos están ulceradas con exudación serohemática en la superficie (factores pronósticos desfavorables).
A veces el primer síntoma del melanoma es la aparición de adenopatías en cadenas linfáticas que drenan el área en la que se ha desarrollado la neoplasia (p. ej. en caso del melanoma de recto o melanoma subungueal).
Historia naturalArriba
El melanoma infiltra capas de la piel cada vez más profundas y produce metástasis en la piel vecina o poco alejada del tumor primario (focos satélite y metástasis in-transit), metástasis en los ganglios linfáticos y también metástasis a distancia por vía linfática o sanguínea.
Los melanomas que se desarrollan en las extremidades presentan mejor pronóstico que los del tronco. En caso de metástasis a distancia, la mediana de supervivencia aumentó significativamente en la última década y en la actualidad es de por lo menos unos años.
DiagnósticoArriba
El diagnóstico se basa en la anamnesis (teniendo en cuenta los factores de riesgo) y en un examen físico exhaustivo que debe abarcar toda la piel prestando atención a las áreas recubiertas de vello (incluido el cuero cabelludo), las palmas de las manos, las plantas de los pies y la piel entre los dedos.
Rasgos de la lesión cutánea que inducen sospecha de melanoma:
1) forma asimétrica, irregular
2) distribución desigual del color
3) bordes irregulares
4) cambios de grosor y de superficie de la lesión
5) tamaño >6 mm
6) prurito.
Es imperativo tener presente la posibilidad de aparición de melanoma subungueal, de las mucosas (p. ej. de la vulva, del recto, de la cavidad oral) y de la úvea.
Criterios diagnósticos
Para confirmar el diagnóstico, así como determinar la estadificación de la neoplasia y el pronóstico, resulta necesario el examen histológico. La lesión cutánea sospechosa se extirpa por completo con un pequeño margen (1-3 mm) y, en caso de que se confirme el diagnóstico de melanoma, en función de su estadio, se toma la decisión de ampliar la resección hasta unos márgenes de seguridad óptimos, y se seleccionan los enfermos candidatos para la biopsia del ganglio centinela (si el grosor de la infiltración del melanoma es ≥1 mm, así como en ciertos melanomas de >0,8 mm de grosor en caso de adicionales factores pronósticos desfavorables).
Valoración de la extensión
En la actualidad, se recomienda la clasificación del American Joint Committee on Cancer (AJCC) basada en el sistema TNM (→tabla 24.7-1). A fin de valorar la extensión local, que es de importancia fundamental para el pronóstico, se utiliza el índice de Breslow que, simplificando, consiste en medir el grosor de la infiltración del melanoma en escala métrica. Además, con un examen microscópico se evalúa la presencia de ulceración y la actividad mitótica del melanoma (son factores pronósticos importantes).
TratamientoArriba
Tratamiento quirúrgico
El tratamiento quirúrgico es el método de elección. Es obligatorio resecar la lesión con un margen cuya extensión depende del grosor del melanoma (0,5-2 cm), y realizar biopsia del ganglio centinela (es decir, el primer ganglio linfático en la vía del drenaje de la linfa). En la actualidad, en caso de resultado positivo de la biopsia del ganglio centinela, se puede renunciar a la linfadenectomía complementaria, aunque una linfadenectomía que abarque el correspondiente drenaje linfático sigue siendo una alternativa terapéutica. En enfermos con metástasis en ganglios linfáticos detectables clínicamente y —de preferencia— con confirmación citológica, se realiza una resección completa del correspondiente grupo de ganglios linfáticos regionales.
Un tratamiento quirúrgico radical adecuado, en caso de melanoma avanzado localmente resulta suficiente y requiere únicamente observación clínica. En caso de estadio III y resección completa de las lesiones en estadio IV es necesario aplicar el tratamiento posoperatorio complementario (inmunoterapia o terapia molecular dirigida). No se recomienda radioterapia complementaria.
Tratamiento del melanoma avanzado y diseminado
1. Inmunoterapia y terapia molecular dirigida: son las opciones más eficaces. Se ha demostrado un efecto beneficioso en el estadio IV con diversas opciones:
1) Inmunoterapia con ipilimumab. Es un anticuerpo monoclonal humano que bloquea el antígeno CTLA-4 [cytotoxic T-lymphocyte-associated protein 4] y, en consecuencia, aumenta la actividad del sistema inmune, lo que se refleja en que los linfocitos T atacan células neoplásicas.
2) Inmunoterapia con nivolumab (en monoterapia o asociado con ipilimumab) y pembrolizumab. Son anticuerpos monoclonales que bloquean el receptor de muerte programada tipo 1 o el ligando de dicho receptor.
3) Terapia con inhibidores de la transducción de señales. Estos fármacos bloquean las señales que una molécula transmite a otra dentro de una célula. Es posible que, al impedir esta transmisión, se destruyan células de melanoma. En esta categoría se incluyen los siguientes:
a) inhibidores BRAF (dabrafenib, vemurafenib, encorafenib), que bloquean la actividad de proteínas elaboradas por los genes BRAF mutados
b) inhibidores MEK (trametinib, cobimetinib, binimetinib), que bloquean unas proteínas llamadas MEK1 y MEK2 que afectan la multiplicación y supervivencia de las células de melanoma; combinaciones de inhibidores BRAF y MEK utilizadas para tratar el melanoma: dabrafenib y trametinib, vemurafenib y cobimetinib, o encorafenib y binimetinib.
Todavía no se ha determinado la secuencia óptima del tratamiento sistémico (sobre todo en los enfermos con mutación en el gen BRAF). El tratamiento con inhibidores de BRAF/MEK aumenta el porcentaje de respuestas (~70 %) y acelera la mejoría clínica. En caso de administrar inmunoterapia la respuesta es menos frecuente, pero en la mayoría de los casos es prolongada y puede persistir después de concluir la inmunoterapia.
Los resultados de estudios prospectivos demostraron también la eficacia de muchos de los fármacos enumerados más arriba en enfermos con melanoma en estadios III y IV (tras la extirpación total de metástasis), por lo que, en la actualidad, tras el tratamiento quirúrgico, estos enfermos son derivados a un tratamiento complementario.
2. Extirpación de las metástasis a distancia. Se considera p. ej. cuando las metástasis son poco numerosas (particularmente si afectan un órgano), cuando aparecieron transcurridos 12 meses después del tratamiento primario, o cuando, basándose en las pruebas de imagen, se puede esperar una resección completa y el tiempo de supervivencia esperado (teniendo en cuenta el estado clínico general) supera 3 meses.
3. Quimioterapia con un fármaco citotóxico (p. ej. dacarbazina). Lleva a la remisión en <20 % de los enfermos (incluidas las pocas respuestas completas). Actualmente, al introducir inmunoterapia y fármacos moleculares, el papel de la quimioterapia resulta muy limitado.
4. Los resultados actuales de las investigaciones sobre las vacunas en el tratamiento del melanoma diseminado son decepcionantes. No obstante, se ha demostrado la eficacia del tratamiento con el virus atenuado del herpes simple tipo 1 (talimogén laherparepvec, T-VEC) al que se le ha insertado la secuencia de codificación del factor estimulante de colonias de granulocitos y macrófagos humano (GM-CSF). El fármaco se introduce en el tumor, el virus se replica de manera selectiva en las células neoplásicas, las cuales al producir GM-CSF inmunoestimulante provocan la muerte celular y la liberación de antígenos derivados del tumor.
5. La quimioterapia con perfusión de miembro aislado con hipertermia consiste en la administración intraarterial de altas dosis de un fármaco citostático (normalmente melfalán) a un miembro aislado de la circulación sistémica. Este método tiene aplicación en caso de recidiva del melanoma localmente avanzada y localizada en un miembro tras una resección radical (sin metástasis a distancia), o en caso de aparición de numerosas metástasis in-transit (localizadas entre el tumor primario y la estación de ganglios linfáticos más cercana; se originan en las células neoplásicas que quedaron atrapadas en los vasos linfáticos). También se puede optar por la resección si el número de metástasis no es demasiado alto.
VIGILANCIAArriba
Durante los primeros 2 años, las pruebas de control deben realizarse cada 3 meses. Si los ganglios linfáticos regionales no se han resecado, las pruebas deben realizarse 1 × mes. Transcurridos 2 años, las pruebas se realizan cada 3-6 meses; y transcurridos 5 años, cada 6-12 meses (después 1 × año). La frecuencia individual de las pruebas de control depende, sobre todo, de la profundidad de infiltración del melanoma, es decir, del riesgo de recaída de la enfermedad.
No existen indicaciones claras en cuanto a las pruebas de imagen, pero suelen recomendarse una radiografía de tórax y una ecografía abdominal cada 6 meses. Si los ganglios linfáticos regionales no se han resecado, la ecografía de la región afectada debe realizarse cada 3 meses durante ≥2 años tras la cirugía (luego cada 6-12 meses).
Situaciones especialesArriba
Melanoma del globo ocular
El melanoma es la neoplasia primaria maligna del globo ocular más frecuente en adultos, particularmente las metástasis en la úvea, y constituye ~10 % de todos los casos de melanoma. El melanoma puede aparecer en la piel de los párpados, en la conjuntiva o en el segmento anterior (el iris →fig. 24.7-4) o posterior de la úvea (el cuerpo ciliar, la coroides →fig. 24.7-5). El pronóstico es peor que en casos de melanoma cutáneo. En ciertas situaciones clínicas, es posible la terapia protónica. En caso de melanoma de coroides está indicada la braquiterapia epiescleral.
Melanoma de las mucosas
El melanoma de las mucosas con más frecuencia aparece en la cavidad oral, vías respiratorias superiores y esófago (50 %), vulva (20 %) y en la zona anogenital (20 %). El pronóstico es malo (la supervivencia a los 5 años es del 25 %). El tratamiento consiste en una extirpación total. Con mayor frecuencia que en casos de melanoma de localización cutánea se recurre a la radioterapia o quimioterapia complementarias, o a inmunoterapia/terapia molecular dirigida. En casos especiales, debido a un acceso quirúrgico difícil, considerar solo la radioterapia.
PronósticoArriba
El riesgo de recaída local del melanoma de piel es del 3-15 % en función de la localización del foco primario, grosor de la infiltración y presencia de ulceración. El porcentaje de supervivencia a los 5 años depende del estadio clínico y es en el grado I del el 95 %, en el II del 75 %, en el III del 60 %, y en el IV del 20 %.
PrevenciónArriba
1) Identificar a personas con factores de riesgo.
2) Evitar exposición solar excesiva, particularmente cortos episodios de exposición solar intensa que provoca quemaduras de piel.
3) Identificar lesiones sospechadas de evolucionar hacia el melanoma (regla ABCDE):
a) asimétricas (A)
b) de bordes irregulares y dentados (B)
c) de color no uniforme o que cambia con el tiempo (C)
d) de >6 mm de diámetro y que van creciendo (D)
e) de superficie elevada (E).
Las lesiones sospechosas requieren un diagnóstico y una eventual biopsia excisional.
TABLAS Y FIGURAS
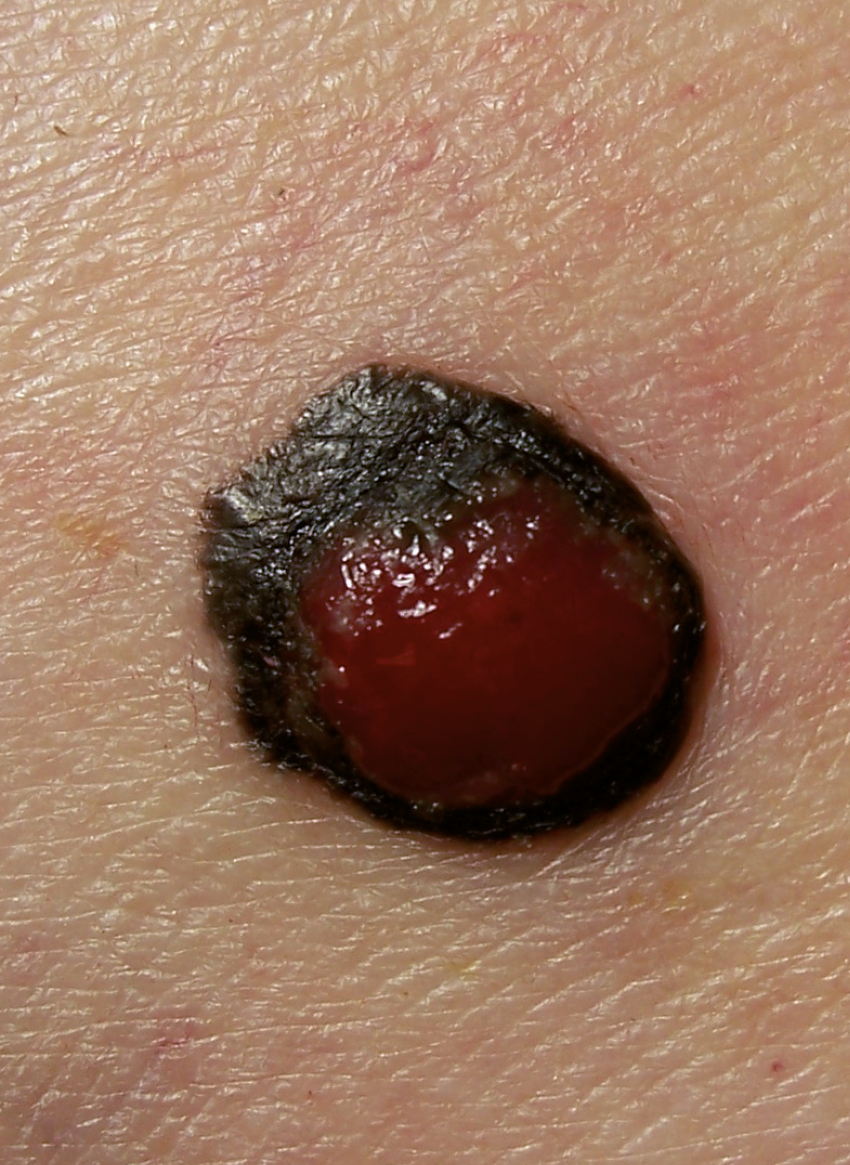
Fig. 24.7-1. Melanoma superficial (foto: Dr. Wojciech M. Wysocki)
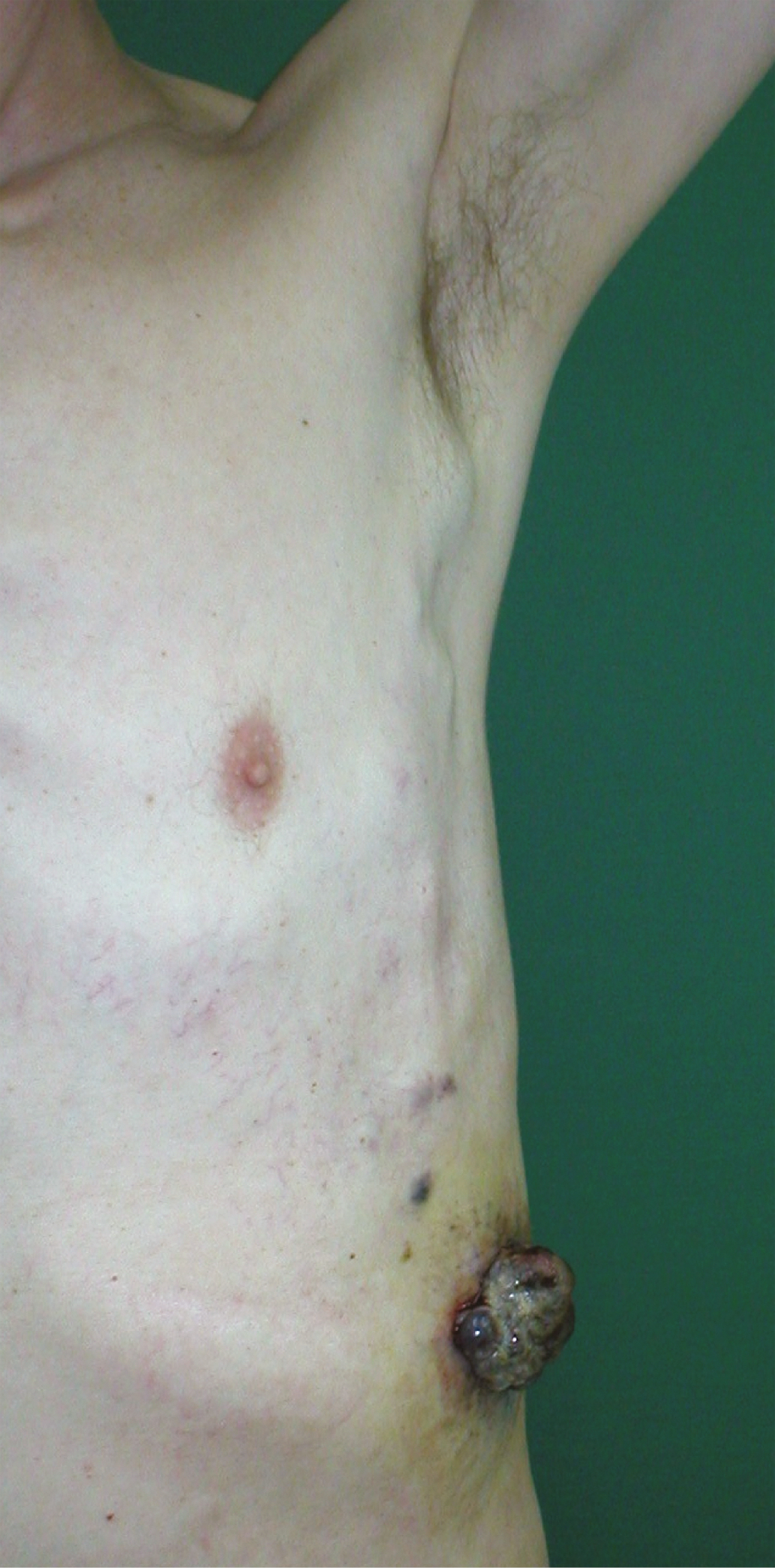
Fig. 24.7-2. Melanoma (forma nodular): foco principal con ulceración. Un poco más arriba puede verse un nódulo perteneciente a lesiones cutáneas. En la parte inferior de la axila es visible una metástasis en un ganglio linfático que eleva la piel, mientras que, entre el foco primario y la cavidad axilar, en el tejido subcutáneo, se observan metástasis in transit (foto: Dr. Wojciech M. Wysocki)
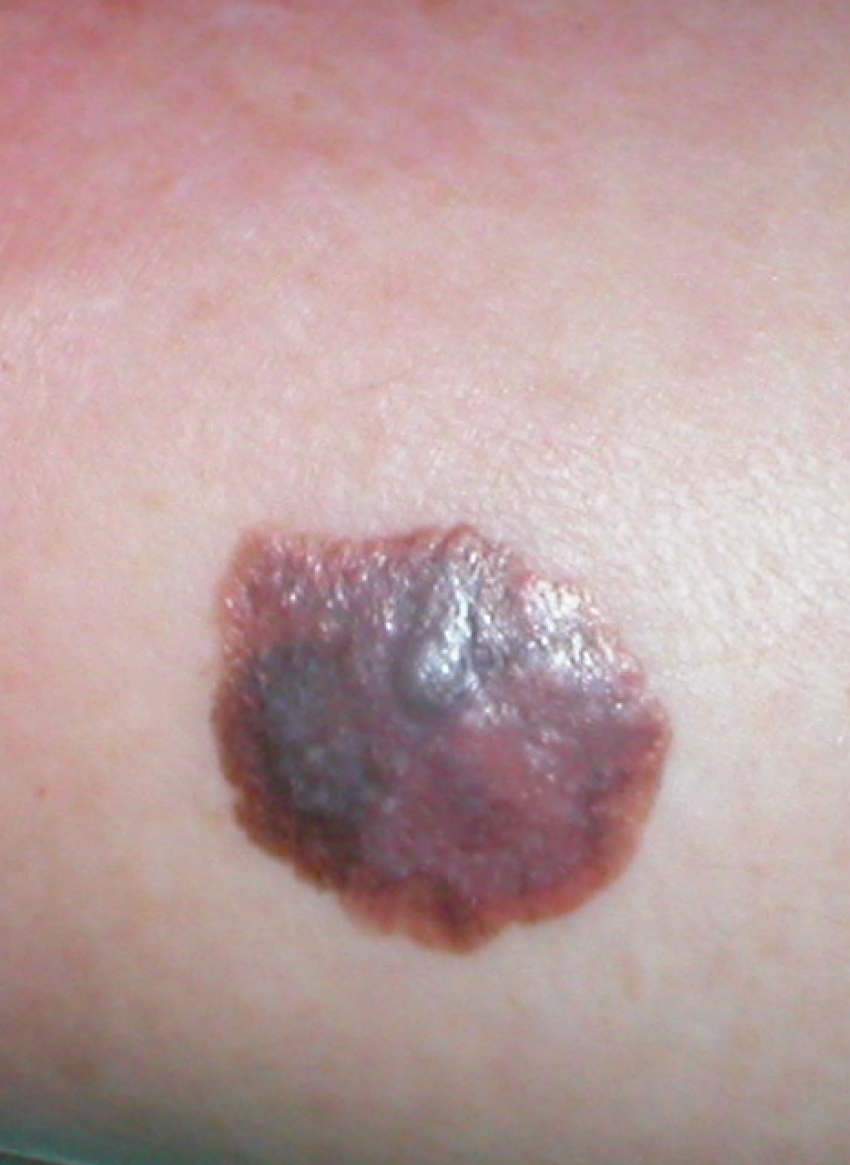
Fig. 24.7-3. Melanoma lentigo maligno (foto: Dr. Wojciech M. Wysocki)
Clasificación clínica de la estadificación del melanoma de piel (8.ª revisión del TNM de 2017)
|
Estadificación
|
TNM
|
|
0
|
Tis N0 M0
|
|
IA
|
T1a N0 M0
|
|
IB
|
T1b N0 M0
T2a N0 M0
|
|
IIA
|
T2b N0 M0
T3a N0 M0
|
|
IIB
|
T3b N0 M0
T4a N0 M0
|
|
IIC
|
T4b N0 M0
|
|
III
|
T1-4 N1-3 M0
|
|
IV
|
Todos los T, todos los N, M1
|
|
Rasgo T
Tis: melanoma in situ
T1: profundidad de la infiltración ≤1mm (T1a: <0,8 mm sin ulceración; T1b: <0,8 mm con ulceración o 0,8-1,0 mm independientemente de la presencia de ulceración)
T2: 1,01-2,0 mm (T2a: sin ulceración, T2b: con ulceración)
T3: 2,01-4 mm (T3a: sin ulceración, T3b: con ulceración)
T4: >4 mm (T2a: sin ulceración, T2b: con ulceración)
Rasgo N
N0: no se detectan metástasis en ganglios linfáticos
N1: metástasis en 1 ganglio linfático detectada microscópicamente (N1a), clínicamente (N1b) o presencia de una metástasis in-transit, de un tumor satélite o microsatélite sin afectación ganglionar (N1c)
N2: metástasis en 2-3 ganglios linfático detectadas microscópicamente (N2a), clínicamente (N2b) o presencia de una metástasis in-transit, de un tumor satélite o microsatélite con afectación de 1 ganglio (N2c)
N3: metástasis en ≥4 ganglios linfático detectadas microscópicamente (N3a), clínicamente/paquete de ganglios (N3b) o metástasis in-transit o tumores satélite con afectación de 2-3 ganglios/paquete (N3c)
Rasgo M
M0: no se detectan metástasis a distancia
M1: se detectan metástasis a distancia (M1a: en la piel o tejidos blandos; M1b: en los pulmones [+/– rasgo M1a]); M1c: en otros órganos fuera del sistema nervioso central [+/– M1a o M1b]); M1d: en el sistema nervioso central [+/– M1a o M1b o M1c]).
|
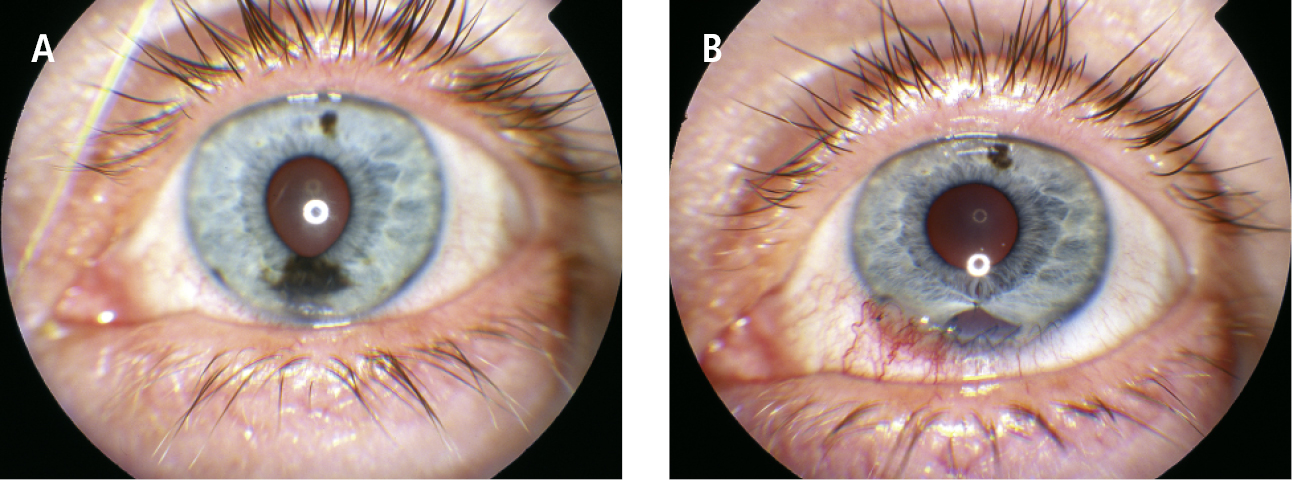
Fig. 24.7-4. Melanoma de iris: antes (A) y después de la resección (B) (foto: Profa. Bożena Romanowska-Dixon)
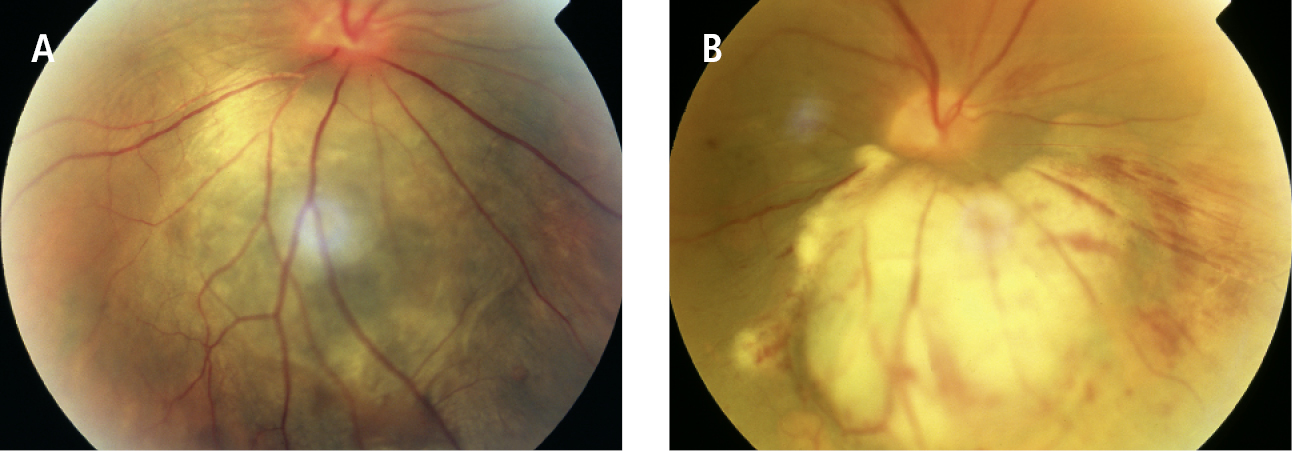
Fig. 24.7-5. Melanoma de coroides: antes de la braquiterapia asociada a termoterapia transpupilar (A) y después del tratamiento (B)
 Español
Español
 English
English
 українська
українська









