COMENTARIO
Cómo citar: Demkow M., Comentario. En: Bodzioch M., Leśniak W., Prewencja wtórna udaru mózgu u chorych z drożnym otworem owalnym. Podsumowanie wytycznych American Academy of Neurology 2020, Med. Prakt., 2021; 5: 40-43
Siglas y abreviaturas: ESUS (embolic stroke of undetermined source) — ACV embólico de origen indeterminado, FA — fibrilación auricular, FOP — foramen oval permeable, RMN — resonancia magnética nuclear
El debate sobre el manejo de los pacientes con foramen oval permeable (FOP) se reabre cada varios años. Esto se debe a que, cada cierto tiempo, se publican los resultados de ensayos multicéntricos sobre la eficacia de las intervenciones de cierre del tabique. Como consecuencia, han ido apareciendo más recomendaciones y opiniones de expertos.1-4
Hay que tener en cuenta que el FOP se diagnostica en 1 de cada 4 adultos. Es una variante anatómica del corazón sano y no se debe denominar como cardiopatía. Se ha demostrado que el FOP no es un factor de riesgo independiente para los ACV en la población general. Por lo tanto, es indiscutible que la prevención primaria de estos accidentes (cierre del tabique) no tiene justificación alguna.
El embolismo paradójico (cruzado) sistémico causado por la entrada de material embólico en la circulación arterial sistémica se ha descrito desde los años 50 del siglo pasado (Johnson). Este es el diagnóstico que se debe establecer cuando la causa del embolismo es la circulación venosa sistémica (p. ej. tromboflebitis de miembros inferiores), hay una conexión entre la circulación venosa y la arterial (FOP), hay embolismos arteriales sistémicos y el origen de los embolismos no se encuentra en las venas pulmonares, el corazón izquierdo o las arterias sistémicas. En esta situación, se debe considerar (recomendación de clase IIa/C3) el cierre del tabique interauricular como prevención secundaria de eventos embólicos en la circulación sistémica. Esta situación tampoco es debatible.
Sin embargo, lo que sí se debate en las recomendaciones y opiniones de los expertos es el problema de los pacientes con FOP que han sufrido un ACV isquémico criptogénico.1-4
En un 40 % de las personas jóvenes (<55 años) no se consigue determinar la causa del ACV isquémico. Este ACV se conoce como criptogénico (de etiología desconocida), o según la nomenclatura actual, ACV embólico de origen indeterminado (ESUS). Al parecer, el FOP es el doble de frecuente en estos pacientes (se diagnostica en un 50 %) que en el resto de la población. Actualmente, el embolismo paradójico (cruzado) secundario al FOP se considera un posible mecanismo responsable del ACV isquémico en los pacientes en los que no se haya determinado otra causa. En relación con el diagnóstico del embolismo paradójico en un paciente con FOP que haya sufrido un ACV criptogénico, se puede hablar de distintos grados de probabilidad, pero no de certeza. El ACV criptogénico de un paciente con FOP no tiene por qué guardar relación con un embolismo cruzado. Las opiniones y recomendaciones citadas indican a qué pacientes con FOP y ESUS se les puede proponer el cierre del tabique como prevención secundaria de eventos embólicos cerebrales.
Resumiendo de manera breve y práctica estas recomendaciones, las personas que cumplan las siguientes condiciones son aptas para el cierre del FOP
1) Edad <55-60 años
2) Antecedentes de ACV embólico documentado por pruebas de imagen (resonancia magnética nuclear [RMN])
3) Ausencia de una causa del ACV más probable que el FOP (sospecha o confirmación de material embólico en el lado izquierdo del corazón o en las arterias periféricas: ateroesclerosis, vasculitis, fibrilación auricular [FA], trastornos de la coagulación). Estas guías presentan una lista de pruebas diagnósticas útiles.1 Se ha otorgado especial importancia a la FA latente, y se considera que la FA puede ser la causa de una parte significativa de los ACV en estos pacientes. Este diagnóstico se debe considerar principalmente en los pacientes con factores de riesgo de FA (hipertensión arterial, obesidad, diabetes, hipertiroidismo, nicotinismo, apnea del sueño, aurículas aumentadas), en cuyo caso se deben llevar a cabo pruebas de diagnóstico exhaustivas (seguimiento por ECG durante varios días e incluso implante temporal de un dispositivo subcutáneo para detectar arritmias).
4) Presencia de FOP con un cortocircuito importante derecha-izquierda durante la prueba de provocación (Valsalva) en el ecocardiograma transesofágico. No se trata de una importancia "volumétrica hemodinámica". La importancia está determinada por el número de burbujas del contraste ecocardiográfico (p. ej. solución salina agitada) administrado en una vena sistémica (p. ej. vena basílica) que atraviesan el FOP durante la prueba de Valsalva en dirección a la aurícula izquierda (>20-30 burbujas en los primeros ciclos cardíacos indican un cortocircuito importante).
5) Antecedentes de episodio neurológico que el neurólogo diagnosticó como ACV embólico a partir de la totalidad del cuadro clínico y el resultado de la RMN.
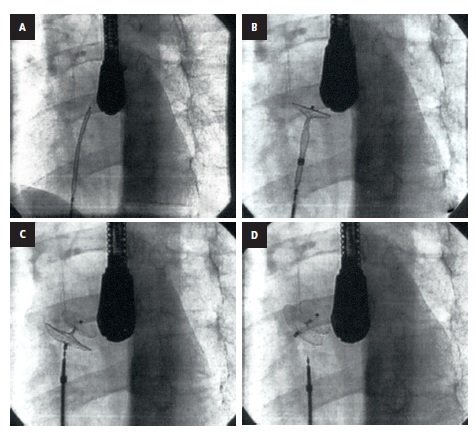
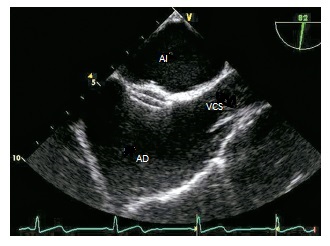
El tratamiento de elección es una intervención endovascular, posible en la gran mayoría de los pacientes, que consiste en cerrar el tabique con un implante (fig. 1). Este dispositivo se introduce a través de un catéter de acceso mediante una punción de la vena femoral en la ingle (fig. 2). Un cardiólogo invasivo con experiencia relevante en este ámbito debe determinar las posibilidades de llevar a cabo esta intervención basándose en un ecocardiograma transesofágico y además debe informar al paciente sobre los beneficios y los riesgos potenciales de la intervención. La figura 3 presenta un ecocardiograma transesofágico posterior a la intervención.
Después de esta intervención, se recomienda administrar un tratamiento antiplaquetario dual (ácido acetilsalicílico 75 mg 1 × d y clopidogrel 75 mg 1 × d) durante 3 meses, y en adelante solo ácido acetilsalicílico de manera indefinida o durante al menos 5 años. También está indicada la prevención de la endocarditis infecciosa durante 6 meses.
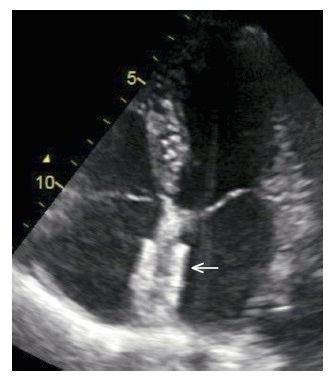
Se recomienda agendar consultas ambulatorias para realizar un ecocardiograma transtorácico 1-3 meses después de la intervención, y en adelante cada año en función de las necesidades (fig. 4). Esta prueba se realiza para comprobar que el implante esté en una posición adecuada, así como los posibles cortocircuitos residuales, trombos en el implante o derrame pericárdico.
La intervención no requiere que los pacientes implementen ninguna limitación en su vida cotidiana. Los implantes de uso habitual están hechos de materiales no ferromagnéticos, por lo que su presencia no supone una contraindicación para la RMN.
En resumen, según las observaciones de los estudios multicéntricos, el cierre endovascular del FOP reduce significativamente el riesgo de recurrencia de ACV embólicos en los pacientes con antecedentes de ESUS cuidadosamente seleccionados para tal intervención.
Fig. 1. Implantes utilizados en la práctica clínica para el cierre endovascular del foramen oval. A. Amplatzer PFO. B. Helex (reimpreso de: Szczeklik A., Tendera M., red., Kardiologia. Podręcznik oparty na zasadach EBM, Kraków, Medycyna Praktyczna, 2009: 588) Fig. 2. Cierre percutáneo del foramen oval permeable. A-D. Etapas de implantación de un dispositivo de oclusión Amplatzer PFO (reimpreso de: Szczeklik A., Tendera M., red.: Kardiologia. Podręcznik oparty na zasadach EBM, Kraków, Medycyna Praktyczna, 2009: 588) Fig. 3. Ecocardiograma transesofágico: implante reciente de un dispositivo de oclusión Amplatzer en el foramen oval. AD — aurícula derecha, AI — aurícula izquierda, VCS — vena cava superior (reimpreso de: Szczeklik A., Tendera M., red., Kardiologia. Podręcznik oparty na zasadach EBM, Kraków, Medycyna Praktyczna, 2009: 589) Fig. 4. Ecocardiograma transtorácico (proyección de 4 cámaras) tras una intervención de cierre del foramen oval permeable: dispositivo de oclusión Amplatzer PFO en el tabique interauricular, posición correcta del implante (flecha)
Bibliografía:
1. Messé S.R., Gronseth G.S., Kent D.M. y cols., Practice advisory update summary: patent foramen ovale and secondary stroke prevention. Report of the Guideline Subcommittee of the American Academy of Neurology, Neurology, 2020; 94: 876-8852. Araszkiewicz A., Bartuś S., Demkow M. y cols., Interventional closure of patent foramen ovale in prevention of thromboembolic events. Consensus document of the Association of Cardiovascular Interventions and the Section of Grown-up Congenital Heart Disease of the Polish Cardiac Society, Kardiol. Pol., 2019; 77: 1094-1105
3. Baumgartner H., De Backer J., Babu-Narayan S.V. y cols., ESC Scientific Document Group: 2020 ESC Guidelines for the management of adult congenital heart disease, Eur. Heart. J., 2021; 42: 563–645 (red. Med. Prakt. 2021; 3: 10–43)
4. Pristipino C., Sievert H., D’Ascenzo F. y cols., Evidence Synthesis Team; Eapci Scientific Documents and Initiatives Committee; International Experts: European position paper on the management of patients with patent foramen ovale. General approach and left circulation thromboembolism, Eur. Heart J., 2019; 40: 3182-3195
 Español
Español
 English
English
 українська
українська