Aortopatías
Síndrome de Marfan y otras enfermedades hereditarias de la aorta torácica
En los pacientes jóvenes con síndrome de Marfan o con una enfermedad hereditaria de la aorta torácica asociada a dicho síndrome, raíz aórtica dilatada y válvula aórtica tricúspide, se recomienda realizar una anuloplastia aórtica con reimplante y remodelado para reparar la válvula, siempre y cuando un cirujano experimentado se encargue de la intervención [I/C].
En los pacientes con síndrome de Marfan, la cirugía se recomienda en los casos de enfermedad de la raíz aórtica con un diámetro máximo de la aorta ≥50 mm a nivel sinusal [I/C]. Asimismo, se debe considerar en los casos de enfermedad de la raíz aórtica y diámetro de la aorta ≥45 mm a nivel sinusal cuando se presenten factores de riesgo adicionales (antecedentes familiares de disección aórtica con diámetro pequeño [o antecedentes de disección aórtica espontánea en el paciente], insuficiencia aórtica progresiva, embarazo planificado, hipertensión arterial descontrolada y/o aumento rápido del diámetro aórtico >3 mm/año [en mediciones repetidas realizadas mediante la misma técnica de imagen con sincronización ECG, al mismo nivel de la aorta, comparadas directamente y confirmadas mediante otra técnica de imagen]) [IIa/C].
En los pacientes con mutación del gen TGFBR1 o TGFBR2 (incluidos aquellos con síndrome de Loeys-Dietz) y enfermedad de la raíz aórtica con un diámetro máximo de la aorta ≥45 mm a nivel sinusal, se debe considerar el tratamiento quirúrgico [IIa/C].
Válvula aórtica bicúspide
El tratamiento quirúrgico de la aorta se debe considerar si el diámetro de la aorta ascendente es:
1) ≥50 mm en caso de VAB en pacientes con factores de riesgo adicionales (antecedentes familiares de disección aórtica con diámetro pequeño, embarazo planificado, hipertensión en la circulación sistémica y/o aumento del diámetro aórtico >3 mm/año [en mediciones repetidas realizadas mediante la misma técnica de imagen con sincronización ECG, al mismo nivel de la aorta, valoradas directamente y confirmadas mediante otra técnica de imagen]) o coartación aórtica
2) ≥55 mm en el resto de pacientes [IIa/C].
Síndrome de Turner
En las mujeres >16 años con síndrome de Turner con diámetro indexado de la aorta ascendente >25 mm/m2 (en los casos de superficie corporal extrema, este umbral se puede corregir) y:
1) con factores de riesgo adicionales de disección aórtica (VAB, elongación del cayado aórtico, coartación aórtica, hipertensión arterial), se debe considerar programar una cirugía del aneurisma de la raíz aórtica y/o de la aorta ascendente como método de elección [IIa/C]
2) sin factores de riesgo adicionales, se puede considerar dicha operación [IIb/C].
Obstrucción del tracto de salida del ventrículo derecho
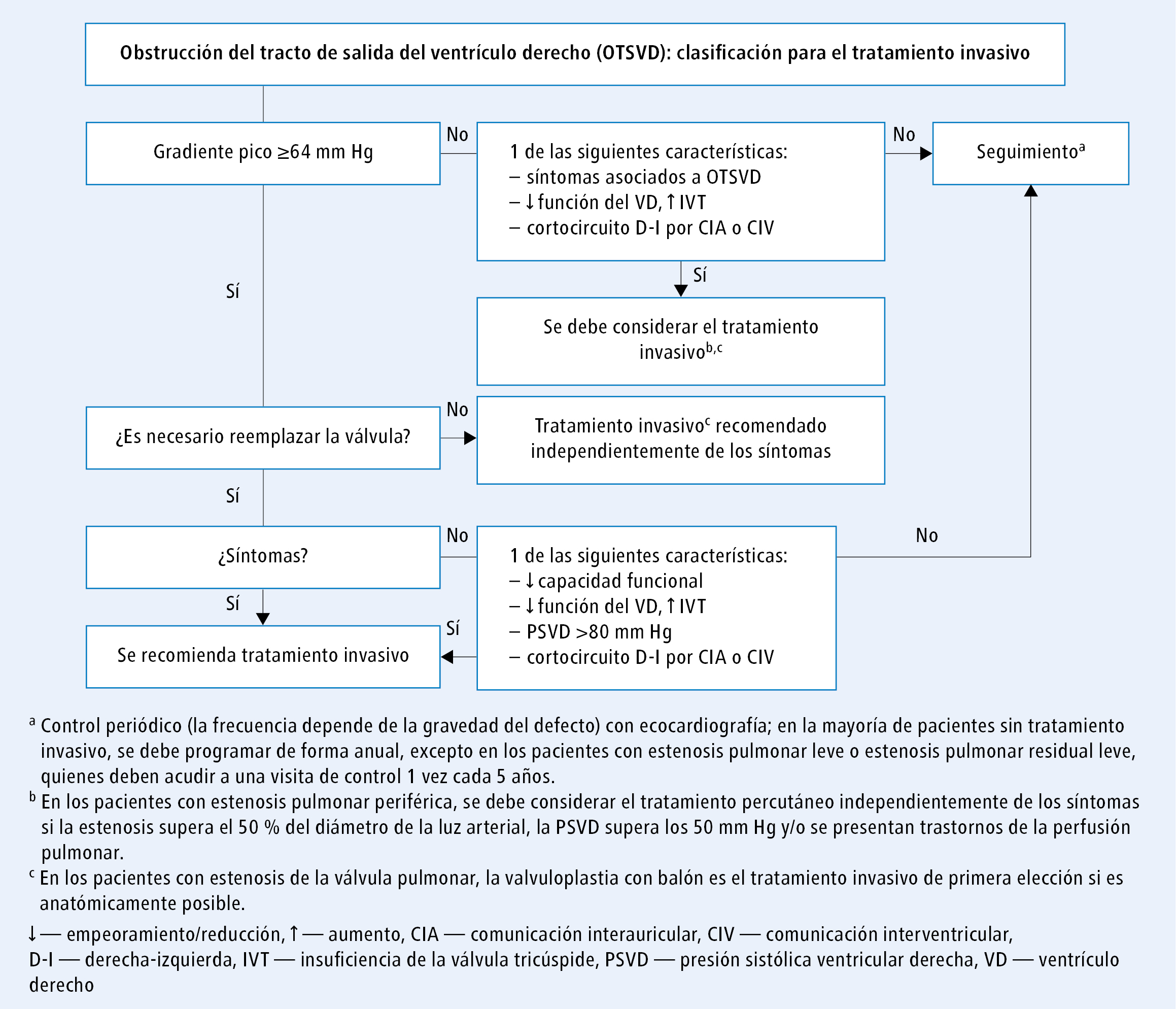
La figura 6 presenta el protocolo para determinar la aptitud para el tratamiento invasivo de los pacientes con obstrucción del tracto de salida del ventrículo derecho (OTSVD).
Fig. 6. Algoritmo de toma de decisiones sobre el tratamiento invasivo de la obstrucción del tracto de salida del ventrículo derecho (a partir de las guías de la ESC 2020, modificado)En los casos de estenosis valvular pulmonar (EVP), la valvuloplastia con balón es el tratamiento invasivo de elección siempre y cuando sea anatómicamente posible [I/C].
Suponiendo que el reemplazo de la válvula no sea necesario, se recomienda el tratamiento invasivo de la OTSVD a cualquier nivel, independientemente de los síntomas, si la estenosis es grave (el gradiente pico por Doppler es >64 mm Hg: la presión sistólica ventricular derecha (PSVD) estimada con base en la velocidad de la onda retrógrada a través de la válvula tricúspide confirma la EVP grave) [I/C].
Si la única opción de tratamiento es el reemplazo quirúrgico de la válvula, se recomienda en los pacientes con estenosis grave:
1) que presenten síntomas de estenosis [I/C]
2) asintomáticos que presenten ≥1 de las siguientes manifestaciones:
a) reducción objetiva de la capacidad física
b) empeoramiento de la función ventricular derecha y/o progresión de la insuficiencia de la válvula tricúspide (al menos hasta un nivel moderado)
c) PSVD >80 mm Hg
d) cortocircuito derecha-izquierda por CIA o CIV [I/C].
En los pacientes con gradiente pico por Doppler <64 mm Hg, el tratamiento invasivo se debe considerar si se presenta ≥1 de las siguientes manifestaciones:
1) síntomas relacionados con la EVP
2) empeoramiento de la función ventricular derecha y/o progresión de la insuficiencia de la válvula tricúspide (al menos hasta un nivel moderado)
3) cortocircuito derecha-izquierda por CIA o CIV [IIa/C].
Independientemente de los síntomas, se debe considerar el tratamiento transcatéter de la EVP si la estenosis supera el 50 % del diámetro de la luz arterial, la PSVD supera los 50 mm Hg y/o se presentan trastornos de la perfusión pulmonar [IIa/C].
Anomalía de Ebstein
En los pacientes con insuficiencia grave de la válvula tricúspide y síntomas o empeoramiento objetivo de la capacidad física, se recomienda la cirugía correctiva [I/C]. Un cirujano que trate CC y tenga experiencia operando anomalías de Ebstein debe encargarse de la cirugía [I/C].
Si existe una indicación para la operación de la válvula tricúspide y se puede esperar una buena tolerancia hemodinámica, se recomienda cerrar la CIA o el agujero oval persistente (AOP) durante la reparación de la válvula [I/C].
En los pacientes con dilatación progresiva de las cavidades cardíacas derechas y empeoramiento de la función sistólica del ventrículo derecho, se debe considerar la cirugía correctiva independientemente de los síntomas [IIa/C].
En los pacientes con arritmias sintomáticas o signos de preexcitación en el ECG, se debe realizar un estudio electrofisiológico, y después una ablación —siempre y cuando sea posible— o un tratamiento quirúrgico de las arritmias en caso de que se haya programado otra cirugía cardíaca [I/C].
En caso de documentar un embolismo periférico probablemente causada por un embolismo cruzado, se debe considerar el cierre percutáneo aislado de la CIA/el AOP mediante un oclusor. No obstante, esto requiere un análisis preoperatorio exhaustivo para descartar la posibilidad de que la intervención aumente la presión en la aurícula derecha y reduzca el gasto cardíaco [IIa/C].
Si la cianosis es el problema dominante (SaO2 en reposo <90 %), se puede considerar el cierre percutáneo aislado de la CIA/el AOP mediante un oclusor. No obstante, esto también requiere un análisis preoperatorio exhaustivo con el fin de descartar la posibilidad de que la intervención aumente la presión en la aurícula derecha y reduzca el gasto cardíaco [IIb/C].
Pacientes tras cirugías correctivas de tetralogía de Fallot
En los pacientes sintomáticos con insuficiencia pulmonar grave (es decir, con una fracción de regurgitación en la RMN >30-40 %) y/u OTSVD al menos moderada (velocidad pico >3 m/s), se recomienda el reemplazo de la válvula [I/C]. En los pacientes con salida ventricular no nativa (después de haberse sometido a una cirugía de la salida ventricular derecha con homoinjerto, injerto de vena yugular bovina o bioprótesis/conducto), se debe dar preferencia al reemplazo percutáneo si las características anatómicas del paciente lo permiten [I/C].
Por otro lado, en los pacientes asintomáticos con insuficiencia pulmonar grave y/u OTSVD, se debe considerar el reemplazo valvular si presentan ≥1 de los siguientes signos:
1) reducción objetiva de la capacidad de esfuerzo
2) dilatación progresiva del ventrículo derecho (hasta un volumen telesistólico ventricular derecho [VTSVD] >80 ml/m2 y/o un volumen telediastólico ventricular derecho [VTDVD] ≥160 ml/m2; confirmados en mediciones repetidas) y/o progresión de la insuficiencia de la válvula tricúspide hasta al menos moderada
3) disfunción sistólica progresiva del ventrículo derecho
4) OTSVD con PSVD >80 mm Hg [IIa/C].
Se debe considerar el cierre de la CIV en los pacientes con CIV residual y una sobrecarga volumétrica significativa del ventrículo izquierdo, o si se han sometido a cirugía en la válvula pulmonar.
En los pacientes con TV sostenida que se vayan a someter a un reemplazo de la válvula pulmonar o un implante valvular percutáneo, se debe considerar realizar un mapeo preoperatorio con catéter y dañar los istmos anatómicos responsables de la TV antes o durante la intervención [IIa/C].
Se debe considerar la realización de un estudio electrofisiológico, incluida una estimulación ventricular programada, para estratificar el riesgo de MSC en los pacientes con factores de riesgo adicionales (disfunción ventricular izquierda o derecha, TV sostenida y sintomática, duración de QRS ≥180 ms, cicatrización ventricular derecha extensa en la RMN) [IIa/C].
El DCI se debe considerar en algunos pacientes con tetralogía de Fallot y numerosos factores de riesgo de MSC, como disfunción ventricular izquierda, TV sintomática no sostenida, duración de QRS ≥180 ms, cicatrización ventricular derecha en la RMN o TV inducida durante la estimulación ventricular programada [IIa/C]. De forma alternativa al DCI, se puede considerar la ablación percutánea o la ablación quirúrgica para tratar la TV monomorfa sostenida sintomática en los pacientes con función biventricular conservada, siempre y cuando la intervención se lleve a cabo en un centro altamente especializado y se puedan lograr los efectos previstos de la ablación (no inducibilidad de la arritmia, bloqueo de la conducción a lo largo de la línea de ablación) [IIb/C].
Transposición de grandes arterias
Pacientes tras corrección fisiológica
1. Recomendaciones de tratamiento quirúrgico
En los pacientes sintomáticos con estenosis de la aurícula venosa pulmonar, se recomienda una corrección quirúrgica (la intervención percutánea raramente es posible) [I/C].
En los pacientes sintomáticos con estenosis del túnel intraauricular no aptos para la intervención percutánea, se recomienda la corrección quirúrgica [I/C]. En los pacientes sintomáticos con cortocircuito del parche no aptos para el cierre percutáneo, se recomienda la corrección quirúrgica [I/C].
En los pacientes con insuficiencia grave de la válvula AV sistémica (tricúspide) sin disfunción sistólica ventricular significativa (FE >40 %), se debe considerar la corrección o el reemplazo de la válvula independientemente de los síntomas [IIa/C].
No se recomienda colocar una banda en la arteria pulmonar en los adultos como entrenamiento del ventrículo izquierdo para después realizar una corrección anatómica [III/C].
2. Indicaciones para el tratamiento percutáneo
En los pacientes sintomáticos con estenosis del túnel intraauricular, se recomienda el implante de un stent siempre que sea técnicamente posible [I/C].
En los pacientes sintomáticos con cortocircuito del parche y cianosis en reposo y esfuerzo, o con alta sospecha de embolismo paradójico, se recomienda colocar un stent (recubierto) o realizar un cierre percutáneo mediante un dispositivo implantable siempre que sea técnicamente posible [I/C].
En los pacientes con cortocircuito del parche y síntomas causados por un cortocircuito izquierda-derecha, se recomienda colocar un stent (recubierto) o realizar un cierre percutáneo siempre que sea técnicamente posible [I/C].
En los pacientes asintomáticos con cortocircuito del parche y sobrecarga volumétrica ventricular significativa causada por un cortocircuito izquierda-derecha, se debe considerar la colocación de un stent (recubierto) o el cierre percutáneo mediante un dispositivo implantable siempre que sea técnicamente posible [IIa/C].
En los pacientes con cortocircuito del parche que precisen del implante de un estimulador cardíaco o un DCI, se debe considerar el cierre del cortocircuito del parche con un stent recubierto siempre que sea técnicamente posible antes de introducir los electrodos transvenosos [IIa/C].
En los pacientes asintomáticos con estenosis del túnel intraauricular, se puede considerar la colocación de un stent siempre que sea técnicamente posible [IIb/C].
Pacientes tras corrección anatómica
En los casos de estenosis de arteria coronaria que causa isquemia, se recomienda colocar un stent u operar (en función del origen de la isquemia) [I/C].
La cirugía de la raíz neoaórtica se debe considerar si su diámetro es >55 mm (en las personas de estatura media) [IIa/C]. A la hora de decidir si operar la insuficiencia valvular neoaórtica grave, se debe tener en cuenta que se trata de una reoperación, técnicamente más complicada.
En caso de estenosis de una rama de la arteria pulmonar, se debe considerar la colocación de un stent independientemente de los síntomas si se constata una estenosis del diámetro >50 %, una PSVD >50 mm Hg y/o una reducción de la perfusión pulmonar secundaria [IIa/C].
Transposición de las grandes arterias congénitamente corregida
En los pacientes sintomáticos con insuficiencia grave de la válvula tricúspide y función sistólica del ventrículo derecho sistémico conservada o levemente alterada (FE >40 %), se recomienda el reemplazo de la válvula tricúspide [I/C], y si la función de este ventrículo está más alterada (FE ≤40 %), se puede considerar dicho reemplazo [IIb/C]. En los pacientes asintomáticos con insuficiencia grave de la válvula tricúspide, dilatación progresiva del ventrículo derecho sistémico y/o función sistólica del ventrículo derecho sistémico levemente alterada (FE >40 %), se debe considerar el reemplazo de la válvula [IIa/C].
En caso de bloqueo AV completo y necesidad de estimulación ventricular >40 %, se debe considerar la estimulación biventricular [IIa/C].
Enfermos tras un implante de conducto entre el ventrículo derecho y la arteria pulmonar
Los pacientes sintomáticos con PSVD >60 mm Hg (puede ser menor en caso de reducción de flujo) y/o insuficiencia pulmonar grave (fracción de regurgitación en la RMN >30-40 %) deben someterse a un tratamiento invasivo, preferentemente a un implante transcatéter de válvula pulmonar (ITVP) si es anatómicamente posible [I/C]. En los pacientes asintomáticos con OTSVD grave y/o insuficiencia de la válvula pulmonar grave, este tratamiento se debe considerar si se presentan ≥1 de las siguientes manifestaciones:
1) reducción objetiva de la capacidad física (en la PECP)
2) dilatación progresiva del ventrículo derecho (hasta un VTSVD ≥80 ml/m2 y/o un VTDVD ≥160 ml/m2) y/o aumento de la insuficiencia tricúspide hasta por lo menos moderada
3) disfunción sistólica progresiva del ventrículo derecho
4) PSVD >80 mm Hg [IIa/C].
Corazón univentricular
Se recomienda que los adultos con corazón univentricular no operados o que hayan tenido una operación paliativa se sometan a un análisis exhaustivo en un centro especializado, mediante diversas técnicas de imagen y de diagnóstico invasivo, con el objetivo de decidir si la cirugía o el tratamiento percutáneo pueden beneficiarles [I/C].
Solo se pueden considerar candidatos a la operación de Fontan ciertos pacientes sintomáticos con cianosis que se hayan sometido a una valoración exhaustiva (RVP baja, función normal de las válvulas AV, función ventricular conservada) [IIa/C].
En los pacientes con flujo pulmonar elevado —poco probable en la edad adulta—, se debe considerar colocar una banda en la arteria pulmonar o apretar más la banda previamente colocada [IIa/C].
En los pacientes con cianosis grave y flujo pulmonar reducido:
1) sin aumento de RVP y PAP: se debe considerar el procedimiento bidireccional de Glenn [IIa/C]
2) no aptos para el procedimiento de Glenn: se puede considerar una anastomosis entre la circulación sistémica y la arteria pulmonar [IIb/C].
En los pacientes en mal estado clínico en los que la cirugía estándar sea imposible, se debe considerar el trasplante de corazón o corazón y pulmón [IIa/C].
Pacientes tras operación de Fontan
La arritmia auricular sostenida con conducción AV rápida es una emergencia y se debe tratar de forma urgente mediante una cardioversión eléctrica [I/C].
El tratamiento anticoagulante está indicado si se observan o se han observado un trombo auricular, arritmias auriculares o incidentes tromboembólicos [I/C].
Se recomienda desaconsejar el embarazo a las mujeres que se hayan sometido a una operación de Fontan y hayan sufrido cualquier complicación secundaria [I/C].
Se recomienda realizar un cateterismo cardíaco (y tomar la decisión sobre esta prueba rápidamente, sin muchas restricciones) en caso de edemas inexplicados, reducción de la capacidad de esfuerzo, arritmia (de nueva aparición), cianosis o hemoptisis [I/C].
En los pacientes con trastornos del ritmo, se debe considerar un enfoque proactivo con respecto al estudio electrofisiológico y la ablación (si estuviera indicada) [IIa/C].
Se debe considerar la realización periódica de pruebas de imagen del hígado (ecografía, TC o RMN) [IIa/C].
En algunos pacientes con presión/resistencia pulmonar elevada pero sin aumento de la presión ventricular telediastólica, se puede considerar el uso de antagonistas del receptor de endotelina o inhibidores de la fosfodiesterasa 5 [IIb/C].
En algunos pacientes con cianosis significativa, se puede considerar el cierre percutáneo de la fenestración (creada en algunos pacientes y en algunos centros durante la operación de Fontan), pero esto requiere un análisis exhaustivo antes de la intervención para descartar que provoque un aumento de la presión venosa sistémica o una reducción del gasto cardíaco [IIb/C].
Anomalías de las arterias coronarias
En los pacientes con anomalías de las arterias coronarias, se recomienda realizar pruebas funcionales de imagen no farmacológicas (p. ej. gammagrafía cardíaca, ecocardiografía o prueba de esfuerzo con RMN) para confirmar o descartar la isquemia miocárdica [I/C].
1. Origen anómalo de una arteria coronaria en la arteria pulmonar: en los pacientes con origen anómalo de la arteria coronaria izquierda en la arteria pulmonar (ALCAPA), se recomienda operar [I/C]. En los pacientes con origen anómalo de la arteria coronaria derecha en la arteria pulmonar (ARCAPA) y síntomas que se puedan atribuir a la arteria coronaria anómala, se recomienda operar [I/C]. en los pacientes asintomáticos con ARCAPA y disfunción ventricular o isquemia miocárdica que se puedan atribuir a la anomalía coronaria, se debe considerar operar [IIa/C].
2. Origen aórtico anómalo de las arterias coronarias: en los pacientes con origen aórtico anómalo de una arteria coronaria (AAOCA), síntomas típicos de angina e indicios de isquemia miocárdica inducida por una carga en la zona vascular correspondiente, o con características anatómicas de alto riesgo (curso intramural de la arteria y origen anómalo [origen en hendidura, origen en ángulo agudo, origen >1 cm sobre la unión sinotubular]), se recomienda operar [I/C].
La cirugía se debe considerar en los pacientes asintomáticos:
1) con AAOCA (de la arteria coronaria derecha [AAORCA] o izquierda [AAOLCA]) y manifestaciones de isquemia miocárdica [IIa/C]
2) con AAOLCA sin manifestaciones de isquemia miocárdica, pero con características anatómicas de alto riesgo (véase más arriba) [IIa/C].
La cirugía se puede considerar:
1) en los pacientes sintomáticos con AAOCA, aunque no haya indicios de isquemia miocárdica ni características anatómicas de alto riesgo [IIb/C]
2) en los pacientes asintomáticos con AAOLCA, sin isquemia miocárdica y sin características anatómicas de alto riesgo si tienen <35 años [IIb/C].
La intervención quirúrgica no se recomienda en los pacientes asintomáticos con AAORCA, sin isquemia miocárdica y sin características anatómicas de alto riesgo [III/C].
 Español
Español
 English
English
 українська
українська