Descripción del caso clínico
Un hombre de 72 años fue admitido en el servicio de cirugía general, derivado a la colecistectomía por colelitiasis sintomática. La anamnesis reveló hipertensión arterial, hipercolesterolemia y FA paroxística. El enfermo tomó regularmente apixabán (5 mg por la mañana y por la noche), rosuvastatina (20 mg por la noche), amlodipino (5 mg por la mañana) y nebivolol (5 mg por la mañana). Su peso fue de 75 kg, los niveles de creatinina de 92,8 μmol/l (1,05 mg/dl) y la TFGe (calculada a partir de la fórmula de Cockroft‑Gault) de 67,5 ml/min/1,73 m2.
El día de ingreso hospitalario se discontinuó la terapia con apixabán (el paciente recibió la última dosis la noche anterior), manteniendo el tratamiento con los demás fármacos. Después de 24 h, se realizó la colecistectomía laparoscópica bajo anestesia general. En las pruebas de laboratorio de control no se observó disminución importante de los niveles de hemoglobina. El día de la intervención por la noche (a las 12 h de la finalización de la cirugía), se administró apixabán a dosis de 5 mg y se continuó el tratamiento previo hasta el alta hospitalaria.
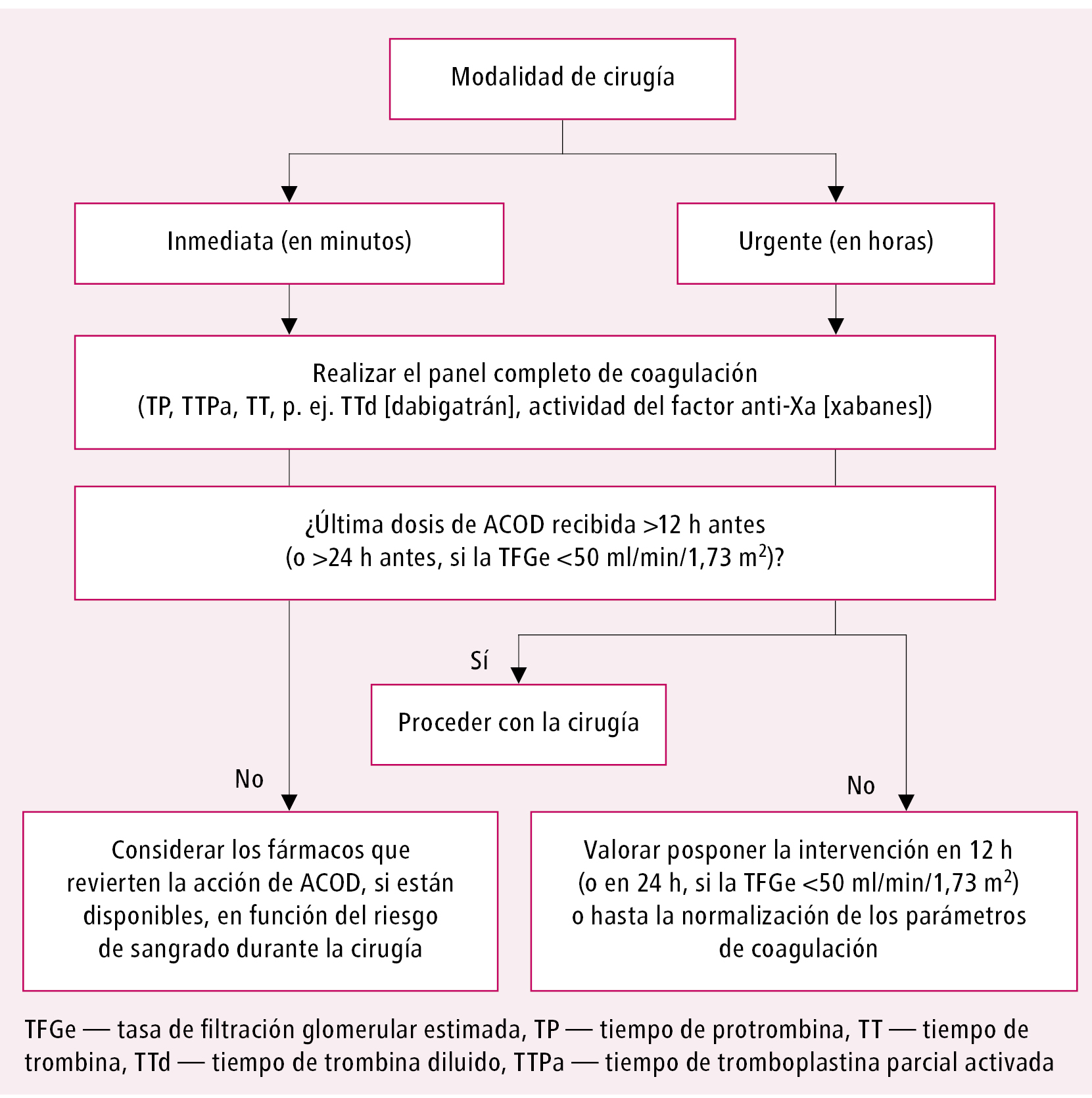
Fig. Estrategia de manejo del paciente tratado con anticoagulantes orales directos (ACOD) preparados para cirugías no programadas, según las recomendaciones de la European Society of Cardiology, modificado7
| Tabla 1. Categorías de riesgo tromboembólico en diferentes estados clínicos | |||
|---|---|---|---|
|
Riesgo tromboembólico |
Prótesis valvular cardíaca mecánica |
Fibrilación auricular |
ETV |
|
Bajo |
Prótesis aórtica mecánica bicúspide sin otros factores de riesgo del ACV |
1‑4 ptos. en la escala CHA2DS2‑VASc sin antecedentes de ACV, AIT ni episodio de embolismo periférico |
Antecedente de 1 episodio de ETV en >12 meses anteriores (actualmente sin otros factores de riesgo de la ETV) |
|
Intermedio |
Prótesis aórtica mecánica bicúspide y 1 de los factores de riesgoa |
5‑6 ptos. en la escala CHA2DS2‑VASc o antecedentes de ACV, TIA o episodio de embolismo periférico en >3 meses |
– Episodio de ETV en los últimos 3‑12 meses o ETV recidivante – Formas más leves de trombofilia (p. ej. heterocigota para la mutación G20210A del gen de protrombina o factor V Leiden) |
|
Alto |
– Prótesis mitral mecánica o prótesis aórtica mecánica antiguas (de tipo jaula‑bola, o de disco pivotante) – ACV o AIT en los últimos 6 meses |
– 7‑9 ptos. en la escala CHA2DS2‑VASc o antecedentes de ACV, TIA o episodio de embolismo periférico en <3 meses – Cardiopatía reumática |
– Episodio de ETV en los últimos 3 meses – Trombofilia grave (p. ej. déficit de antitrombina, de la proteína C o de la proteína S, síndrome antifosfolipídico o coexistencia de varias alteraciones) – Neoplasia maligna (tratamiento en los últimos 6 meses o en estadio de tratamiento paliativo) |
|
a Factores de riesgo: fibrilación auricular, antecedentes de ACV o de AIT, hipertensión arterial, diabetes mellitus, insuficiencia cardíaca congestiva, edad >75 años. ACV— accidente cerebrovascular, AIT — accidente isquémico transitorio, ETV — enfermedad tromboembólica venosa A partir de las guías del ACCP y las polacas (2012) y de la posición de los expertos del ACC (2017) Reimpreso de: Niżankowski R. y cols., Żylna choroba zakrzepowo‑zatorowa. En: Gajewski P. (red.), Interna Szczeklika 2022, Kraków, Medycyna Praktyczna, 2022: 606 | |||
| Tabla 2. Riesgo de sangrado relacionado con la intervención | |
|---|---|
|
Riesgo |
Tipo de intervención |
|
Muy bajo |
– Tratamiento quirúrgico de cataratas o de glaucoma – Intervenciones odontológicas (p. ej. extracción de 1‑3 dientes, intervenciones periodontales, colocación de implante, endodoncia, eliminación del sarro dental acumulado en la bolsa periodontal) – Estudio endoscópico sin biopsia ni resección – Intervenciones menores en la piel (p. ej. incisión del absceso, resección de un pequeño fragmento de piel, biopsia) |
|
Bajo |
– Cirugías abdominales (colecistectomía, cirugías de hernia, resección del intestino grueso) – Cirugías ortopédicas menores (de pies, de manos, artroscopia) – Cirugía de mama – Intervenciones odontológicas complejas (extracción de varios dientes) – Endoscopia con biopsia única – Gastroscopia o colonoscopia con biopsia única – Punción con aguja gruesa (p. ej. de médula ósea o ganglio linfático) – Cirugías oftalmológicas distintas al tratamiento de cataratas |
|
Alto |
– Cirugías abdominales con biopsia hepática, litotricia extracorpórea por ondas de choque – Cirugía extensa por neoplasia maligna (p. ej. de páncreas, de hígado) – Anestesia subaracnoidea o epidural – Intervenciones vasculares (p. ej. reparación de aneurisma de aorta abdominal, puente vascular) – Cirugías ortopédicas mayores – Intervenciones con biopsia de órgano bien vascularizado (riñón, próstata) – Cirugías plásticas de reconstrucción – Polipectomía de intestino grueso – Punción lumbar – Reparación intravascular de aneurisma – Intervenciones torácicas, resección de pulmón – Neurocirugías (intracraneales, de médula espinal) – Cirugías urológicas (prostatectomía, resección de tumor de vejiga) |
|
Según las guías de la ESC (2022) Reimpreso de: Leśniak W., Konsultacje kardiologiczne u chorych poddawanych operacjom pozasercowym. Podsumowanie wytycznych European Society of Cardiology 2022, Med. Prakt., 2022; 12: 17 | |
| Tabla 3. Situaciones clínicas en las que se debe considerar la terapia puente durante la interrupción de antagonistas de la vitamina K (AVK) o anticoagulantes orales directos (ACOD)4,7 |
|---|
|
1) Antecedentes de ACV o de trombosis venosa profunda en los últimos 3 meses 2) Alto riesgo de recidiva de trombosis venosa profunda por trombofilia de alto riesgo (p. ej. déficit de antitrombina, déficit de la proteína C y/o S, síndrome antifosfolipídico) 3) Antecedentes de evento tromboembólico durante la discontinuación de anticoagulantes 4) Presencia de trombo en el ápice ventricular izquierdo 5) FA y riesgo muy alto de ACV (>6 ptos. en la escala CHA2DS2VASc) 6) Válvula mitral mecánica, válvula aórtica mecánica de antigua generación o válvula aórtica mecánica si coexiste con ≥1 de los siguientes factores de riesgo: FA, antecedentes de evento tromboembólico, disfunción ventricular izquierda de grado importante, hipercoagulabilidad |
|
Nota: en todos los casos es necesario estimar el riesgo de sangrado individual y los potenciales beneficios de la disminución del riesgo de eventos tromboembólico mediante la terapia puente. FA — fibrilación auricular |
| Tabla 4. Dosis de heparinas recomendadas en la terapia puente4 | |
|---|---|
|
Heparina |
Dosis |
|
Enoxaparina |
1 mg/kg VSc 2 × d o 1,5 mg/kg VSc 1 × d |
|
Dalteparina |
100 UI/kg VSc 2 × d o 200 UI/kg VSc 1 × d |
|
Nadroparina |
85 UI/kg VSc 2 × d o 170 UI/kg VSc 1 × d |
|
Heparina no fraccionada |
VSc 2 × dd o en infusión iv. continua a las dosis que permitan prolongar el TTPa hasta 1,5‑2 veces el valor de referencia |
|
TTPa — tiempo de tromboplastina parcial activada, VSc — por vía subcutánea Nota: en las personas con aclaramiento de creatinina <30 ml/min se prefiere la heparina no fraccionada, eventualmente se puede reducir en el 50 % la dosis de la heparina de bajo peso molecular (p. ej. enoxaparina 1 mg/kg 1 × d) y/o modificar la dosis guiándose por la actividad plasmática de anti‑Xa. | |
| Tabla 5. Reglas para suspender los anticoagulantes de acción directa (ACOD) antes de intervenciones quirúrgicas programadasa | ||||||
|---|---|---|---|---|---|---|
|
Aclaramiento de la creatinina (ml/min) |
Rivaroxabánb |
Apixabán |
Dabigatrán | |||
|
Riesgo de sangrado relacionado con la cirugíac,d | ||||||
|
Bajo |
Alto |
Bajo |
Alto |
Bajo |
Alto | |
|
≥80 |
≥24 h |
≥48 h |
≥24 h |
≥48 h |
≥24 h |
≥48 h |
|
50‑79 |
≥24 h |
≥48 h |
≥24 h |
≥48 h |
≥36 h |
≥72 h |
|
30‑49 |
≥24 h |
≥48 h |
≥24 h |
≥48 h |
≥48 h |
≥96 h |
|
15‑29 |
≥36 h |
≥48 h |
≥36 h |
≥48 h |
No utilizar |
No utilizar |
|
<15 |
No hay indicaciones oficiales para su uso | |||||
|
Nota: no debe utilizarse la terapia puente con heparina. a Momento de administración de la última dosis de fármaco antes del día de la cirugía (p. ej. un paciente con alto riesgo de sangrado con una cirugía programada para el miércoles omite la dosis de rivaroxabán el lunes y el martes). b En caso de utilizar rivaroxabán a dosis bajas (2,5 mg 2 × ) como vasoprotección, el fármaco debe discontinuarse 24 h antes de la intervención. c Véase tabla 2. d En caso de cirugía con riesgo de sangrado muy bajo, la intervención debe realizarse con la concentración mínima de ACOD (es decir, 12 o 24 h después de la toma de la última dosis en caso de la administración de, respectivamente, 2 × y 1 × ). A partir de las guías de la ESC (2022) Reimpreso de: Leśniak W., Konsultacje kardiologiczne u chorych poddawanych operacjom pozasercowym. Podsumowanie wytycznych European Society of Cardiology 2022, Med.Prakt., 2022; 12: 20 | ||||||
| Tabla 6. Efecto esperado de anticoagulantes orales directos (ACOD) sobre los resultados de las pruebas de coagulación | ||||
|---|---|---|---|---|
|
|
Dabigatrán |
Apixabán |
Edoxabán |
Rivaroxabán |
|
TP (INR) |
↑a |
↑a |
↑a |
↑a |
|
TTPa |
↑↑ durante el pico de acción y normalmente ↑ con los niveles más bajos de fármaco en sangrea |
↑a,b |
↑a,b |
↑a,b |
|
TCA |
↑ |
↑ |
↑ |
↑ |
|
TT |
↑↑↑a |
– |
– |
– |
|
a Los valores normales no descartan la presencia de fármaco en sangre. b Durante el pico de acción. INR — índice internacional normalizado, TCA — tiempo de coagulación activado, TP — tiempo de protrombina, TT — tiempo de trombina, TTPa — tiempo de tromboplastina parcial activada | ||||
| Tabla 7. Características y dosificación de las sustancias que revierten la acción de anticoagulantes orales directos (ACOD)7,18 | ||||
|---|---|---|---|---|
|
|
Concentrado de factores del complejo de protrombina (CCP) |
Idarucizumab |
Andexanet alfa | |
|
Mecanismo de acción |
Concentrado de los factores de coagulación II, VII, IX y X |
Anticuerpo monoclonal con una afinidad por el dabigatrán |
Afinidad inespecífica por todos los inhibidores del factor Xa | |
|
Indicaciones de la ficha técnica |
Tratamiento de hemorragias o prevención de sangrados quirúrgicos en los enfermos con déficit de los factores protrombínicos adquirido o congénito |
En caso de cirugía no programada u otra intervención urgente o de riesgo vital, o en caso de sangrado no controlado |
En sangrados de riesgo vital | |
|
Bolo (dosis inicial) |
|
2 × 2,5 g iv. (en un intervalo de 15 min) |
Dosis baja |
Dosis altaa |
|
400 mg iv. en 15 min |
800 mg iv. en 30 min | |||
|
Infusión |
25‑50 UI/kg o 2000 UI |
No se utiliza |
480 mg iv. en 2 h (4 mg/min) |
960 mg iv. en 2 h (8 mg/min) |
|
a Indicada si el ACOD se administró <8 h antes y la dosis de apixabán/rivaroxabán fue >5/10 mg, o se desconoce la dosis utilizada. iv. — por vía intravenosa | ||||
| Tabla 8. Ejemplos de bloqueos centrales/profundos y periféricos | ||||
|---|---|---|---|---|
|
Bloqueo central / bloqueo nervioso profundo |
Bloqueo nervioso superficial | |||
|
Bloqueo central: anestesia subaracnoidea anestesia epidural Bloqueo profundo: bloqueo del ganglio estrellado o del plexo cervical profundo bloqueo subclavicular bloqueo del plexo lumbar o sacro bloqueo del plano transverso abdominal simpatectomía lumbar |
Bloqueo del nervio occipital mayor o de los nervios cutáneos del cuello Bloqueo supraclavicular, axilar Bloqueo del nervio cubital, radial Bloqueo de los nervios intercostales Bloqueo del plano del erector espinal (ESP), bloqueos PECS I y PECS II, bloqueo del plano serrato anterior Bloqueo del nervio pudendo o femoral Bloqueo de los nervios safeno, tibial y peroneo (profundo, superficial) Bloqueo de la fascia ilíaca, del canal aductor o del triángulo femoral | |||
|
A partir del artículo 19 de la bibliografía | ||||
| Tabla 9. Momento de interrupción de anticoagulantes antes de un bloqueo central o bloqueo nervioso profundo y de su reinstauración20 | |||||
|---|---|---|---|---|---|
|
Fármaco y dosis |
Tiempo desde la última dosis hasta el bloqueo |
Valores diana de las pruebas de coagulación durante la intervención |
Tiempo desde el bloqueo hasta la reinstauración del fármaco | ||
|
Antagonistas de la vitamina K |
Acenocumarol 3 días, warfarina 5 días (se debe verificar el INR antes de la intervención) |
INR en el rango de referencia |
Dependiendo de la cirugía (basándose en las guías de profilaxis con anticoagulantes o de tratamiento anticoagulante) Por la noche o por la mañana siguiente al bloqueo; ≥4 h | ||
|
Antagonistas anti‑Xa |
A dosis bajas: | ||||
|
|
Rivaroxabán ≤10 mg |
24 h |
No es necesario realizar pruebas |
6‑8 h | |
|
|
Apixabán 2 × 2,5 mg |
36 h | |||
|
A dosis altas: | |||||
|
|
rivaroxabán 20 mg o 2 × 15 mg |
72 h o hasta lograr los valores diana en las pruebas de coagulaciónc |
Concentración del fármaco <30 ng/ml, eventualmente actividad de anti‑Xa ≤0,1 UI/ml |
6‑8 h (valorar la prolongación, si durante la punción aparece sangre en la aguja)a | |
|
|
apixabán 2 × 5 mg, 2 × 10 mg (eventualmente 2 × 2,5 mg, si se cumplen 2 de 3 siguientes: edad ≥80 años, peso ≤60 kg, creatinina ≥133 µmol/l) | ||||
|
|
edoxabán 60 mgb | ||||
|
Dabigatrán |
A dosis bajas: 1 × 220 mg, 1 × 150 mg |
48 h |
No es necesario realizar pruebas |
| |
|
A dosis altas: 2 × 150 mg, 2 × 110 mg |
72 h o hasta lograr los valores diana en las pruebas de coagulación |
Concentración del fármaco <30 ng/ml, como alternativa: tiempo de trombina en el rango de referencia |
24 h después de la cirugía | ||
|
Heparina de bajo peso molecular (HBPM) |
A dosis bajas: ≤50 UI de anti‑Xa/kg/d o ≤40 mg de enoxaparina/d |
12 h (24 h, si la TFGe <30 ml/min/1,73 m2) |
No es necesario realizar pruebas |
4 h (valorar la prolongación hasta 24 h, si durante la punción aparece sangre en la aguja) | |
|
A dosis altas: >50 UI de anti‑Xa/kg/d o >40 mg de enoxaparina/d |
24 h o hasta lograr los valores diana en las pruebas de coagulación (48 h, si la TFGe <30 ml/min/1,73 m2) |
Actividad de anti‑Xa ≤0,1 UI/ml |
≥24 h | ||
|
Heparina no fraccionada |
A dosis bajas: ≤200 UI/kg/d VSc ≤100 UI/kg/d iv. |
4 h |
No es necesario realizar pruebas |
1 h | |
|
A dosis altas: >200 UI/kg/d VSc >100 UI/kg/d iv. |
Valores diana en las pruebas de coagulación (≥6 h para iv., ≥12 h para VSc)d |
Actividad anti‑Xa, TTPa o TCA en el rango de referencia en laboratorio |
1‑2 h | ||
|
Fondaparinux |
A dosis bajas: ≤2,5 mg/d |
36 h |
No es necesario realizar pruebas |
6‑12 h | |
|
A dosis altas: >2,5 mg/d |
Idealmente se debe renunciar al bloqueo, pero si es necesario, tras observar valores diana en las pruebas de coagulación (≥4 días)d |
Actividad de anti‑Xa ≥0,1 UI/ml |
No administrar | ||
|
a No utilizar antagonistas anti‑Xa a dosis altas si se mantiene el catéter epidural o para el bloqueo profundo continuo. INR — índice internacional normalizado, iv. — por vía intravenosa, TCA — tiempo de coagulación activado, TFGe — tasa de filtración glomerular estimada, TTPa — tiempo de tromboplastina parcial activada, VSc — por vía subcutánea | |||||
Bibliografía
- Colacci M., Tseng E.K., Sacks C.A., Fralick M., Oral anticoagulant utilization in the United States and United Kingdom, J. Gen. Intern. Med., 2020; 35: 2505‑2507; doi: 10.1007/s11 606‑020‑05 904‑0
- Omling E., Jarnheimer A., Rose J. y cols., Population‑based incidence rate of inpatient and outpatient surgical procedures in a high‑income country, Br. J. Surg., 2017; 105: 86‑95
- Beyer‑Westendorf J., Gelbricht V., Förster K. y cols., Peri‑interventional management of novel oral anticoagulants in daily care: results from the prospective Dresden NOAC registry, Eur. Heart J., 2014; 35: 1888‑1896
- Douketis J.D., Spyropoulos A.C., Murad M.H. y cols., Perioperative management of antithrombotic therapy: an American College of Chest Physicians clinical practice guideline, Chest, 2022; 162: e207‑e243
- Spyropoulos A.C., Douketis J.D., How I treat anticoagulated patients undergoing an elective procedure or surgery, Blood, 2012; 120: 2954‑2962
- Gallego P., Apostolakis S., Lip G.Y.H., Bridging evidence‑based practice and practice‑based evidence in periprocedural anticoagulation, Circulation, 2012; 126: 1573‑1576
- Halvorsen S., Mehilli J., Cassese S. y cols., 2022 ESC Guidelines on cardiovascular assessment and management of patients undergoing non‑cardiac surgery, Eur Heart J., 2022; 43: 3826‑3924
- Hylek E.M., Regan S., Go A.S. y cols., Clinical predictors of prolonged delay in return of the international normalized ratio to within the therapeutic range after excessive anticoagulation with warfarin, Ann. Intern. Med., 2001; doi: 10.7326/0003‑4819‑135‑6‑200 109 180‑00 008
- Douketis J.D., Spyropoulos A.C., Kaatz S. y cols., Perioperative bridging anticoagulation in patients with atrial fibrillation, N. Engl. J. Med., 2015; 373: 823‑833
- Windyga J., Powikłania leczenia przeciwkrzepliwego, Hematologia, 2010; 1: 142‑150
- Undas A., Zawilska K., Ogólne zasady leczenia przeciwkrzepliwego. En: Gajewski P. (red.). Interna Szczeklika 2022, Medycyna Praktyczna, Kraków, 2022, pp 594‑609
- Healey J.S., Eikelboom J., Douketis J. y cols., Periprocedural bleeding and thromboembolic events with dabigatran compared with warfarin: results from the Randomized Evaluation of Long‑Term Anticoagulation Therapy (RE‑LY) randomized trial, Circulation, 2012; 126: 343‑348
- Garcia D., Alexander J.H., Wallentin L. y cols., Management and clinical outcomes in patients treated with apixaban vs warfarin undergoing procedures, Blood, 2014; 124: 3692‑3698
- Sherwood M.W., Douketis J.D., Patel M.R. y cols., Outcomes of temporary interruption of rivaroxaban compared with warfarin in patients with nonvalvular atrial fibrillation: results from the rivaroxaban once daily, oral, direct factor Xa inhibition compared with vitamin K antagonism for prevention of stro, Circulation, 2014; 129: 1850‑1859
- Shaw J.R., Li N., Vanassche T. y cols., Predictors of preprocedural direct oral anticoagulant levels in patients having an elective surgery or procedure, Blood Adv., 2020; 4: 3520‑3527
- Steffel J., Collins R., Antz M. y cols., 2021 European Heart Rhythm Association practical guide on the use of non‑vitamin k antagonist oral anticoagulants in patients with atrial fibrillation, EP Eur., 2021; 23: 1612‑1676
-
Majeed A., Ågren A., Holmström M. y cols., Management of rivaroxaban‑ or apixaban‑associated major bleeding with prothrombin complex concentrates: a cohort study, Blood., 2017; 130: 1706‑1712
Piran S., Schulman S., Treatment of bleeding complications in patients on anticoagulant therapy, Blood, 2019; 133: 425‑435
- Studzińska D., Mikiewicz M., Szczeklik W., Praktyka kliniczna – opieka okołooperacyjna. Opieka okołooperacyjna nad chorym przyjmującym leki przeciwpłytkowe, Med. Prakt., 2023; 1: 98‑103
- Kietaibl S., Ferrandis R., Godier A. y cols., Regional anaesthesia in patients on antithrombotic drugs: Joint ESAIC/ESRA guidelines, Eur. J. Anaesthesiol., 2022; 39: 100‑132.
 Español
Español
 English
English
 українська
українська