EtiopatogeniaArriba
1. Agente etiológico: parásitos protozoarios del género Leishmania (familia Trypanosomatidae). El género comprende, al menos, 22 especies patógenas para los humanos que se dividen en los subgéneros Viannia (V.) y Leishmania. (L.). Estas especies presentan diferentes tropismos: las especies L (L.) donovani y L. (L.) infantum tienen principal tropismo visceral, siendo los principales agentes causantes de la leishmaniasis visceral, mientras que el resto de las especies tienen tropismo cutaneo. Los complejos de especies L. (L.) tropica, L. (L.) maior, L. (L.) mexicana, L. (V.) guyanensis y L. (V.) brazilienzis causan la mayoría de los casos de leishmaniasis cutánea. Las especies del subgénero Viannia tienen, además, tropismo mucoso. Estas especies tienen diferentes vectores y reservorios, por lo que difieren sus áreas endémicas.
2. Patogenia: la infección comienza cuando los flebotomíneos hembras, al picar, regurgitan promastigotes junto con la saliva y los inoculan en la dermis, donde estos son fagocitados por los macrófagos de la piel. Dentro de los fagolisosomas, se transforman en amastigotes que logran sobrevivir y reproducirse hasta que se produzca la lisis. Una vez liberadas, vuelven a infectar numerosas células fagocíticas de la sangre, la médula, el hígado (células de Kupffer), el bazo, los ganglios linfáticos y la piel (células de Langerhans). En la forma cutánea o mucosa, la presencia de los parásitos genera una reacción inflamatoria granulomatosa crónica con producción factores inflamatorios como IFN-γ por parte de macrófagos y neutrófilos. Esta respuesta ocasiona un edema e induración característica en forma de pápula/nódulo. Posteriormente, con el crecimiento de la reacción granulomatosa, en la zona central del nódulo se produce necrosis con la clásica úlcera cutánea. En el caso de la leishmaniasis visceral, las especies viscerotrópicas infectan macrófagos de órganos hematopoyéticos (hígado, bazo y medula ósea). Las complejas estrategias de supervivencia del parásito en el organismo del huésped, incluso después de un tratamiento clínicamente efectivo, consisten en neutralizar los componentes del complemento e inhibir la liberación de radicales superóxidos y óxido nítrico de los macrófagos, así como la inducción de los linfocitos colaboradores CD4+.
3. Reservorio y vía de transmisión: la infección se transmite a través de artrópodos dípteros de la subfamilia Phlebotominae, principalmente de los géneros Phlebotomus (África, Asia, sur de Europa) o Lutzomyia (Sudamérica y Centroamérica). El reservorio de los parásitos pueden ser animales de compañía (p. ej. perros para L. (L.) infantum), silvestres (p. ej. roedores o marsupiales para L. (V.) brazilienzis) o humanos infectados (p. ej. L (L.) donovani o L. (L.) tropica). Las especies de vectores y reservorios principales suelen estar relacionados con la especie de Leishmania. Se ha descrito la transmisión parenteral (por transfusión sanguínea o consumo de narcóticos intravenosos con agujas y/o jeringuillas compartidas), por trasplante de órgano y congénita.
4. Factores de riesgo: la exposición a vectores en una región endémica de Leishmania es el principal factor de riesgo para contraer la enfermedad. Esto puede suceder en el contexto de un viaje o viviendo en una zona endémica, y dependiendo del ciclo de transmisión de cada especie, se asocia a distintas actividades. La inmunodeficiencia celular se asocia a una peor evolución o respuesta terapéutica.
5. Periodo de incubación y transmisibilidad: el periodo de incubación de la leishmaniasis visceral puede durar entre semanas y años (normalmente entre 2 semanas y 2 meses), y de la leishmaniasis cutánea, entre semanas y meses.
EpidemiologíaArriba
La leishmaniasis está presente en los cinco continentes y es endémica en 102 países o territorios. Los vectores se encuentran en distintos ambientes (desde desérticos a selváticos y de domestico-urbanos a silvestres) de zonas tropicales y subtropicales. Se identifican 3 ecorregiones epidémicas de leishmaniasis visceral en el mundo: África del Este (Etiopia, Eritrea, Kenia, Somalia, Sudan, Sudan del Sur y Uganda) con el 57 % de los casos, subcontinente indio (Bangladesh, Inda y Nepal) con el 18 % y América, donde Brasil concentra casi el total de restante 16 % de los casos. En el caso de la leishmaniasis cutánea, el 95 % de los casos se dan entre las Américas, el Mediterráneo y el Centro y Oriente Medio de Asia. Más del 80 % de los casos ocurren en 7 países: Afganistán, Argelia, Brasil, Colombia, Irak, Pakistán y Siria. Por su parte, la leishmaniasis mucosa se presenta principalmente en América del Sur (Bolivia, Brasil y Perú).
No hay datos exactos sobre la prevalencia de la leishmaniasis. El número de casos nuevos anuales de leishmaniasis cutánea a nivel global se estima en 0,7-1,2 millones, y de leishmaniasis visceral en 0,1-0,4 millones. El número de casos de leishmaniasis cutánea diagnosticada en países no endémicos está en aumento. El mayor número de contagios se ha observado después de viajes a Bolivia y Costa Rica. Los brotes de leishmaniasis suelen aparecer en regiones de conflictos armados y migraciones causadas por ellos (p. ej. últimamente en Siria) o con grandes modificaciones del ambiente.
Cuadro clínico E HISTORIA naturalArriba
El cuadro clínico de la infección por Leishmania depende de varios factores, como la especie de parásito, la virulencia de la cepa y las predisposiciones genéticas, la variabilidad de la respuesta inmune y el estado nutricional del huésped. Las infecciones asintomáticas son posibles. En algunos casos, los síntomas pueden aparecer varios años después de la infección si el huésped presenta trastornos de la inmunidad debido a, p. ej., una infección por VIH o un tratamiento inmunosupresor.
Las dos formas clínicas principales son la leishmaniasis visceral y la cutánea.
1. Leishmaniasis visceral (kala azar): es la forma clínica más grave que puede ocasionar la muerte. Se debe sospechar en personas que hayan estado expuestas al contagio y presenten fiebre (irregular, alta, a veces con 2 picos durante el día y con escalofríos) y esplenomegalia, ocasionalmente acompañada de hepatomegalia, pérdida de masa corporal y pérdida de apetito. La presentación suele ser subaguda, con síntomas que se prolongan durante varias semanas o meses, y a los que se agrega tos, hemorragia nasal, diarrea, vómitos, edemas, linfadenopatías, ictericia (poco común) y oscurecimiento en la coloración de la piel. Son raras las situaciones de progresión más rápida con insuficiencia hepática o síndrome hemofagocítico.
2. Leishmaniasis cutánea: aparece entre 2 y 4 semanas después de la picadura del insecto, que normalmente se produce en las áreas expuestas (extremidades, cara, orejas). Se caracteriza por nódulos inflamatorios, aislados o múltiples, que progresan a ulceraciones. Alrededor de la lesión original pueden formarse nuevas lesiones satélites. La manifestación más típica es la leishmaniasis cutánea localizada, en la que se observa una úlcera crónica de 2-5 cm de diámetro, fondo limpio, color rosado, tejido granuloso, redondeada, de bordes regulares y elevados, indolora y de base indurada (→fig. 19.4-1). En ocasiones, se observa una linfadenopatía local o un trayecto linfangítico nodular. La historia natural depende del agente etiológico, en algunos casos con tendencia a la cicatrización (atrófica y sin anexos) y en otros hacia la crónificación. Existen otro tipo de presentaciones atípicas (nódulos sin ulceración), diseminada (acneiformes) o difusa (nódulos/ placas) que están asociados a distintas especies.
La leishmaniasis mucosa suele presentarse como una complicación de las lesiones cutáneas. Aunque puede aparecer por contigüidad a una lesión cutánea o ser concomitante a esta, lo más común es que se presente con lesiones en los cartílagos de la nariz luego de años de la primoinfección. En los casos de evolución prolongada compromete labios, paladar blando y la laringe.
DiagnósticoArriba
Exploraciones complementarias
1. Identificación del agente etiológico:
1) estudios microscópicos del material extraído de las lesiones cutáneas (raspadura o frotis de muestra de los bordes de la ulceración) o de los órganos del sistema reticuloendotelial en la leishmaniasis visceral (aspirado de bazo: sensibilidad >95 %; análisis de médula o una muestra del hígado: sensibilidad 70-85 %) mediante tinción de Giemsa para detectar amastigotes; el frotis de sangre periférica se caracteriza por una sensibilidad baja; los estudios anatomopatológicos pueden identificar cambios compatibles (granulomas), pero la detección de amastigotes es menor que en otras muestras
2) estudios moleculares (PCR y rt-PCR): se usa el mismo material que en los estudios microscópicos, y sangre
3) cultivo con aislamiento de parásito
4) pruebas serológicas (ELISA, inmunofluorescencia indirecta e inmunocromatografia rK39): poco útiles en la forma cutánea, útiles en la forma visceral (sensibilidad >90 %, especificidad ~80 %)
5) la prueba intradérmica consiste en el análisis de la reacción local a la inyección de promastigotes muertos; se utiliza para diagnosticar la leishmaniasis cutánea en Sudamérica; no tiene presentación comercial.
2. Otras:
1) Análisis de sangre en laboratorio: puede detectarse trombocitopenia, leucopenia, anemia normocítica, hipergammaglobulinemia, hipoalbuminemia, hiperbilirrubinemia y actividad elevada de ALT, AST y fosfatasa alcalina.
2) Pruebas de imagen: son de utilidad en los casos de leishmaniasis visceral. La ecografía y TC axial de abdomen pueden visualizar hepatomegalia, esplenomegalia y/o ascitis, que en las etapas iniciales pueden pasar desapercibidas en el examen físico.
Criterios diagnósticos
El diagnóstico se basa en detectar Leishmania spp. en el análisis microscópico. Sin embargo, debido a las frecuentes dificultades diagnósticas, se recomienda el uso de varios métodos para aumentar las probabilidades de obtener un resultado positivo.
Diagnóstico diferencial
1. Leishmaniasis visceral: malaria, histoplasmosis, esquistosomiasis, neoplasias linfáticas y mieloproliferativas, absceso hepático amebiano, endocarditis infecciosa, cirrosis hepática, tuberculosis.
2. Leishmaniasis cutánea: infecciones cutáneas bacterianas (impétigo, ectima contagioso, carbunco, nocardiosis, actinomicosis, pian, micobacteriosis), dermatomicosis, miasis forunculoide, cáncer de piel, otras enfermedades cutáneas (pioderma gangrenoso, prurigo nodular, sarcoidosis, liquen plano).
TratamientoArriba
Tratamiento causal
La elección del tratamiento depende del tipo de leishmaniasis, la presentación clínica y la especie causante o experiencia local.
1. Leishmaniasis visceral: siempre se utiliza tratamiento sistémico. Se pueden utilizar 3 grupos de fármacos: anfotericina B (liposomal o desoxicolato) por vía parenteral (iv.), compuestos de antimonio pentavalente (estibogluconato de sodio, antimoniato de meglumina) por vía parenteral (iv. o IM) o miltefosina VO (dosificación →Perspectiva latinoamericana). La anfotericina B liposomal presenta la mejor eficacia y el mejor perfil de seguridad. La miltefosina es de utilidad solo en caso de L. donovani. La IDSA recomienda la terapia con antimonio pentavalente en personas inmunocompetentes con leishmaniasis visceral adquirida en áreas con baja prevalencia de especies de Leishmania resistente al antimonio, si no es posible utilizar la anfotericina B o miltefosina.
2. Leishmaniasis cutánea: los tratamientos se dividen en locales y sistémicos. Los tratamientos locales solo se pueden aplicar en caso de lesiones no complicadas (clasificación según IDSA: →tabla 19.4-1). Las opciones son físicas (crioterapia o termoterapia) o químicas (antimoniales pentavalentes intralesionales o paromomicina tópica), solas o en combinación. Los tratamientos sistémicos son de elección en caso de leishmaniasis cutáneas complicadas, lesiones múltiples y compromisos mucosos: anfotericina B (liposomal o desoxicolato) por vía parenteral (iv.), compuestos de antimonio pentavalente (estibogluconato de sodio, antimoniato de meglumina) por vía parenteral (iv. o IM), miltefosina (VO), isetionato de pentamidina o ketoconazol o fluconazol. En algunos pacientes, las lesiones pueden remitir de forma espontánea. Las heridas con cicatrización espontánea no requieren tratamiento. La terapia acelera la curación de las heridas. Además, disminuye el riesgo de recurrencia y aparición de lesiones secundarias en otras localizaciones (dosificación →Perspectiva latinoamericana).
PERSPECTIVA LATINOAMERICANA
1. Criterios de la leishmaniasis cutánea no complicada según la OPS: lesión única de hasta 900 mm2 (diámetro de 3 cm) en cualquier localización, excepto cabeza y regiones periarticulares, ausencia de inmunosupresión y posibilidad de efectuar seguimiento.
2. Métodos de tratamiento y dosificación según la OPS:
1) leishmaniasis visceral (siempre se utiliza tratamiento sistémico)
a) anfotericina B liposomal: 3-5 mg/kg/d iv. durante 3-6 días, hasta una dosis total de 20 mg/kg
b) anfotericina B desoxicolato: 1 mg/kg/d iv. durante 14 días, hasta una dosis total de 800 mg
c) compuestos de antimonio pentavalente (estibogluconato de sodio, antimoniato de meglumina): 20 mg de antimonio/kg iv. o IM durante 28 días
d) miltefosina (solo para L. donovani): 2,5 mg/kg VO en 3 dosis divididas durante 28 días
La elección de antimonio pentavalente se encuentra limitada a situaciones de bajo riesgo de complicaciones al tratamiento.
2) leishmaniasis cutánea
a) tratamiento local
– termoterapia: tras una anestesia local se aplica el electrodo a 50 °C por periodos de 30 s, hasta cubrir toda el área de la lesión; se realizan 1-3 sesiones, con un intervalo de 1 semana
– antimonio pentavalente intralesional: 1-5 infiltraciones de 1-5 ml por sesión cada 3-7 días
b) tratamiento sistémico
– antimonio pentavalente sistémico: 10 a 20 mg Sb+5/kg/d en dosis única diaria durante 20 días; máx. 3 ampollas/d
– anfotericina B liposomal: 3 mg/kg iv. 1 × d durante 6-7 días
– anfotericina B desoxicolato: 0,7-1 mg/kg/d iv. hasta 25-30 dosis
– ketoconazol (L. panamensis y L. Mexicana): 600 mg VO 1 × d durante 4 semanas
– miltefosina (L. guyanensis y L. panamensis): 1,5-2,5 mg/kg (hasta 150 mg) VO en 3 dosis divididas durante 28 días
– isetionato de pentamidina (L. guyanensis): 3-4 mg/kg/d IM en 3-4 dosis en días alternos iv.
3) leishmaniasis mucosal
a) antimonio pentavalente sistémico + pentoxifilina oral: 20 mg Sb+5/kg/d de antimonio pentavalente en dosis única diaria durante 30 días, máx. 3 ampollas/d; 400 mg depentoxifilina cada 8 h durante 30 días
b) anfotericina B liposomal: 2-3 mg/kg iv. hasta completar 3,5 g
c) anfotericina B desoxicolato: 0,7-1 mg/kg/d iv. hasta 25-45 dosis
d) miltefosina: 1,5-2,5 mg/kg VO (hasta 150 mg) en 3 dosis divididas durante 28 días
e) isetionato de pentamidina: IM 3 a 4 mg/kg/d en 7-10 dosis en días alternos.
Tratamiento sintomático
En los casos de leishmaniasis visceral se puede requerir un tratamiento de soporte de las complicaciones.
ComplicacionesArriba
La leishmaniasis cutánea post-kala-azar (post-kala-azar dermal leishmaniasis, PKDL) se manifiesta mediante un exantema maculopapular que dura entre 6 meses y varios años después del tratamiento de la leishmaniasis visceral por L. donovani. En algunos pacientes aparecen nódulos y masas que se asemejan a la lepra. La PKDL se ha descrito en pacientes de países del Cuerno de África y el sur de Asia. La mayoría de los casos son leves y remiten de forma espontánea. Los pacientes pueden ser una fuente de infección para los insectos que transmiten la leishmaniasis.
SITUACIONES ESPECIALESArriba
Embarazo
La leishmaniasis visceral en embarazadas está asociada a un riesgo elevado de muerte fetal e infección congénita del recién nacido. En el tratamiento de la forma visceral durante el embarazo se utiliza la anfotericina B. La miltefosina está contraindicada en embarazadas.
Infección por VIH
Los parásitos del género Leishmania y el VIH influyen en mecanismos de respuesta celular similares, lo que intensifica los efectos clínicos desfavorables en pacientes con coinfección. El desarrollo de la leishmaniasis visceral en las personas infectadas por VIH puede ser grave y/o atípico, con una respuesta insuficiente al tratamiento. En los pacientes con leishmaniasis visceral y VIH, la anfotericina B es el fármaco de primera elección, pero es posible que se necesiten dosis más altas del fármaco. Después del tratamiento, se recomienda una profilaxis farmacológica secundaria, especialmente en los pacientes con un recuento de linfocitos T CD4+ <200/ml. No hay ningún esquema de profilaxis primaria.
PronósticoArriba
Por lo general, el pronóstico es bueno en la forma cutánea. En muchos casos de las regiones endémicas las lesiones remiten de forma espontánea. La leishmaniasis mucosa puede causar una destrucción irreversible de los cartílagos de la nariz, los labios, el paladar blando y la laringe, lo que conlleva un riesgo de obstrucción de vía aérea o sobreinfecciones bacterianas, incluidas las potencialmente mortales. La leishmaniasis visceral es una enfermedad progresiva que, si no se diagnostica ni se trata, puede provocar la muerte. Los factores asociados a un mal pronóstico son anemia grave, enfermedad prolongada, ictericia, malnutrición, edad <1 año y >40 años, sobreinfecciones, sangrados de mucosas, síntomas gastrointestinales, neutropenia (<500/μl), trombocitopenia (<50 000/μl) y alteraciones de la inmunidad (VIH/sida, trasplante, etc.).
PrevenciónArriba
Métodos específicos
No existen.
Métodos no específicos
1. Protección frente a las picaduras de los insectos vectores (→Métodos inespecíficos de protección contra los vectores).
2. Limitación del reservorio del parásito, lo que incluye el tratamiento de los pacientes infectados (incluidas las personas con PKDL).
Notificación obligatoria
Sí.
TABLAS Y FIGURAS
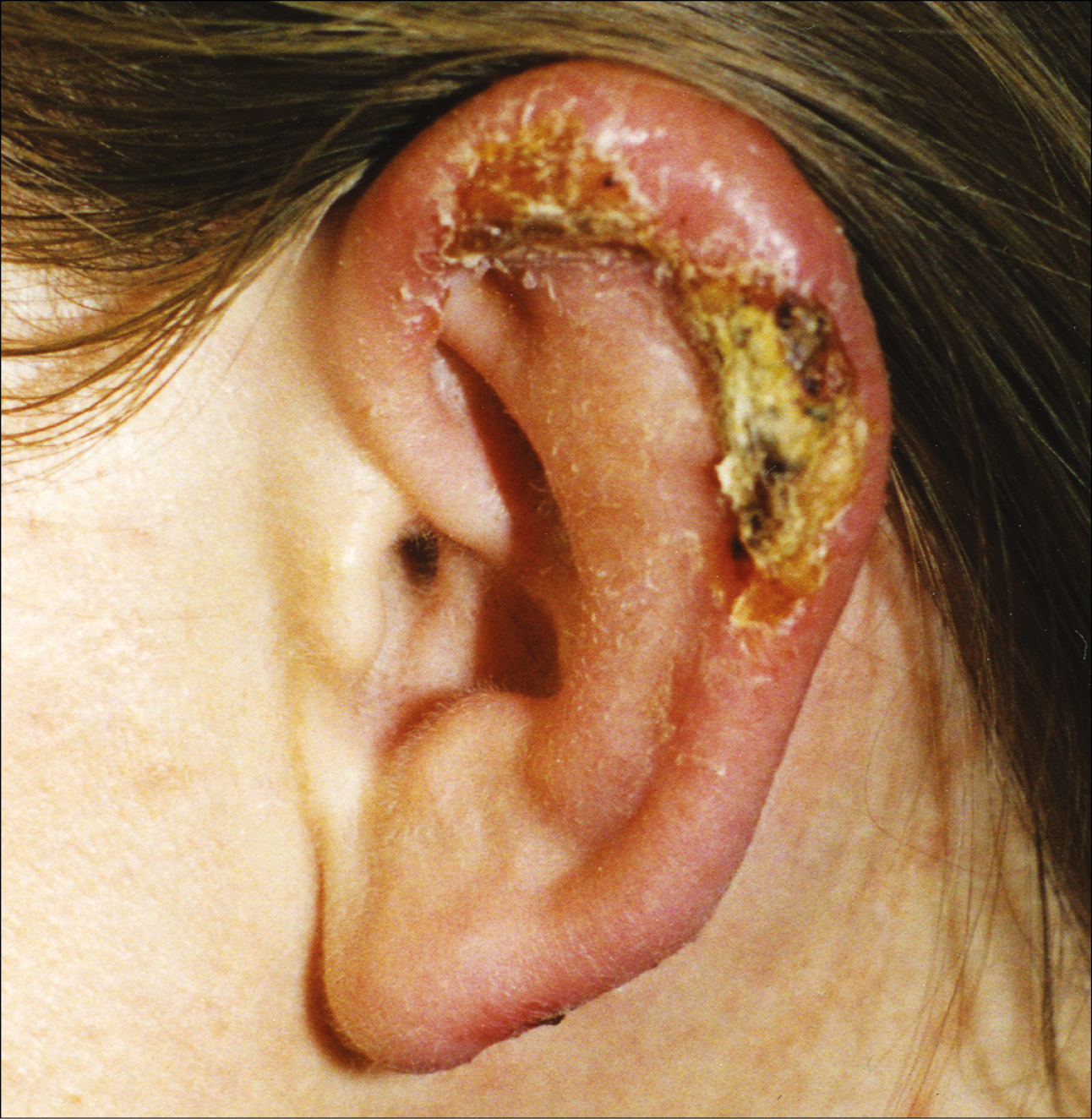
Fig. 19.4-1. Leishmaniasis cutánea: ulceraciones cubiertas por costra en la oreja
Criterios de leishmaniasis cutánea complicada según IDSA y ASTMH 2016
|
1) Infección por una especie de Leishmania asociada a riesgo de desarrollar leishmaniasis mucosa, principalmente en Bolivia, Perú y Brasil
2) >4 lesiones cutáneas de >1 cm
3) Lesiones cutáneas de >5 cm
4) Nódulos subcutáneos
5) Linfadenopatía localizada (>1 cm de aumento)
6) Tratamiento tópico dificultado por el tamaño o la ubicación de las lesiones cutáneas
7) Afectación de cara, dedos de manos o pies y genitales externos
8) Inmunodepresión en una persona infectada
9) Fracaso de la terapia local 2-3 meses después de la conclusión del tratamiento
|
|
A partir de: Aronson N., Herwaldt BL. y cols,. Diagnosis and Treatment of Leishmaniasis: Clinical Practice Guidelines by the Infectious Diseases Society of America (IDSA) and the American Society of Tropical Medicine and Hygiene (ASTMH), Clin Infect Dis., 2016 Dec 15; 63(12): 1539-1557. doi: 10.1093/cid/ciw742
|
 Español
Español
 English
English
 українська
українська





