Definición y etiopatogeniaArriba
La definición de neumonía adquirida en la comunidad (NAC) de la BTS distingue las NAC diagnosticadas en el ámbito ambulatorio y en el hospital.
Criterios de definición de NAC en el ámbito ambulatorio:
1) síntomas de infección aguda de vías respiratorias bajas (tos y ≥1 de los síntomas: disnea, dolor pleurítico, hemoptisis)
2) nuevas anomalías locales objetivadas en la exploración física del tórax
3) ≥1 de los síntomas generales (sudoración, escalofríos, mialgias o temperatura corporal ≥38 °C)
4) ausencia de otras causas que expliquen los síntomas.
PERSPECTIVA LATINOAMERICANA
En América Latina la confirmación del diagnóstico mediante una radiografía y/o TC de tórax constituye el estándar de oro.
Criterios de definición de NAC diagnosticada en el hospital:
1) síntomas y signos que indican infección aguda de vías respiratorias bajas
2) en la radiografía de tórax: presencia de opacidad no observada previamente que no se puede explicar de otra manera (p. ej. por edema pulmonar o infarto pulmonar).
Estas definiciones no incluyen a pacientes con enfermedad neoplásica o inmunodeprimidos, ingresados por neumonía en los servicios de oncología, hematología, cuidados paliativos, enfermedades infecciosas o de tratamiento del sida.
Agentes etiológicos: la NAC está causada por un número reducido de especies de microorganismos, siendo los más frecuentes: Streptococcus pneumoniae, Haemophilus influenzae, Moraxella catarrhalis, Staphylococcus aureus, estreptococos del grupo B, bacterias aerobias gramnegativas, como Enterobacteriaceae (p. ej. Escherichia coli), y los microorganismos atípicos como Mycoplasma pneumoniae, Chlamydophila pneumoniae y Legionella pneumophila. En un 30-50 % de los casos la NAC tiene etiología viral, siendo los más frecuentes: SARS-CoV-2 (durante la pandemia), otros coronavirus (CoV-229E, CoV-NL63, CoV-OC43, CoV-HKU1), virus de gripe (A y B), rinovirus, virus de paragripe, adenovirus, VRS, bocavirus y metaneumovirus humanos. En ~25 % de los enfermos se producen infecciones polimicrobianas; más frecuentemente por S. pneumoniae y C. pneumoniae o S. pneumoniae y virus de gripe o paragripe.
PERSPECTIVA CHILENA
En Chile los principales agentes causales de la NAC en el huésped inmunocompetente son: Streptoccoccus pneumoniae (30 %), H. influenzae (5 %), virus respiratorios (30 %) y microorganismos atípicos (10 %), no logrando identificar el agente causal en un tercio de los casos. Los bacilos gramnegativos y S. aureus ocasionan <5 % de los casos.
Los microorganismos entran en las vías respiratorias bajas más frecuentemente por microaspiración del contenido de las vías respiratorias altas, aspiración del contenido de la cavidad oral y vías respiratorias altas, por inhalación (gotas de secreciones de vías respiratorias de enfermo con infección viral con tos, y en la infección por Legionella a través de inhalación del aerosol de gotas de agua que contienen esta bacteria, así como en neumonías fúngicas raras, por inhalación de esporas y pequeños fragmentos del micelio). La vía hematógena de infección es muy rara (p. ej. en usuarios de drogas iv.).
CUADRO CLÍNICO E HISTORIA NATURALArriba
1. Síntomas (en general de inicio agudo): temperatura elevada, en general ≥38 °C, escalofríos y sudoración, dolor torácico de características pleuríticas, tos, a veces expectoración purulenta y disnea (en algunos enfermos). En enfermos de edad avanzada las manifestaciones asociadas a la NAC son más a menudo inespecíficas y la fiebre se presenta con menor frecuencia; a veces el primer síntoma es una difícil conexión con el medio por alteración de la conciencia. Como la neumonía es una de las causas más frecuentes de sepsis, las primeras manifestaciones pueden incluir hipotensión, alteraciones de la conciencia o disfunción de otros órganos y sistemas (p. ej. renal o hepática).
2. Signos: taquipnea, taquicardia; sobre el área del infiltrado inflamatorio: broncofonía, matidez a la percusión, crepitaciones, a veces soplo bronquial; en caso de derrame pleural se aprecia matidez a la percusión, abolición de las vibraciones vocales y disminución de los ruidos respiratorios.
3. Historia natural: depende sobre todo de la edad del enfermo, de las enfermedades concomitantes y del agente etiológico. Las neumonías causadas por estafilococos, Legionella y bacterias anaerobias suelen presentar un curso más grave que las neumonías por neumococos o micoplasma.
DiagnósticoArriba
Exploraciones complementarias
1. Pruebas de laboratorio: características de proceso inflamatorio. Los niveles de proteína C-reactiva sérica están elevados en la mayoría de los pacientes; una concentración <20 mg/l es un argumento en contra de una etiología bacteriana. A la hora de decidir sobre iniciar o interrumpir la antibioticoterapia, también es útil determinar la PCT sérica (→tabla 1). La leucocitosis con predominio de neutrófilos orienta a una etiología bacteriana.
PERSPECTIVA CHILENA
En Chile, en los enfermos con sospecha clínica y confirmación radiológica de NAC se recomienda iniciar antibioticoterapia empírica independientemente de la concentración inicial de PCT. Se sugiere emplear la PCT sérica en la suspensión de antibióticos en la NIH o VAP.
2. Valoración de la oxigenación de la sangre: pulsioximetría (posible hipoxemia); en enfermos con riesgo de hipercapnia (p. ej. con EPOC), con SpO2 <92 % y con neumonía grave, realizar gasometría arterial o de sangre capilar arterializada.
3. Pruebas de imagen: el estudio radiológico de tórax es la técnica de elección en el diagnóstico de neumonía. Está indicado a la hora de diferenciar una bronquitis aguda de una neumonía en caso de manifestaciones de infección de las vías respiratorias inferiores, y ≥1 de las siguientes alteraciones: taquicardia (>100/min), taquipnea (>24/min), temperatura corporal >38 °C o alteraciones focales en la auscultación pulmonar.
Radiografía de tórax. En proyección posteroanterior (PA) y lateral: opacidades parenquimatosas (en la mayoría de los casos la radiografía basta para establecer el diagnóstico; en caso de deshidratación importante los hallazgos pueden evidenciarse solo después de hidratar al paciente; en ~7 % de los enfermos las lesiones parenquimatosas aparecen incluso 72 h después de la aparición de las manifestaciones clínicas). La radiografía no permite determinar la etiología de la neumonía, pero con precaución puede ayudar a sospecharla (infiltrado sólido de distribución segmentaria o lobar sugiere neumonía por neumococos; lesiones multifocales con tendencia a la cavitación sugieren una neumonía estafilocócica; las lesiones en los lóbulos superiores, sobre todo de pulmón derecho, con signos de cavitación sugieren infección por K. pneumoniae).
La TC es mucho más sensible que la radiografía para detectar las lesiones en el parénquima pulmonar y es más eficaz para detectar complicaciones. La TC también es útil para descartar la neumonía en los pacientes con manifestaciones clínicas de una infección del aparato respiratorio y cuadro radiológico incierto.
La ecografía a veces permite detectar signos de infiltración del parénquima pulmonar, sin embargo, un resultado negativo no descarta la neumonía (sensibilidad 80-90 %, especificidad 70-90 %, en función de la experiencia del examinador).
4. Pruebas microbiológicas:
1) Cultivos de esputo y hemocultivo. Indicaciones: neumonía grave, uso de tratamiento empírico contra SARM, antecedentes de infección por SARM o P. aeruginosa, hospitalización o tratamiento antibiótico parenteral en los últimos 90 días.
2) Cultivo de otro material: lavado bronquial, fluido de lavado broncoalveolar (el umbral de corte para diferenciar entre la colonización y la infección es de 104 UFC/ml), material de las vías respiratorias bajas obtenido mediante un cepillo (PSB, umbral de corte recomendado para diferenciar entre la colonización y la infección es de 103 UFC/ml), líquido pleural, y en casos especiales las muestras obtenidas a través de la punción transtorácica del infiltrado pulmonar o del aspirado de la punción traqueal.
3) Antígeno de L. pneumophila en la orina (solo detecta el serogrupo 1): en enfermos con neumonía grave y en caso de sospecha de legionelosis (foco de legionelosis o un viaje reciente).
4) Antígeno de S. pneumoniae en orina (en enfermos con neumonía grave; sensibilidad 50-80 %, especificidad ~90 %) o en el líquido pleural (sensibilidad y especificidad casi del 100 %).
5) PCR: en el diagnóstico de infecciones causadas por Chlamydophila, Francisella tularensis, L. pneumophila, M. pneumoniae, Nocardia asteroides, S. pneumoniae, Pneumocystis jiroveci, Toxoplasma gondii, Coccidioides, Aspergillus, Mycobacterium tuberculosis. Los kits diagnósticos Multiplex PCR permiten una identificación simultánea de distintos patógenos responsables de infecciones respiratorias bajas (se deben realizar [a partir del esputo o el aspirado traqueal] en enfermos con neumonía grave cuando se considera la posibilidad de utilizar antibióticos no habituales).
5. Broncoscopia. Proporciona material para estudio mediante lavado bronquial, lavado broncoalveolar (LLBA), muestras de parénquima pulmonar (especialmente importante ante la sospecha de infecciones oportunistas) y de ganglios linfáticos. Durante el estudio también se puede eliminar secreciones bronquiales acumuladas.
6. Toracocentesis (→Punción pleural (toracocentesis)) y pruebas bioquímicas, citológicas y microbiológicas del líquido pleural: considerar en caso de derrame pleural.
Manejo diagnóstico
Se debe tomar en cuenta la neumonía en presencia de síntomas indicativos de infecciones del aparato respiratorio, en algunos enfermos con alteraciones en las pruebas de imagen torácicas y en los pacientes con sepsis. En cada enfermo admitido al hospital se debe solicitar:
1) radiografía de tórax
2) hemograma de sangre periférica con recuento diferencial de leucocitos
3) determinación de la proteína C-reactiva (eventualmente de procalcitonina), urea, creatinina, sodio y potasio, bilirrubina, AST y ALT en suero
4) estudio de oxigenación de sangre (pulsioximetría y eventualmente gasometría arterial)
5) otras pruebas en función de la situación clínica.
La ineficacia del tratamiento empírico inicial obliga a una intensiva búsqueda del agente etiológico y a la realización de un nuevo diagnóstico diferencial.
Criterios diagnósticos
→Definición y etiopatogenia.
Valoración de la gravedad de la enfermedad
Para tomar la decisión sobre el lugar del tratamiento se debe utilizar la escala CRB-65 (→fig. 1) o escala CURB-65, que además incluye la concentración de urea (→fig. 2). Asimismo se utiliza el índice PSI/PORT (→tabla 2). En las recomendaciones de la ERS/ESICM/ESMID/ALAT (2023) se propone considerar que la NAC es grave cuando requiere tratamiento en la UCI.
Diagnóstico diferencial
1. Enfermedades infecciosas: COVID-19, gripe, bronquitis aguda, infección aguda de la vía respiratoria alta o baja, tuberculosis pulmonar, exacerbación de asma, EPOC o de bronquiectasias.
2. Enfermedades no infecciosas: insuficiencia ventricular izquierda aguda o exacerbación de insuficiencia cardíaca crónica, SDRA, embolismo pulmonar, aspiración/neumonía por químicos, enfermedades intersticiales pulmonares (p. ej. neumonía por hipersensibilidad, neumonía organizada criptogénica, neumonía eosinofílica, neumonía intersticial aguda, daño pulmonar inducido por fármacos, daños por radiación, lesiones intersticiales en el curso de conectivopatías sistémicas), cáncer de pulmón y atelectasia.
TRATAMIENTOArriba
Recomendaciones generales
1. Tratamiento ambulatorio: no fumar, reposo, ingesta abundante de líquidos; prescribir paracetamol o AINE para bajar la fiebre y disminuir el eventual dolor pleurítico.
2. Tratamiento hospitalario:
1) Oxigenoterapia bajo control de SpO2 (en los enfermos con EPOC bajo control de gasometría arterial repetida periódicamente), para obtener PaO2 ≥60 mm Hg y SpO2 94-96% (en enfermos con EPOC y otros con riesgo de hipercapnia: 88-92 %). Considerar la oxigenoterapia nasal de alto flujo (ONAF) en los pacientes con cociente PaO2/FiO2 disminuido sin aumento evidente de esfuerzo respiratorio. Si se observan signos de hipoventilación (hipercapnia) y de esfuerzo respiratorio elevado → considerar la VNI.
2) Valorar el estado de hidratación y nutrición del enfermo; si está indicado, perfundir líquidos y utilizar suplementos nutricionales.
3) Ante la presencia de derrame pleural → toracocentesis temprana, en caso de empiema pleural y en algunos enfermos con derrame paraneumónico complicado → drenaje pleural.
4) En enfermos con NAC grave considerar la administración de metilprednisolona iv. 0,5 mg/kg 2 × d durante 5 días; sin embargo, los glucocorticoides no pueden administrarse de manera rutinaria. Según las guías ATS/IDSA, el shock séptico resistente al tratamiento es una indicación para administrar glucocorticoides en la NAC.
Antibioticoterapia
1. En enfermos derivados al hospital con sospecha de NAC considerar el inicio inmediato del tratamiento antibiótico si el estado del enfermo es grave o se prevé una demora en la hospitalización (>2 h). En los enfermos ingresados empezar la antibioticoterapia lo más rápido posible después de establecer el diagnóstico, estrictamente en un plazo ≤4 h.
2. Elección del antibiótico: tratamiento empírico inicial →fig. 3.
Si se conoce el agente etiológico →tabla 3. En el hospital, cuando el estado clínico del enfermo lo permite → cambiar el antibiótico de iv. a VO (utilizar el mismo fármaco u otro fármaco del mismo grupo).
3. Duración del tratamiento: ≥5 días, 48 h desde la estabilidad clínica; en NAC causada por SARM o P. aeruginosa: 7 días. Un tratamiento más prolongado está indicado en caso de neumonía necrótica, complicaciones (abscesos pulmonares, exudado paraneumónico, empiema pleural) y focos extrapulmonares de la infección.
Criterios de estabilidad clínica:
1) temperatura corporal <37,8 °C (según algunos expertos <37,2 °C)
2) pulso ≤100/min
3) presión arterial sistólica ≥100 mm Hg
4) SpO2 ≥90 % o PaO2 ≥60 mm Hg (al respirar aire ambiente)
5) posibilidad de recibir alimentación VO
6) ausencia de alteraciones de la conciencia. Si no se observa una mejoría esperada, no modificar la antibioticoterapia antes de 3 días del tratamiento.
PERSPECTIVA LATINOAMERICANA
El tratamiento utilizado en América Latina se basa en la actualización de las recomendaciones del Grupo de Trabajo de la Asociación Latinoamericana del Tórax (ALAT) sobre la neumonía adquirida en la comunidad (2004).
En Chile el tratamiento se basa en la actualización del Consenso Chileno de Neumonía Adquirida en la Comunidad en Adultos (2023).
vigilanciaArriba
Enfermos tratados en condiciones ambulatorias
Pruebas de control después de 48 h o antes, si aparecen síntomas preocupantes. Si no hay mejoría, considerar derivar al enfermo al hospital, entre otros fines, para realizar radiografía de tórax.
Enfermos tratados en hospital
1. Observar: temperatura corporal, frecuencia respiratoria, pulso, presión arterial, estado de conciencia y SpO2; inicialmente ≥2 × d y con mayor frecuencia en enfermos con neumonía grave. El estado general de los enfermos que han recibido un antibiótico adecuado mejora en el transcurso de 24-48 h. En este caso se observa una remisión de la fiebre, taquicardia y taquipnea.
2. Si los signos clínicos remiten en 5-7 días, no realizar radiografía de tórax antes del alta hospitalaria. Si no se ha producido mejoría satisfactoria → repetir la determinación de proteína C-reactiva o PCT y la radiografía de tórax.
3. Si el tratamiento empírico inicial es ineficaz → buscar de forma intensiva el agente etiológico resistente a los antibióticos utilizados y realizar de nuevo el diagnóstico diferencial.
4. No dar de alta a los enfermos que en las últimas 24 h han tenido ≥2 de los siguientes síntomas: temperatura corporal >37,5 °C, frecuencia respiratoria ≥24/min, frecuencia cardíaca >100/min, presión arterial sistólica ≤90 mm Hg, SpO2 <90 % al respirar aire atmosférico, trastornos de conciencia, incapacidad de comer sin ayuda. Considerar prorrogar el alta hospitalaria en los enfermos con temperatura corporal >37,5 °C.
5. A cada enfermo indicar la fecha de la visita de control después de ~6 semanas.
PERSPECTIVA CHILENA
En Chile en un paciente hospitalizado por NAC se recomienda realizar control ambulatorio precoz en 1-2 semanas para prevenir las complicaciones asociadas, como descompensación de enfermedades crónicas, descompensación cardiovascular o pobre respuesta al tratamiento antibiótico empírico.
ComplicacionesArriba
1. Derrame pleural y empiema pleural →Exudado pleural relacionado con infección.
2. Absceso pulmonar: colección de pus en el parénquima pulmonar, más frecuentemente a consecuencia de neumonía estafilocócica, producida por bacterias anaerobias, K. pneumoniae o Pseudomonas aeruginosa. Los síntomas son parecidos a los de neumonía. El diagnóstico se realiza sobre la base del examen radiológico; la TC es más precisa (cavidad con nivel de contenido líquido en el parénquima pulmonar). Tratamiento: antibioticoterapia y drenaje postural; en los pocos casos sin mejoría → resección quirúrgica. Tratamiento empírico inicial: antibiótico β-lactámico con inhibidor de β-lactamasa (p. ej. ampicilina con sulbactam 3,0 g 4 × d iv. o amoxicilina con ácido clavulánico 1,2 g 3-4 × d iv.) o carbapenem (imipenem, meropenem). No utilizar clindamicina como fármaco de primera línea, salvo en enfermos alérgicos a antibióticos β-lactámicos (600 mg 3 × d iv., a continuación 150-300 mg 4 × d VO). El metronidazol (500 mg 4 × d) debe utilizarse únicamente en combinación con la penicilina (no en monoterapia). Cuando el agente etiológico y su farmacosensibilidad son conocidos → administrar un tratamiento dirigido. Duración del tratamiento: hasta el cierre de la cavidad del absceso (en general 4-7 semanas). El tratamiento quirúrgico es excepcional. Está indicado en abscesos pulmonares grandes (≥6-8 cm) que persisten >12 semanas a pesar del tratamiento conservador.
Situaciones especialesArriba
Neumonía en inmunodeprimidos
Diagnóstico: estos enfermos son especialmente susceptibles a la infección por micobacterias tuberculosas y no tuberculosas, hongos (Aspergillus fumigatus, Candida albicans, Pneumocystis jiroveci) y virus. Identificar el agente etiológico realizando: examen microscópico del esputo (permite el diagnóstico de neumocistosis y tuberculosis, mientras que el aislamiento de los hongos Aspergillus y Candida en el esputo no siempre confirma la etiología), cultivo del esputo, hemocultivo, broncoscopia + lavado bronquial o LBA, eventualmente biopsia pulmonar transbronquial. En casos dudosos considerar biopsia pulmonar quirúrgica.
Tratamiento: en la mayoría de los enfermos empezar antes de la identificación del agente etiológico. Tras excluir inicialmente la tuberculosis y neumocistosis mediante el examen del esputo → administrar tratamiento antibiótico efectivo contra microorganismos grampositivos y gramnegativos, incluyendo P. aeruginosa (como en la NIH en enfermos hospitalizados ≥5 días →más adelante). Si no se ha descartado la infección por estafilococo resistente a meticilina (SARM) → añadir vancomicina o linezolid. En caso de sospecha de legionelosis → macrólido o fluoroquinolona. No administrar fármacos utilizados por el enfermo últimamente a modo de profilaxis. Si el enfermo tiene fiebre durante 4 días después de emplear el tratamiento anteriormente mencionado → añadir un fármaco antifúngico.
TABLAS Y FIGURAS
Uso de la procalcitonina (PCT) en la toma de decisiones sobre el tratamiento antibiótico de la neumonía adquirida en la comunidada
|
Concentración de PCT (µg/l)
|
Probabilidad de infección bacteriana
|
Antibioticoterapia
|
Actuación adicional
|
|
<0,1a
|
Muy baja
|
Nob
|
Considerar repetir la determinación de PCT a las 6-24 h y tomar la decisión sobre el tratamiento según el resultado
|
|
0,1-0,25
|
Baja
|
|
0,25-0,5
|
Alta
|
Síc
|
Actuación según el curso de la enfermedad, considerar repetir la determinación de PCT en días 2-3, 4-5 y 6-8, y opcionalmente 10 del tratamiento
|
|
>0,5
|
Muy alta
|
|
a Algunos autores sugieren utilizar 2 puntos de corte: 0,25 µg/l en enfermos con infecciones leves o moderadas en unidades no quirúrgicas (utilizar escalas qSOFA, MEDS, NEWS) y 0,5 µg/l para enfermos que requieren tratamiento en la UCI. En las guías ATS/IDSA (2019) en los enfermos con sospecha clínica y confirmación radiológica de NAC se recomienda iniciar antibioticoterapia empírica independientemente de la concentración inicial de PCT.
b Considerar la antibioticoterapia a pesar de una concentración baja de PCT en caso de riesgo vital inminente, inestabilidad respiratoria y/o circulatoria, necesidad de tratamiento en UCI, manifestaciones de empiema pleural y resultados positivos de pruebas microbiológicas (p. ej. que detectan antígeno de estreptococo o Legionella).
c Suspender la antibioticoterapia en enfermos tratados en el hospital en un servicio de cuidados no intensivos cuando la concentración de PCT <0,25 µg/l (en UCI <0,5 µg/l). Si la concentración máxima de PCT fue muy alta, considerar la suspensión del tratamiento cuando la concentración de PCT baje un 80-90 %. La persistencia de concentraciones elevadas de PCT indica fracaso del tratamiento.
A partir de: Clin. Chest Med., 2011; 32: 417-430, modificado
|
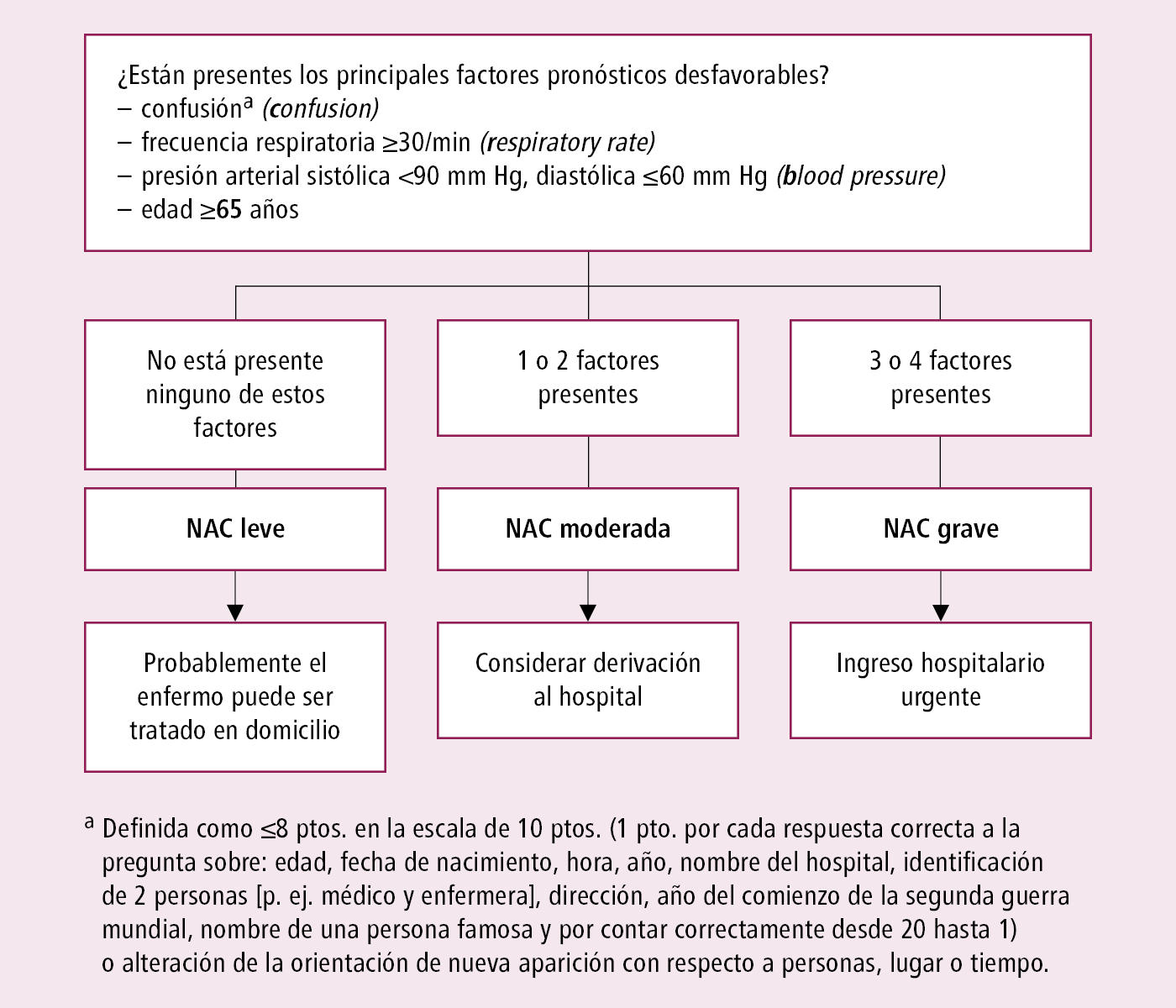
Fig. 3.13-1. Valoración de la gravedad de la neumonía adquirida en la comunidad en el paciente ambulatorio: escala CRB-65 (a partir de las guías BTS 2009 y NICE 2014)
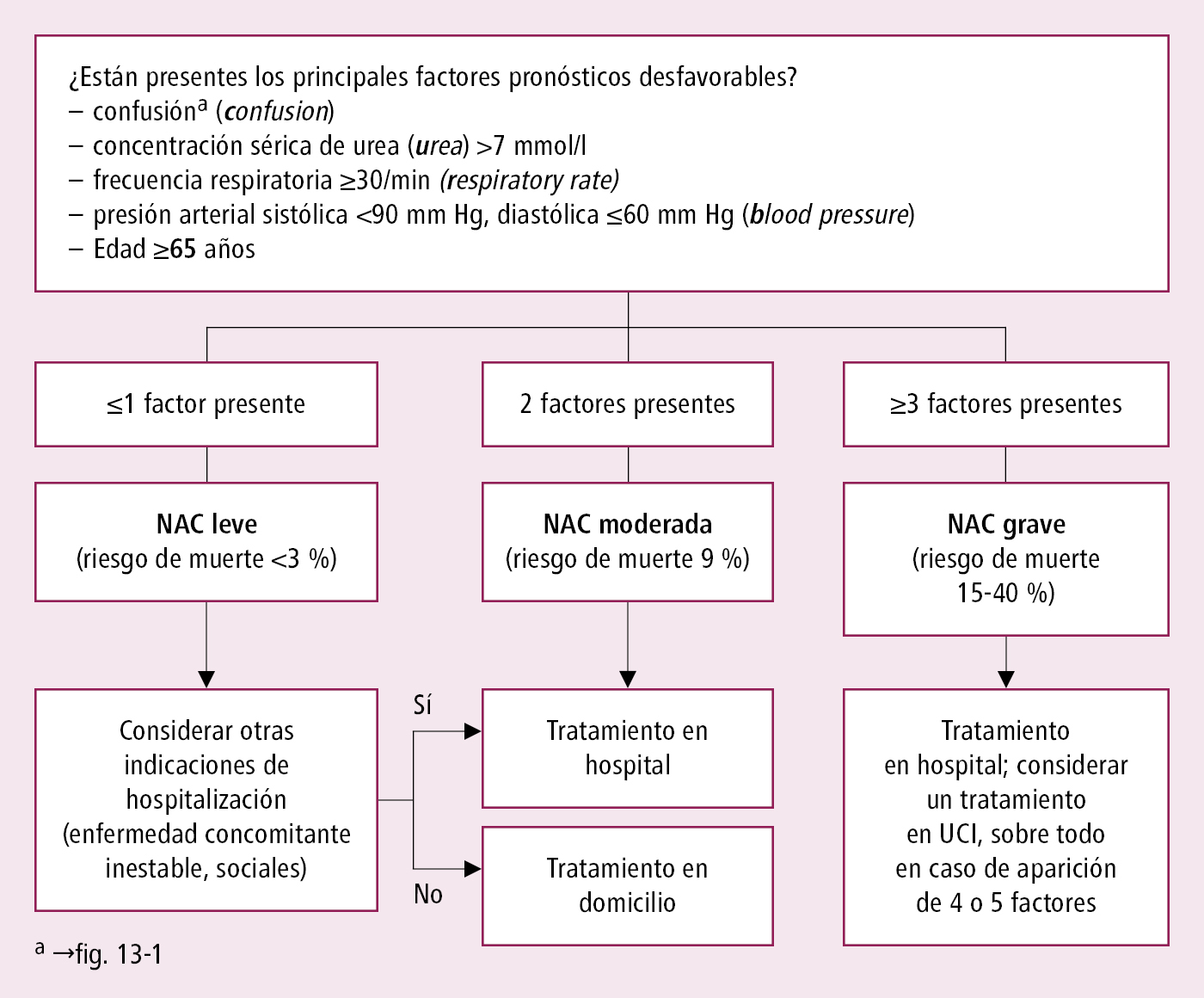
Fig. 3.13-2. Valoración de la gravedad de la neumonía adquirida en la comunidad en el paciente ambulatorio: escala CURB-65 (a partir de las guías BTS 2009 y NICE 2014)
Escala PSI/PORT
|
Factor de riesgo
|
Puntuación
|
|
Edad
|
Hombres: edad en años
Mujeres: edad en años – 10
|
|
Estancia en un centro de cuidados
|
10
|
|
Enfermedad neoplásica activa
|
30
|
|
Enfermedad hepática crónica
|
20
|
|
Insuficiencia cardíaca
|
10
|
|
Enfermedades cerebrovasculares
|
10
|
|
Enfermedad renal crónica
|
10
|
|
Trastornos de la conciencia
|
20
|
|
Frecuencia respiratoria ≥30/min
|
20
|
|
Presión arterial sistólica <90 mm Hg
|
20
|
|
Temperatura corporal <35 °C o ≥40 °C
|
15
|
|
Pulso ≥125/min
|
10
|
|
pH de sangre arterial <7,35
|
30
|
|
Niveles séricos de urea >11 mmol/l (66,1 mg/dl; nitrógeno ureico en la sangre [BUN] >30 mg/dl)
|
20
|
|
Concentración de sodio <130 mmol/l
|
20
|
|
Glucemia ≥14 mmol/l (250 mg/dl)
|
10
|
|
Hematócrito <30 %
|
10
|
|
PaO2 <60 mm Hg o SpO2 ≤90 %
|
10
|
|
Derrame pleural
|
10
|
|
Evaluación de riesgo
|
Grupo
|
Riesgo de muertea
|
Dónde tratar
|
|
Edad ≤50 años sin factores de riesgo adicionales
|
I
|
0,1 %
|
En ambulatorio (en algunos enfermos puede ser necesaria la asistencia médica en domicilio)
|
|
≤70 ptos.
|
II
|
0,6 %
|
En ambulatorio, algunos enfermos pueden beneficiarse de una breve hospitalización en el servicio de observación
|
|
71-90 ptos.
|
III
|
0,9 %
|
En ambulatorio o en hospital, en función de los factores adicionales, incluidos los cuidados en domicilio
|
|
91-130 ptos.
|
IV
|
9,3 %
|
Hospitalb
|
|
>130 ptos.
|
V
|
27 %
|
Hospitalb
|
|
a Riesgo de muerte a los 30 días
b Los enfermos en estado general grave que requieren asistencia ventilatoria, de la función cardiovascular o de otros sistemas deben estar hospitalizados en las unidades de cuidados intensivos.
A partir de: N. Engl. J. Med., 1997; 336: 243, modificado
|
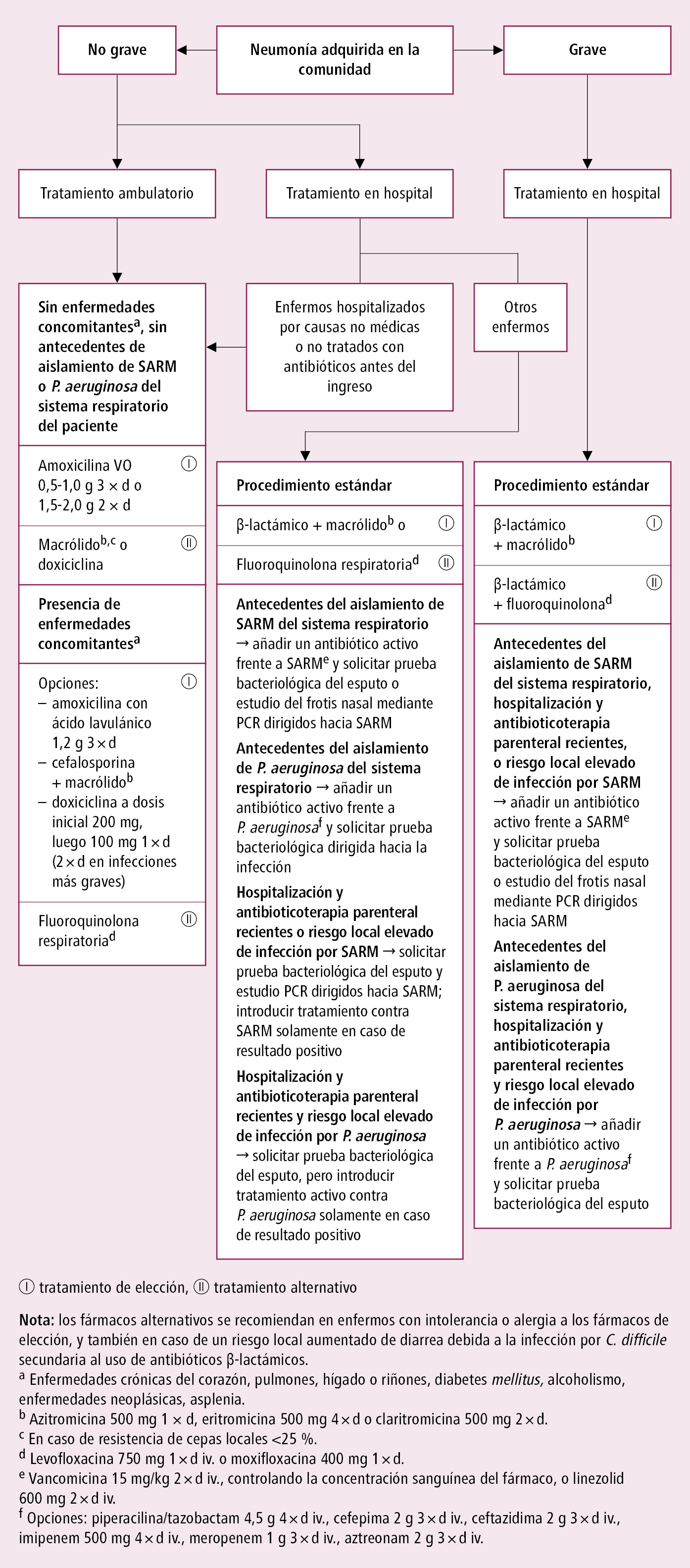
Fig. 3.13-3. Tratamiento empírico inicial en enfermos adultos con neumonía adquirida en la comunidad (a partir de las guías BTS 2009, ERS/ESCMID 2011 y ATS/IDSA 2019, modificado)
Antibioticoterapia en la neumonía según el agente etiológicoa
|
Microorganismo
|
Tratamiento
|
|
de elección
|
alternativo
|
|
Streptococcus pneumoniae
|
Opciones:
– amoxicilina VO 1 g 3 × d
– bencilpenicilina iv. 1,2 g (2 mill. UI) 4 × dc
|
Opciones:
– ampicilina iv. 1-2 g 4 × d
– macrólidob
– cefotaximad iv. 1-2 g 3 × d
– ceftriaxona iv. 2 g 1 × d
– cefuroxima iv. 0,75-1,5 g 3 × d
– levofloxacina, moxifloxacina, vancomicina, teicoplanina o linezolide
|
|
Haemophilus influenzae
|
|
|
Cepas no productoras de β-lactamasa
|
Opciones:
– amoxicilina VO 500 g 3 × d
– ampicilina iv. 500 g 4 × d
|
Opciones:
– cefotaxima iv. 1-2 g 3 × d
– ceftriaxona iv. 2 g 1 × d
– cefuroxima iv. 0,75-1,5 g 3 × d
– fluoroquinolonaf VO o iv.
|
|
|
Cepas que producen β-lactamasa
|
– amoxicilina con ácido clavulánico VO 625 mg 3 × d o iv. 1,2 g 3 × d
|
|
Moraxella catarrhalis
|
Opciones:
– amoxicilina con ácido clavulánico como más arriba
– fluoroquinolonaf
|
Opciones:
– macrólidob
– cefalosporina II o III generación
|
|
Mycoplasma pneumoniae y Chlamydophila pneumoniae
|
Macrólidob
|
Opciones:
– doxiciclina VO o iv., dosis inicial 200 mg, a continuación 100 mg 1 × d (2 × d en infecciones más graves)
– fluoroquinolonaf VO o iv.
|
|
Chlamydia psittaci y Coxiella burnetii
|
Doxiciclina VO o iv., dosis inicial 200 mg, a continuación 100 mg 1 × d (2 × d en infecciones más graves)
|
Macrólidob
|
|
Staphylococcus aureus
|
|
|
Cepas sensibles a meticilina (SASM)
|
Cloxacilina iv. 2-3 g 4 × d
|
Opciones:
– penicilinas con inhibidor de β-lactamasa
– cefazolina iv. 1-2 g 3 × d
– cefuroxima iv. 0,75-1,5 g 3 × d
– clindamicina iv. 300-600 mg 2-4 × d (máx. 4,8 g/d)
|
|
|
Cepas resistentes a meticilina (SARM)
|
Opciones:
– vancomicina iv. 15-20 mg/kg (máx. 2 g) 2-3 × dg
– linezolid VO o iv. 600 mg 2 × d
|
Opciones:
– teicoplanina el 1.er día 3-6 mg/kg cada 12 h, luego 6 mg/kg cada 24 h ± rifampicina 600 mg 1 × d o 2 × d VO
– clindamicina (con sensibilidad confirmada)
– ceftarolina iv. 600 mg 2 × d
– telavancina iv. 10 mg/kg 1 × d
|
|
Bacterias anaerobias
|
Opciones:
– amoxicilina con ácido clavulánico iv. 1,2 g 3 × d
– ampicilina con sulbactam iv. 1,5-3 g 4 × d
|
Opciones:
– bencilpenicilina iv. 3-5 mill. UI 4 × d (o ceftriaxona iv. 1-2 g 1 × d o cefotaxima iv. 1-2 g 3 × d) + metronidazol iv. 500 mg 4 × d
– clindamicina iv. 600 mg 3 × d
|
|
Klebsiella pneumoniae y otros bacilos intestinales gramnegativos (E. coli, Proteus spp.)
|
Opciones:
– cefuroxima iv. 1,5 g 3 × d
– cefotaxima iv. 1-2 g 3 × d
– ceftriaxona iv. 2 g 1 × d
|
Opciones:
– ciprofloxacina iv. 400 mg 2 × d
– imipenemh 500 mg con cilastatina 500 mg iv. 4 × d
– meropenemh iv. 1 g 3 × d
– β-lactámico con inhibidor de β-lactamasa
– añadir aminoglucósido en personas graves o inmunodeprimidas
|
|
Acinetobacter baumannii
|
Aminoglucósido + penicilina activa frente a Pseudomonas o carbapenem (dosificación como en infecciones por Pseudomonas)
|
|
|
Pseudomonas aeruginosa
|
Opciones:
– ceftazidima iv. 2 g 3 × d + aminoglucósidoi
– cefepima + aminoglucósido
– cefoperazona + aminoglucósido
|
Opciones:
– ciprofloxacina iv. 400 mg 2 × d o piperacilina iv. 4 g 3 × d + aminoglucósidoi
– aztreonam o carbapenemh iv. (imipenem 500 mg con cilastatina 500 mg 4 × d o meropenem iv. 1 g 3 × d) + ciprofloxacina como más arriba
– colistinak
– polimixina Bk
|
|
Legionella pneumophila
|
Fluoroquinolonaf:
levofloxacina iv. o VO 500 mg 1-2 × dj
ciprofloxacina iv. 400 mg 2 × d o VO 500 g 2 × d
ofloxacina VO 400 mg 2 × d
moxifloxacina VO 400 mg 1 × d
|
Opciones:
– macrólidob
– doxiciclina VO o iv., dosis inicial 200 mg, a continuación 100 mg 1 × d (2 × d en infecciones más graves)
|
|
a A partir de las guías BTS 2009 ERS/ESCMID 2011, modificado. Tener en cuenta la farmacosensibilidad local de los microorganismos.
b Azitromicina 500 mg 1 × d, claritromicina 500 mg 2 × d o eritromicina 500 mg 4 × d.
c Según las guías ERS/ESCMID 2011, con MIC ≤8 mg/l, es eficaz la dosis de 2 g cada 6 h iv. Dosis de bencilpenicilina recomendadas conforme a las guías EUCAST dependiendo de MIC:
1) ≤0,5 µg/ml: 1,2 g (2 mill. UI) 4 × d;
2) ≤1,0 µg/ml: 2,4 g (4 mill. UI) 4 × d o 1,2 g 6 × d;
3) ≤2 µg/ml: 2,4 g 6 × d.
d Según las guías ERS/ESCMID 2011 cuando MIC ≤8 mg/l, es eficaz la dosis de 2 g cada 6 h iv.
e Opciones cuando MIC para penicilina >8 mg/l.
f Según las guías ERS/ESCMID 2011: levofloxacina o moxifloxacina.
g En infecciones graves, obesidad significativa y en enfermos con insuficiencia renal, hay que vigilar la concentración del fármaco en suero, que debería ser de 15-20 µg/ml antes de la administración de la 4.ª o 5.ª dosis; en infecciones graves se puede considerar el inicio del tratamiento con una sola dosis de carga de 20-30 mg/kg.
h Dosis de carbapenemas en infecciones muy graves: imipenem 1 g con cilastatina 1 g 3-4 × d en infusiones que duran 40-60 min (la dosis máx. de imipenem es de 4 g/d o 50 mg/kg/d; elegir la dosis menor), meropenem iv. 2 g 3 × d (en las guías ERS/ESCMID 2011 se prefiere el meropenem en infusiones que duran 3 h).
i Está indicada la vigilancia de la concentración del fármaco en sangre.
j Cuando el aclaramiento de creatinina es >50 ml/min; en la insuficiencia renal dosis disminuida.
k Se utilizan las polimixinas (habitualmente en combinación con otros antibióticos) en el tratamiento de infecciones por cepas resistentes a los antibióticos de otros grupos.
|
 Español
Español
 English
English
 українська
українська







