Recomendaciones e indicaciones
1. Se recomienda la ecografía Doppler como prueba preliminar en el diagnóstico de la trombosis de la vena porta. La tomografía computarizada (TC) o la resonancia magnética nuclear (RMN) con contraste se recomiendan para evaluar la afectación de las venas mesentéricas y descartar el trombo (infiltración) neoplásico en los pacientes con cirrosis hepática y trombosis reciente de la vena porta y/o la vena mesentérica.1 [D/MB]2. Todos los pacientes con trombosis de la vena porta reciente y sospecha de isquemia intestinal deben acudir inmediatamente a consultas con un cirujano, un hematólogo, un especialista en radiología intervencionista y un especialista en terapia intensiva. Es imprescindible implementar un tratamiento anticoagulante, y en caso de isquemia intestinal aguda, tratamiento quirúrgico.2
Comentario
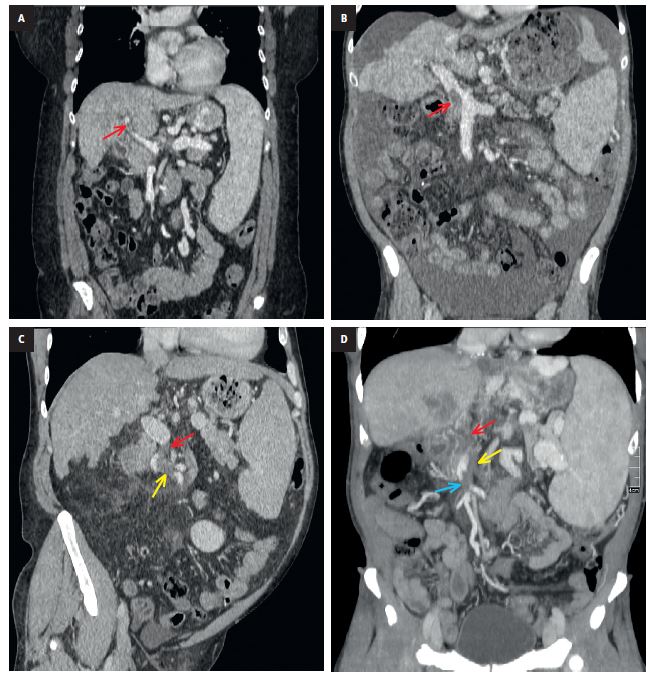
El dolor abdominal, por lo general localizado en el epigastrio, es el síntoma más frecuente de la trombosis aguda (reciente) del sistema portal. Otros síntomas menos frecuentes son náuseas, vómitos, aumento de la temperatura corporal, pérdida de apetito e ictericia. La fiebre, la ascitis, el dolor abdominal durante la palpación, la leucocitosis y el aumento de concentración de lactatos en suero indican isquemia intestinal secundaria a trombosis de la vena porta. La prueba de diagnóstico de elección es la ecografía Doppler, puesto que es menos costosa, su disponibilidad es mayor y no expone a radiación ionizante. Además, permite visualizar masas hiperecogénicas, la dilatación vascular y la ralentización del flujo sanguíneo en la vena porta. La TC permite valorar la afectación por trombo de las venas mesentéricas difíciles de ver en la ecografía. La arterialización de las masas en la luz vascular apunta a su carácter neoplásico (carcinoma hepatocelular).
| Tabla 1. Clasificación de la trombosis del sistema portal de Yerdel y cols.3 | |||
|---|---|---|---|
| Grado | Vena porta (% de afectación de la luz vascular) | Vena mesentérica superior, segmento proximal | Vena mesentérica superior,segmento distal |
| I | <50% | Trombo pequeño o sin trombo | Sin trombo |
| II | >50% | Trombo pequeño o sin trombo | Sin trombo |
| III | 100% | Obstrucción total de la luz vascular | Sin trombo |
| IV | 100% | Obstrucción total de la luz vascular | Obstrucción total de la luz vascular |
| Tabla 2. Factores de riesgo de la trombosis de la vena porta o la vena mesentérica1 | |
|---|---|
| Estado de hipercoagulabilidad | Neoplasia de un órgano de la cavidad abdominal Neoplasia mieloproliferativa Hemoglobinuria paroxística nocturna Otras trombofilias, p. ej. déficit de proteína C, déficit de proteína S, síndrome antifosfolipídico, homocisteinemia Embarazo Anticonceptivos orales hormonales |
| Daño de las venas del sistema portal | Traumatismo de la cavidad abdominal Inflamación en la cavidad abdominal, p. ej. pancreatitis aguda, enfermedades inflamatorias intestinales, colecistitis, diverticulitis, apendicitis Cirugía en la cavidad abdominal (colecistectomía, apendicectomía, colectomía, TIPS) |
| Flujo sanguíneo ralentizado | Cirrosis hepática Insuficiencia cardíaca congestiva |
Bibliografía:
1. Simonetto D.A., Singal A.K., Garcia-Tsao G. y cols., ACG Clinical Guideline: Disorders of the hepatic and mesenteric circulation, Am. J. Gastroenterol., 2020; 115: 18-402. Northup P.G., Garcia-Pagan J.C., Garcia-Tsao G. y cols., Vascular liver disorders, portal vein thrombosis, and procedural bleeding in patients with liver disease: 2020 practice guidance by the American Association for the Study of Liver Diseases, Hepatology, 2021; 73: 366-413
3. Yerdel M.A., Gunson B., Mirza D. y cols., Portal vein thrombosis in adults undergoing liver transplantation: risk factors, screening, management, and outcome, Transplantation, 2000; 69: 1873-1881
4. Plessier A., Darwish-Murad S., Hernandez-Guerra M. y cols., Acute portal vein thrombosis unrelated to cirrhosis: a prospective multicenter follow-up study, Hepatology, 2010; 51: 210-218
5. de Franchis R., Baveno V.I.F., Expanding consensus in portal hypertension: report of the Baveno VI Consensus Workshop: stratifying risk and individualizing care for portal hypertension, J. Hepatol., 2015; 63: 743-752
6. Hollingshead M., Burke C.T., Mauro M.A. y cols., Transcatheter thrombolytic therapy for acute mesenteric and portal vein thrombosis, J. Vasc. Interv. Radiol., 2005; 16: 651-661
7. Riva N., Ageno W., Poli D. y cols., Safety of vitamin K antagonist treatment for splanchnic vein thrombosis: a multicenter cohort study, J. Thromb. Haemost., 2015; 13: 1019-1027
8. European Association for the Study of the Liver, EASL Clinical Practice Guidelines: Vascular diseases of the liver, J. Hepatol., 2016; 64: 179-202
9. Nery F., Valadares D., Morais S. y cols., Efficacy and safety of direct-acting oral anticoagulants use in acute portal vein thrombosis unrelated to cirrhosis, Gastroenterol.Res., 2017; 10: 141-143
10. Naymagon L., Tremblay D., Zubizarreta N. y cols., The efficacy and safety of direct oral anticoagulants in noncirrhotic portal vein thrombosis, Blood Adv., 2020; 4: 655-666
11. Hamulyak E.N., Daams J.G., Leebeek F.W.G. y cols., A systematic review of antithrombotic treatment of venous thromboembolism in patients with myeloproliferative neoplasms, Blood Adv., 2021; 5: 113-121
12. Di Nisio M., Valeriani E., Riva N. y cols., Anticoagulant therapy for splanchnic vein thrombosis: ISTH SSC Subcommittee Control of Anticoagulation, J. Thromb. Haemost., 2020; 18: 1562-1568
13. Undas A., Zawilska K., Inhibitory czynnika Xa (fondaparynuks, rywaroksaban, apiksaban, edoksaban), https://www.mp.pl/interna/chapter/B16.II.2.34.2 (acceso: 6.01.2022)
14. Nery F., Chevret S., Condat B. y cols., Causes and consequences of portal vein thrombosis in 1,243 patients with cirrhosis: results of a longitudinal study, Hepatology, 2015; 61: 660-667
15. Bianchini M., Cavani G., Bonaccorso A. y cols., Low molecular weight heparin does not increase bleeding and mortality post-endoscopic variceal band ligation in cirrhotic patients, Liver Int., 2018; 38: 1253-1262
16. Kuetting D., Wolter K., Luetkens J. y cols., AngioJet-assisted transvenous-transhepatic mechanical thrombectomy in the portal vein., Pol. J. Radiol., 2018; 83: e536-e44
17. Salem R., Vouche M., Baker T. y cols., Pretransplant portal vein recanalization-transjugular intrahepatic portosystemic shunt in patients with complete obliterative portal vein thrombosis, Transplantation, 2015; 99: 2347-2355
18. Qi X., Guo X., Yoshida E.M. y cols., Transient portal vein thrombosis in liver cirrhosis, BMC Med., 2018; 16: 83
19. Senzolo M., Sartori M.S., Rossetto V. y cols., Prospective evaluation of anticoagulation and transjugular intrahepatic portosystemic shunt for the management of portal vein thrombosis in cirrhosis, Liver Int., 2012; 32: 919-927
20. Northup P., Reutemann B., Management of coagulation and anticoagulation in liver transplantation candidates, Liver Transpl., 2018; 24: 1119-1132
21. Loffredo L., Pastori D., Farcomeni A., Violi F., Effects of anticoagulants in patients with cirrhosis and portal vein thrombosis: a systematic review and meta-analysis, Gastroenterology, 2017; 153: 480-487
22. Lee H.F., Chan Y.H., Chang S.H. y cols., Effectiveness and safety of non-vitamin K antagonist oral anticoagulant and warfarin in cirrhotic patients with nonvalvular atrial fibrillation, J. Am. Heart Assoc,. 2019; 8: e011 112
23. De Gottardi A., Trebicka J., Klinger C. y cols., Antithrombotic treatment with direct-acting oral anticoagulants in patients with splanchnic vein thrombosis and cirrhosis, Liver Int., 2017; 37: 694-699
24. Intagliata N.M., Maitland H., Pellitier S., Caldwell S.H., Reversal of direct oral anticoagulants for liver transplantation in cirrhosis: A step forward, Liver Transpl., 2017; 23: 396-397
25. Faraoun S.A., Boudjella Mel A., Debzi N. y cols., Budd-Chiari syndrome: a prospective analysis of hepatic vein obstruction on ultrasonography, multidetector-row computed tomography and MR imaging, Abdom. Imaging., 2015; 40: 1500-1509
26. Van Wettere M., Purcell Y., Bruno O. y cols., Low specificity of washout to diagnose hepatocellular carcinoma in nodules showing arterial hyperenhancement in patients with Budd-Chiari syndrome, J. Hepatol., 2019; 70: 1123-1132
27. Ren W., Qi X., Yang Z. y cols., Prevalence and risk factors of hepatocellular carcinoma in Budd-Chiari syndrome: a systematic review, Eur. J. Gastroenterol. Hepatol., 2013;
28. Moucari R., Rautou P.E., Cazals-Hatem D. y cols., Hepatocellular carcinoma in Budd-Chiari syndrome: characteristics and risk factors, Gut, 2008; 57: 828835
29. Pieri L., Paoli C., Arena U. y cols., Safety and efficacy of ruxolitinib in splanchnic vein thrombosis associated with myeloproliferative neoplasms, Am. J. Hematol., 2017; 92: 187-195
30. Sharma S., Texeira A., Texeira P. y cols., Pharmacological thrombolysis in Budd Chiari syndrome: a single centre experience and review of the literature, J. Hepatol., 2004; 40: 172-180
31. Perello A., Garcia-Paga n J.C., Gilabert R. y cols., TIPS is a useful long-term derivative therapy for patients with Budd-Chiari syndrome uncontrolled by medical therapy, Hepatology, 2002; 35: 132-139c
32. Oldakowska-Jedynak U., Ziarkiewicz M., Ziarkiewicz-Wroblewska B. y cols., Myeloproliferative neoplasms and recurrent thrombotic events in patients undergoing liver transplantation for Budd-Chiari syndrome: a single-center experience, Ann.Transplant., 2014; 19: 591–597
Volver al artículo principal: Guías ACG y AASLD: manejo de la trombosis de la vena porta y de las venas hepáticas
 Español
Español
 English
English
 українська
українська