Indicaciones
Insuficiencia respiratoria aguda o crónica. En la mayoría de los estados agudos, está indicada con la SpO2 (SaO2) <90-92 % (excepción →más adelante). El tratamiento domiciliario con oxígeno se usa en la insuficiencia respiratoria crónica avanzada (causada con mayor frecuencia por EPOC, menos frecuentemente por bronquiectasias, fibrosis pulmonar idiopática o fibrosis quística); a veces también en pacientes con insuficiencia cardíaca crónica o con enfermedad neoplásica avanzada. Indicaciones para la oxigenoterapia domiciliaria en la EPOC, que se han extendido a otras enfermedades pulmonares crónicas: PaO2 <55 mm Hg o PaO2 55-59 mm Hg con presencia de hipertensión pulmonar, hematocrito >55 %, cor pulmonale crónico o trastornos del ritmo cardiaco.
Contraindicaciones
Una creciente retención del CO2 en pacientes con insuficiencia respiratoria crónica (con mayor frecuencia a causa de EPOC) no es una contraindicación para la oxigenoterapia si se presenta hipoxemia, pero debe incitar a disminuir el contenido de oxígeno presente en la mezcla respiratoria o a iniciar la ventilación pulmonar mecánica.
Complicaciones
1. Efectos indeseables del oxígeno: el uso del oxígeno en altas concentraciones (>50 %, es decir, FiO2 >0,5) puede ser perjudicial, dependiendo de su concentración y del tiempo de exposición. Se distinguen 4 grupos de síntomas: traqueítis y bronquitis (cambios inflamatorios con sequedad excesiva de la mucosa y deterioro del aclaramiento mucociliar), atelectasia por absorción (durante la respiración de oxígeno al 100 % se elimina el nitrógeno, necesario para prevenir el colapso alveolar, siendo sustituido por el oxígeno que se absorbe rápidamente), lesión pulmonar aguda (indistinguible de las lesiones patológicas que requieren la administración de oxígeno a elevadas concentraciones), displasia broncopulmonar (en neonatos).
2. Consecuencias de respirar con mezcla seca y fría de gases (sobre todo por tiempo prolongado): sequedad y ulceración de las mucosas, deterioro del transporte mucociliar, retención de secreciones y aumento de su densidad (que conducen a la formación de focos de atelectasia), broncoespasmo, infecciones.
Equipo
1. Fuentes de oxígeno:
1) hospitalarias (fuentes de oxígeno limpio): oxígeno líquido o gaseoso (comprimido en balones de distinta capacidad), suministrado al paciente a través de una instalación central o con un balón portátil
2) extrahospitalarias (oxigenoterapia domiciliaria): concentradores que aumentan la concentración del oxígeno obtenido del aire ambiental (hasta un 85-95 %) y lo suministran de forma continua al paciente; con menor frecuencia se emplea (en oxigenoterapia casera) el oxígeno comprimido en botellas o el oxígeno líquido en botellas.
PERSPECTIVA CHILENA
En Chile pueden usarse concentradores de oxígeno en pacientes con movilidad limitada <15 m y el oxígeno comprimido en cilindros. El oxígeno líquido está disponible en reservorios conocidos como depósitos, termo o estanques, que permiten el llenado de una mochila portátil para facilitar el desplazamiento del paciente.
2. Medidor de flujo con posibilidad de regulación: conectado a la instalación central de oxígeno, al balón o al concentrador, permite obtener la concentración deseada de oxígeno en la mezcla de gases aspirados.
3. Máscaras y cánulas de oxígeno:
1) Cánula nasal estándar (llamada gafas nasales, bigoteras o nariceras →fig. 27.21-1), colocada en ambas fosas nasales: usada con mayor frecuencia; el flujo de oxígeno 1 l/min proporciona una concentración de oxígeno en la mezcla respiratoria del 24 % y el aumento del flujo en cada siguiente 1 l/min (en el rango de 2-8 l/min) aumenta la concentración en un 4 % (la relación entre el flujo y la concentración de O2 no es totalmente lineal y puede ser modificada por el tipo de respiración, el volumen corriente y si el paciente respira por la boca o por la nariz); a veces (principalmente durante la broncoscopia) se utiliza la cánula colocada en una sola fosa nasal.
2) Máscaras sencillas (comunes; →fig. 27.21-2): proporcionan la concentración de oxígeno en la mezcla respiratoria de un 40-60 % con un flujo de 5-8 l/min (5-6 l/min – 40 %, 6-7 l/min – 50 %, 7-8 l/min – 60 %). Debido a la alta concentración de oxígeno y una precisión insuficiente, no están indicadas en enfermos con riesgo de hipercapnia (→más adelante). No utilizar el flujo <5 l/min por el riesgo de reinhalación del CO2 espirado y de aumento de la resistencia durante la inspiración.
3) Máscaras con válvulas de Venturi (→fig. 27.21-3): la administración de oxígeno puro (100 %) con una determinada velocidad de flujo (según la instrucción del fabricante) permite obtener la concentración de este gas definida con precisión (24 %, 25 %, 28 %, 35 %, 40 %, 50 % y 60 %) en la mezcla respiratoria; recomendadas en pacientes con EPOC y en otros pacientes con riesgo de hipercapnia →más adelante. Si la frecuencia respiratoria es >30/min, aumentar el flujo de oxígeno en un 50 % del recomendado en la instrucción del fabricante.
4) Máscaras con retorno parcial (con bolsa de reservorio sin válvula que impide la mezcla de aire con oxígeno puro): alta concentración de oxígeno (7 l/min – 70 %, 8 l/min – 80 %, 9-15 l/min – 90-95 %).
5) Máscaras sin retorno (→fig. 27.21-4): con bolsa de reservorio y válvula que impide la mezcla de aire con oxígeno puro; permiten obtener altas concentraciones de oxígeno (como aquellas con retorno parcial).
6) Bolsas autoexpandibles con máscara facial: por lo general sirven para la ventilación asistida manual y para la ventilación de reemplazo, pueden estar equipadas con válvula y bolsa de reservorio, permiten alta concentración de oxígeno (igual que las máscaras con retorno parcial) con un gran flujo de oxígeno (y con la bolsa autoexpandible llena [y el reservorio, si forma parte del equipo]).
7) Cánula nasal de alto flujo de gases (hasta 80 l/min: oxigenoterapia nasal de alto flujo, ONAF) →fig. 27.21-5): permite administrar una concentración de oxígeno aproximadamente del 100 % en la mezcla de los gases espirados (si se administra oxígeno puro). A diferencia del oxígeno seco y frío aportado por los sistemas de oxígeno convencionales, en las cánulas de alto flujo el oxígeno administrado es acondicionado, humidificado y calentado a valores ajustables de 31-37 ºC. Produce una presión positiva leve en las vías respiratorias altas (más alta que la presión atmosférica) y puede ayudar a eliminar el CO2, facilitar el mantenimiento de la permeabilidad de las vías respiratorias y el reclutamiento alveolar, así como reducir el trabajo de los músculos respiratorios. Requiere un equipo especial, pero suele ser mejor tolerada por los enfermos que la ventilación mecánica no invasiva y la oxigenoterapia con máscara. La ONAF puede ser aplicada a personas con insuficiencia respiratoria (sin hipercapnia, si se administra el oxígeno en alta concentración) y también en la atención posoperatoria y durante la broncoscopia. Se recomienda la ONAF en enfermos con insuficiencia respiratoria hipoxémica (de novo, que no requiere intubación inmediata, también en casos de COVID-19). También se sugiere utilizar este método tras la extubación de los pacientes sometidos a ventilación mecánica durante ≥24 h, con cualquier factor de riesgo elevado de reintubación, así como después de cirugías torácicas y cardíacas en pacientes con obesidad y/u otros factores de riesgo elevado de insuficiencia respiratoria posquirúrgica. Principios de uso de ONAF →más adelante.
4. Tubos de conexión: en caso de concentradores estacionados en casa se permite una longitud de 12 m.
5. Humidificadores y calentadores de gases respiratorios: beneficiosos en caso de respirar a través de una máscara con elevadas concentraciones de oxígeno; los más eficaces son los sistemas activos de humidificación. Una higiene inadecuada durante la humidificación puede causar infecciones respiratorias. No utilizar equipos humidificadores que emplean una capa de líquido procedente de una cánula colocada en el fondo del depósito de líquido (eficacia no demostrada, riesgo de infección).
6. Oxigenoterapia hiperbárica (OHB): consiste en el uso —en pacientes con ventilación espontánea o asistida— de oxígeno puro (al 100 %) en una cámara hiperbárica a una presión de 2-3 atm. Indicaciones básicas:
1) enfermedad por descompresión grave o embolia arterial gaseosa
2) intoxicación por monóxido de carbono (con HbCO >40 %, pérdida de conciencia, y en embarazadas: con HbCO >20 % o signos de sufrimiento fetal); los estudios acerca de la eficacia son contradictorios; su uso es controvertido.
Contraindicaciones:
1) absolutas: neumotórax no tratado
2) relativas: bulas enfisematosas, EPOC (en estadio grave), infecciones del tracto respiratorio superior o de los senos paranasales, traumatismo reciente de oído o intervención en el oído medio, fiebre, claustrofobia.
Normas
No utilizar oxígeno en cercanía del fuego.
1. Insuficiencia respiratoria aguda:
1) Vigilar los resultados de la oxigenoterapia: pulsioximetría →Pulsioximetría, gasometría de sangre →tabla 20.2-1 y →Extracción de sangre para gasometría, a veces capnometría.
2) Tratar de lograr una SpO2 de ~94 % (según las guías de la BTS [2017] 94-98 %, según las guías del grupo MAGIC [2018] 90-94 %) en todos los enfermos, a excepción de los pacientes con:
a) hipercapnia o riesgo elevado de desarrollarla (es decir, los pacientes con EPOC, enfermedades neuromusculares con debilidad de los músculos respiratorios, bronquiectasias, fibrosis quística, con deformidad significativa del tórax, obesidad mórbida o tras sobredosis de opioides, benzodiazepinas u otros fármacos que inhiben el centro respiratorio), en los cuales la SpO2 objetivo es de un 88-92 % (según las guías de la BTS, en caso de shock, sepsis, reacción anafiláctica, traumatismo grave o casi ahogamiento siempre se debe intentar conseguir una SpO2 de un 94-98 % a la espera de los resultados de gasometría)
b) neumotórax, intoxicación por monóxido de carbono (se debe aplicar la oxigenoterapia a la máxima concentración disponible), crisis en el transcurso de anemia drepanocítica o cefalea en racimos, en los que se intenta conseguir la SpO2 del 100 %.
3) Está indicado utilizar oxígeno a la máxima concentración disponible durante la reanimación cardiopulmonar (→Paro cardíaco súbito). Además de los estados arriba mencionados, en los cuales se intenta conseguir una SpO2 del 100 %, se debe administrar oxígeno con el flujo de 15 l/min a través de una máscara con reservorio durante una crisis epiléptica (hasta obtener el resultado de la pulsioximetría) y tras un traumatismo craneal grave (hasta conseguir resultados satisfactorios de la gasometría o hasta intubar al paciente). En la mayoría de los demás casos, la SpO2 objetivo no debe superar el 96 %, puesto que los valores superiores aumentan el riesgo de muerte. En el infarto de miocardio y ACV recientes, la oxigenoterapia puede resultar perjudicial en enfermos con SpO2 ≥90 %.
4) Mantener la PaCO2 ≤60 mm Hg.
5) Recordar que el suministro de oxígeno a los tejidos depende de la PaO2 solo de manera indirecta. Los factores que influyen directamente son la concentración de hemoglobina, la saturación de oxígeno (SaO2), la perfusión sanguínea (gasto cardíaco y presión arterial media) y la capacidad de los tejidos de absorber oxígeno. Esto es especialmente importante en enfermedades que cursan con shock o anemia. Los parámetros que indican un adecuado suministro de oxígeno a los tejidos incluyen la concentración normal de lactato en la sangre y la saturación venosa central (SvO2) >70 % o saturación venosa mixta >75 %.
6) Debido a la toxicidad de la oxigenoterapia a elevadas concentraciones (>50 % = FiO2 >0,5; →más arriba), cuando es necesario administrarla, se usa por lo general en cortos períodos de tiempo (desde algunas horas hasta algunos días) y la falta de mejoría del estado clínico con frecuencia es indicación para la ventilación mecánica de los pulmones.
7) Considerar la ONAF, especialmente si es necesario administrar oxígeno a elevadas concentraciones. Antes de iniciar la ONAF, informar al enfermo sobre este método y seleccionar el tamaño adecuado de cánulas nasales. Durante la ONAF seleccionar:
a) el flujo de la mezcla respiratoria: del rango 10-80 l/min (inicialmente en general 25-40 l/min y aumentar gradualmente hasta el valor objetivo; mayores flujos aumentan la presión positiva en las vías respiratorias, pero en algunos dispositivos disminuyen la FiO2 si no se aumenta simultáneamente el flujo de oxígeno desde su fuente →más adelante)
b) el flujo de oxígeno desde su fuente hasta el dispositivo: la ONAF requiere el uso de reductores que permitan altos flujos de oxígeno (>15 l/min; el flujo de oxígeno desde su fuente no puede ser mayor al seleccionado en el dispositivo)
c) la concentración de oxígeno en la mezcla respiratoria (FiO2): puede no determinarse directamente, sino derivarse del flujo de oxígeno seleccionado y el flujo en el dispositivo (el aumento del flujo de oxígeno desde su fuente aumenta la FiO2, mientras que el aumento del flujo de la mezcla respiratoria en el dispositivo la disminuye [con el flujo constante de oxígeno desde su fuente]; en estos casos, la FiO2 de la mezcla respiratoria obtenida se registra en la pantalla del dispositivo)
d) la temperatura de la mezcla respiratoria (entre 31-37 °C): seleccionar el valor con el que el enfermo se sienta más cómodo.
Para vigilar la ONAF (no solo en enfermos con COVID-19) es útil el índice ROX = SpO2/FiO2/frecuencia respiratoria (p. ej. si la SpO2 es del 90 %, la FiO2 es de 0,5 y la frecuencia respiratoria, de 20/min, el valor ROX es de 9 ptos.). El valor ROX <4,88 a las 12 horas del comienzo de ONAF indica su ineficacia.
2. Agudización de la insuficiencia respiratoria crónica:
1) Debido a la posibilidad del estímulo respiratorio hipoxémico a consecuencia de la hipercapnia (sobre todo en enfermos con EPOC; otras causas más raras →más arriba), no utilizar oxígeno a altas concentraciones en pacientes con disnea hasta que no se verifique (rápidamente) la enfermedad pulmonar que padece.
2) Antes de iniciar la oxigenoterapia realizar una gasometría de la sangre arterial (opcionalmente de la sangre arterializada).
3) En pacientes con riesgo de hipercapnia intentar (por lo general) que la SpO2 sea de un 88-92 %. En caso de hipoxemia aislada el flujo de oxígeno a través de la cánula intranasal suele ser de 2 l/min (en caso de hipoxemia significativa aumentar el flujo de oxígeno, de preferencia usar la máscara de Venturi). En caso de hipercapnia utilizar flujos de oxígeno más bajos (0,5-1 l/min) a través de la cánula intranasal o utilizar la máscara de Venturi, asegurando la menor concentración posible de oxígeno (24 % o 25 %) en la mezcla respiratoria. Se puede tolerar una pequeña hipoxemia (PaO2 50-60 mm Hg), pero se debe evitar una PaO2 <40 mm Hg. En caso de que la PaO2 permanezca tan baja o de que aumente la hipercapnia, considerar la ventilación mecánica no invasiva o invasiva.
4) Vigilar con cuidado los efectos de la oxigenoterapia tomando en cuenta no solo la SpO2 (pulsioximetría →Pulsioximetría), sino también la PaCO2 y el pH (gasometría de la sangre arterial →tabla 20.2-1 y →Extracción de sangre para gasometría).
3. Oxigenoterapia domiciliaria:
1) tratar de obtener una PaO2 >60 mm Hg o SaO2 ≥90 %
2) indicar la administración de oxígeno ≥15 h/d, mejor durante todo el día
3) determinar individualmente el flujo de oxígeno en función de los resultados gasométricos, generalmente en ~2 l/min (0,5-3 l/min)
4) durante el sueño y el esfuerzo físico recomendar el aumento del flujo de oxígeno en 1 l/min.
TABLAS Y FIGURAS
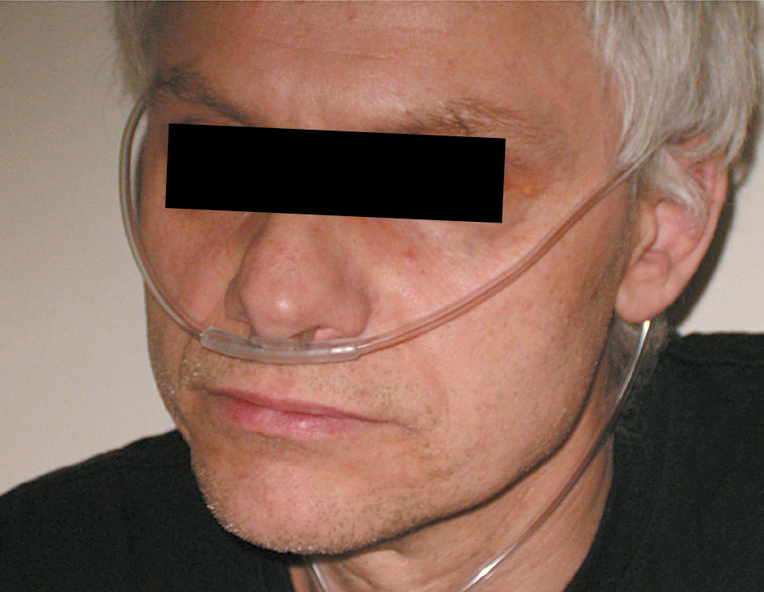
Fig. 27.21-1. Gafas nasales
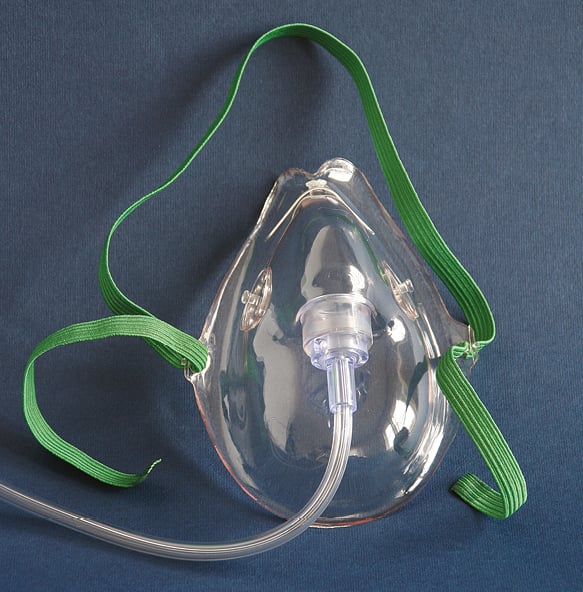
Fig. 27.21-2. Máscara sencilla
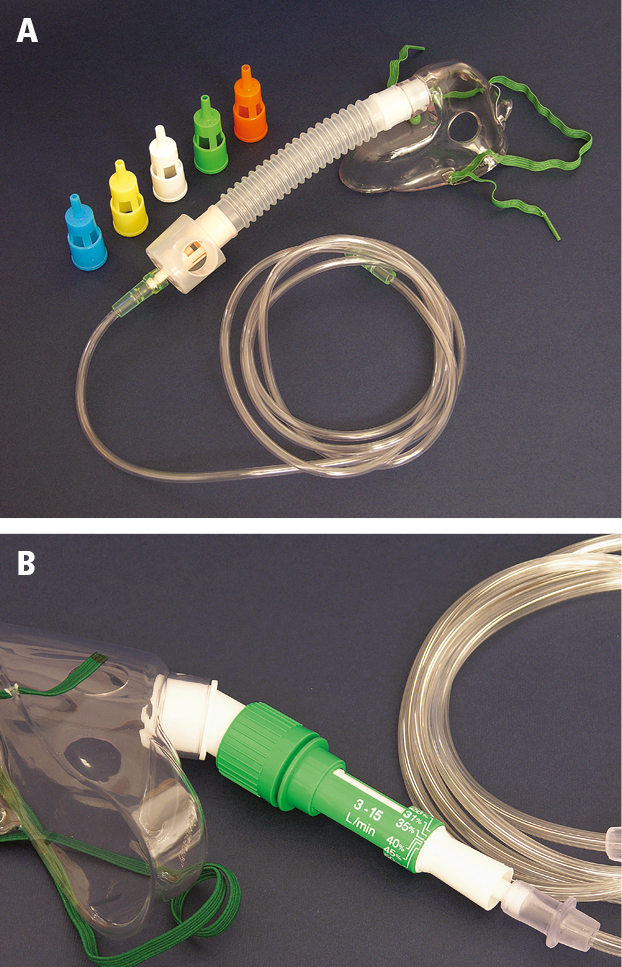
Fig. 27.21-3. Máscara con válvula de Venturi: reemplazable (A) y regulada (B)

Fig. 27.21-4. Máscara sin retorno
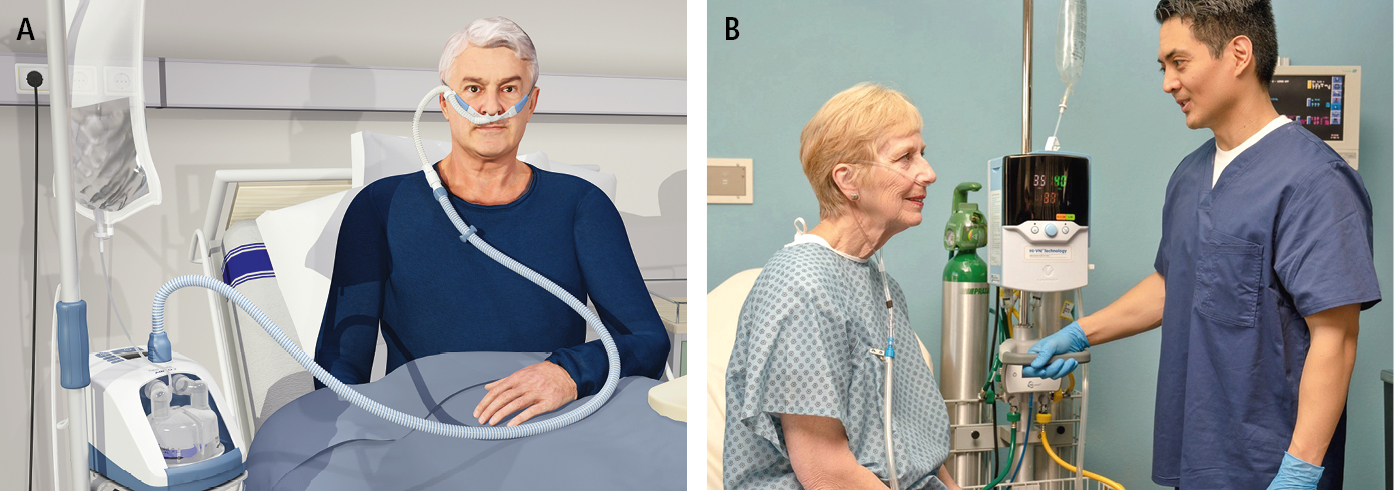
Fig. 27.21-5. Cánula nasal de alto flujo
Parámetros gasométricos en sangre arteriala
|
Símbolo y explicación |
Valor normal |
|
pH |
Logaritmo decimal negativo de la concentración de iones de hidrógeno |
7,35-7,45 |
|
PaCO2 |
Presión parcial de dióxido de carbono en sangre arterial |
35-45 mm Hg (4,65-6,00 kPa) |
|
[HCO3–]act |
Concentración actual de bicarbonato en el plasma |
21-27 mmol/l |
|
[HCO3–]est |
Concentración estándar de bicarbonato |
24 (21-25) mmol/l |
|
EB |
Exceso de bases en la sangre |
Desde −2,3 hasta +2,3 mEq/l |
|
PaO2 |
Presión parcial del oxígeno en sangre arterial |
75-100 mm Hgb (10,00-13,33 kPa) |
|
ctCO2 |
Contenido total del dióxido de carbono en el plasma |
22-28 mmol/l
47-60,5 % del volumen |
|
SaO2 |
Saturación de oxígeno de la hemoglobina en sangre arterial |
95-98 %b |
|
a Extraída sin contacto con el aire.
b Interpretando la PaO2 y la SaO2 siempre es necesario conocer la fracción de oxígeno del aire inspirado en valor decimal (FiO2). Se muestran los valores normales durante la respiración con aire atmosférico a nivel del mar (la concentración de oxígeno es del 20,9 %, lo que corresponde al FiO2 = 0,209). Durante la respiración con oxígeno al 100 % (FiO2 = 1,0) en una persona sana la PaO2 puede llegar a ~600 mm Hg y la SaO2 será del 100 %. |
 Español
Español
 English
English
 українська
українська









