Ми прагнемо й надалі безкоштовно надавати цей тип контенту. На жаль, коштів на це більше немає.
Без Вашої допомоги нам доведеться закрити проект до кінця 2024 року.
Зробіть пожертву
Скорочення: АВ — атріовентрикулярний, АГ — артеріальна гіпертензія, АМР — антагоністи мінералокортикоїдного рецептора, АПФ2 — ангіотензинперетворюючий фермент 2, БРА — блокатори рецептора ангіотензину, ВІТ — відділення інтенсивної терапії, ВМН — верхня межа норми, ВТЕ — венозна тромбоемболія, ГКС — гострі коронарні синдроми, ГРДС — гострий респіраторний дистрес-синдром, іАПФ — інгібітори ангіотензинперетворюючого фермента, ІКД — імплантований кардіовертер-дефібрилятор, КТ-ангіографія — комп'ютерна томографічна ангіографія, ЛДГ — лактатдегідрогеназа, ЛЗ — лікарський засіб, ЛШ — лівий шлуночок, НДШ — нижні дихальні шляхи, НМГ — низькомолекулярний гепарин, НОАК — нові оральні антикоагулянти не антагоністи вітаміну К, НПЗП — нестероїдні протизапальні препарати, НФГ — нефракціонований гепарин, НШТ — надшлуночкова тахікардія, РАС — ренін-ангіотензинова система, РСС — раптова серцева смерть, СН — серцева недостатність, СРБ — С-реактивний білок, СС — серцево-судинний, ССЗ — серцево-судинні захворювання, ССЗВ — синдром системної запальної відповіді, ТЕЛА — тромбоемболія легеневої артерії, ТТЕхоКГ — трансторакальна ехокардіографія, ФП — фібриляція передсердь, ФШ — фібриляція шлуночків, ЧСЕхоКГ — черезстравохідна ехокардіографія, ШВЛ — штучна вентиляція легень, ШТ —шлуночкова тахікардія, ALS (advanced life support) — елементи інтенсивної терапії з підтримки життєдіяльності, BLS (basic life support) — основи підтримки життя, COVID-19 (coronavirus disease) — захворювання, спричинене SARS-CoV-2, CrCl — кліренс креатиніну, cTn (cardiac troponin) — серцевий тропонін, ESC (European Society of Cardiology) — Європейське товариство кардіологів, HFpEF (heart failure with preserved ejection fraction) — серцева недостатність зі збереженою фракцією викиду лівого шлуночка, LQTS (long QT syndrome) — синдром подовженого інтервалу QT, NSTEMI (non-ST elevation myocardial infarction) — інфаркт міокарда без елевації сегмента ST, SARS-CoV-2 (severe acute respiratory syndrome coronavirus 2) — коронавірус тяжкого гострого респіраторного синдрому 2, STEMI (ST-elevation myocardial infarction) — інфаркт міокарда з елевацією сегмента ST, TdP — пірует-тахікардія, WPW (Wolff-Parkinson-White [syndrome]) — синдром Вольфа-Паркінсона-Уайта.
Пацієнти із COVID-19 часто звертаються у лікарню із задишкою (55–57 %), кашлем (76–79 %) та кровохарканням (8 %).1-3 Це також симптоми, характерні для ТЕЛА: задишка спостерігається у 50 %, кашель — 23 % та кровохаркання — 8 % випадків.4 Перехрест клінічної картини обох цих захворювань може призвести до гіподіагностики ТЕЛА. Якщо у пацієнта із COVID-19 спостерігається раптове погіршення вентиляції, тахікардія та гіпотензія, то під час диференційної діагностики необхідно врахувати тромбоемболічні ускладнення (Рамка 1).
Рамка 1
Гостра тромбоемболія легеневої артерії (ТЕЛА) та COVID-19 (відповідно до позиції ESC)21
• Слід зважити застосування антикоагулянтної терапії в стандартних профілактичних дозах у всіх хворих на COVID-19, які поступили в лікарню.
• Гостру ТЕЛА слід підозрювати у хворих на COVID-19 у разі несподіваних дихальних порушень, нової або нез'ясованої тахікардії, падіння артеріального тиску, не пов’язаного з тахіаритмією, гіповолемією або сепсисом, нових змін на ЕКГ, що свідчать про ТЕЛА, та суб'єктивних симптомів тромбозу глибоких вен (ТГВ) кінцівок.
• У разі підтвердження гострої ТЕЛА слід застосувати лікування відповідно до діючих клінічних настанов ESC.
• Слід пам’ятати про те, що пероральні антикоагулянти, які не є антагоністами вітаміну К (НОАК), можуть взаємодіяти з деякими ЛЗ, застосування яких досліджується при COVID-19, особливо з лопінавіром та ритонавіром; у таких випадках слід уникати НОАК. Не було зафіксовано жодних серйозної взаємодії між ЛЗ, застосування яких при COVID-19 досліджується, та гепаринами.
У цій ситуації рекомендується діяти за алгоритмом, який враховує клінічну ймовірність ТЕЛА перед проведенням тесту та визначення концентрації D-димеру. Підвищення концентрації D-димеру може бути вторинним до інфекції та запалення, що значно знижує специфічність результату. Більшість пацієнтів із COVID-19 мають концентрацію D-димеру <1000 нг/мл, у тому числі у 32–53 % пацієнтів результат знаходиться в межах норми.2,5, 22 Важливим аспектом є використання візуалізаційних методів діагностики: компресійної ультрасонографії вен нижніх кінцівок, ехокардіографії та КТ-ангіографії легеневих артерій.
Якщо у пацієнта виконано КТ грудної клітки, проте зміни в легенях не пояснюють дихальну недостатність, слід розглянути питання про проведення КТ-ангіографії легеневих артерій.
Лікування ТЕЛА повинно проводитись відповідно до клінічних настанов ESC на основі оцінки ризику. У пацієнтів із шоком слід негайно застосувати реперфузійну терапію, тоді як гемодинамічно стабільних пацієнтів можна лікувати нефракціонованим (НФГ) або низькомолекулярним (НМГ) гепарином чи пероральним антикоагулянтним не антагоністом вітаміну K (НОАК) з урахуванням можливості прийому пероральних ЛЗ, оцінки функції нирок та ризику швидкого погіршення функціонального стану серцево-судинної та дихальної системи.
Слід підкреслити те, що деякі ЛЗ, що застосовуються для лікування інфекції, спричиненої SARS-CoV-2, інгібують цитохром P450 3A4 (лопінавір та ритонавір), що може посилити дію НОАК та підвищити ризик кровотечі. Хлорохін, в свою чергу, інгібує Р-глікопротеїн, що може знизити концентрацію НОАК, і цей ефект може довго зберігатися (через тривалий період напіввиведення ЛЗ). Застосування антагоністів вітаміну К (АВК) не рекомендується через необхідність контролю МНВ, за винятком пацієнтів із імплантованим механічним клапаном серця або антифосфоліпідним синдромом.6 З огляду на попередні повідомлення про виникнення ТЕЛА у пацієнтів із COVID-19, генералізоване запалення та іммобілізацією, профілактичну антикоагуляцію слід застосовувати у кожного пацієнта, госпіталізованого у зв'язку з COVID-19, водночас враховуючи ризик геморагічних ускладнень.7,8
В кінці лютого та на початку березня цього року, в період пересування хвилі захворюваності на COVID-19 з Китаю та інших азіатських країн на європейський континент, з’явилися тривожні повідомлення, що дозволяли припустити існування зв’язку між інфекцією, спричиненою SARS-CoV-2, та артеріальною гіпертензією (АГ), а також вплив на цю інфекцію ЛЗ, які застосовуються при АГ– іАПФ та блокаторів AT1-рецептора до ангіотензину II (т. зв. БРА, сартанів).9 Були зроблені спроби довести, що АГ може сама по собі підвищити ризик розвитку COVID-19 і погіршити її клінічний перебіг. Також були припущення, що проникнення вірусу SARS-CoV-2 в клітини може бути пов'язане з дією блокаторів РАС. Ці повсюдно поширювані гіпотези сприяли тому, що не лише хворі на АГ, а й лікарі, які доглядали за такими пацієнтами, необґрунтовано відміняли блокатори РАС, які до цього часу застосовувались.9
Огляд раніше опублікованих досліджень, що оцінюють зв’язок між АГ та інфекціями нижніх дихальних шляхів (НДШ), проведених переважно у Фінляндії та Іспанії, не дає підстав вважати, що АГ збільшує ризик розвитку або погіршує клінічний перебіг інфекцій НДШ, особливо бактеріальної або вірусної пневмонії.10,11 Однак такий зв'язок був задокументований у випадку старшого віку, супутніх захворювань серця та цукрового діабету.11 Є достовірні наукові дані, що вказують на те, що АГ — особливо у пацієнтів літнього віку, із більш тяжким перебігом та супровідними органними ускладненнями — є важливим фактором ризику виникнення СС ускладнень та смерті в ході інфекцій НДШ при ранньому та тривалому спостереженні.12,13 Як уже згадувалося, SARS-CoV-2 проникає в клітини після попереднього з'єднання з АПФ2, який відповідає за трансформацію ангіотензину II в ангіотензин 1–7 з гіпотензивною дією (рамка 2, рис.). В експериментальних умовах показано, що ангіотензин 1–7 має судинорозширювальну, протизапальну, антиоксидантну та цитопротекторну дію, зокрема на клітини легеневої тканини. Цікаво, що іАПФ та БРА збільшують експресію АПФ2, що теоретично може позитивно впливати на легеневу тканину під час інфекції COVID-19 (протягом активного періоду хвороби).9
Рамка 2
Ренін-ангіотензинова система та COVID-19 — застосування іАПФ та БРА
1. Ангіотензинперетворюючий фермент 2-го типу (АПФ2) є рецептором для нового вірусу SARS-CoV-2, який викликає COVID-19.
2. Вплив блокаторів ренін-ангіотензинової системи (РАС) на інфективність SARS-CoV-2 шляхом збільшення експресії АПФ2 досі не отримав наукового підтвердження.
3. У контексті пандемії COVID-19, в аспекті актуальних наукових даних, слід продовжувати застосування блокаторів РАС — інгібіторів ангіотензинперетворюючого фермента (іАПФ) та блокаторів рецептора ангіотензину (БРА) у пацієнтів в стабільному стані, відповідно до діючих клінічних настанов наукових товариств. Наукові товариства, зокрема European Society of Hypertension і Deutsche Hochdruckliga, підтримують цю рекомендацію.
(натисність на рисунок, щоб збільшити)
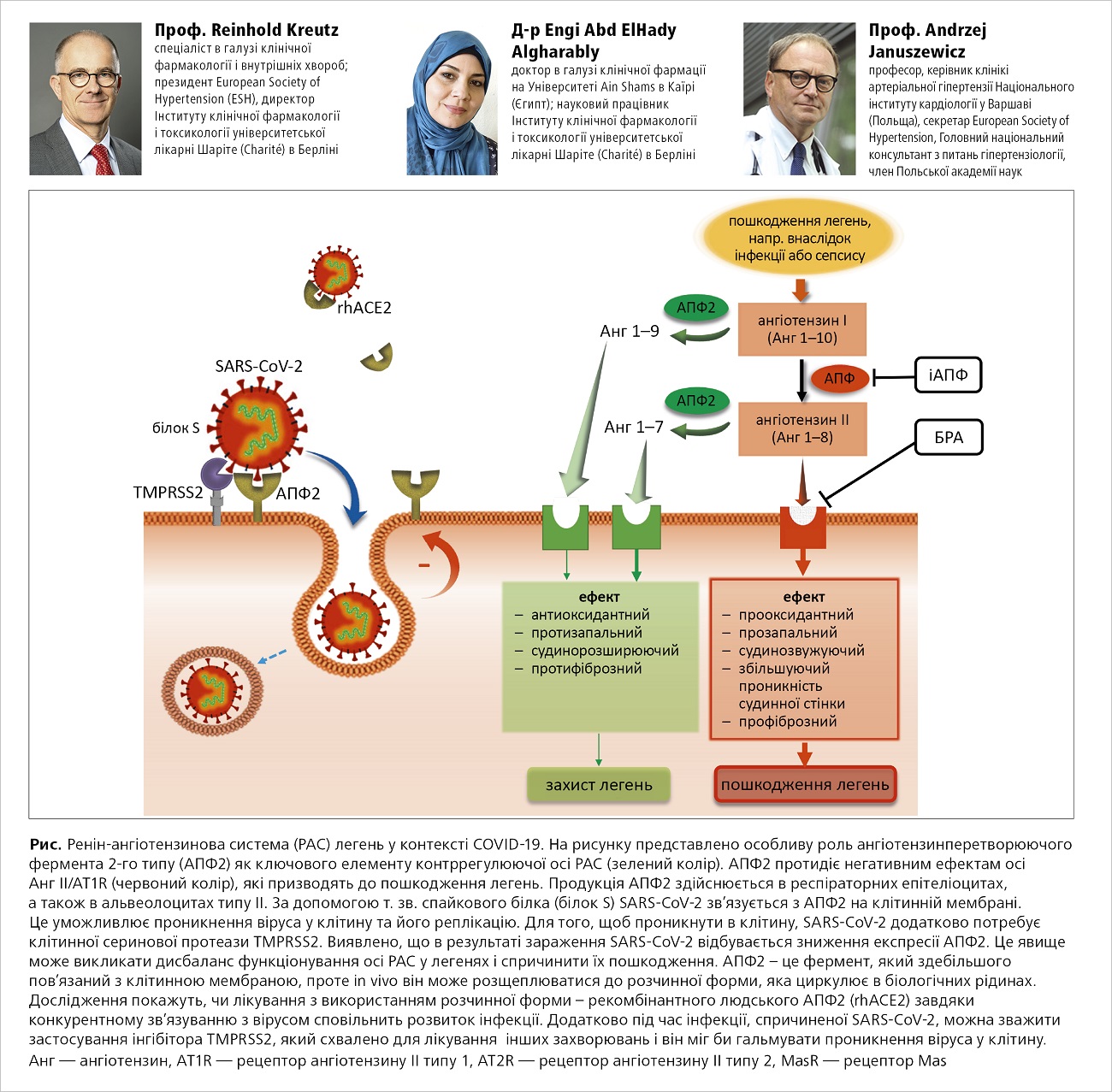
Рисунок 1. Ренін-ангіотензинова система (РАС) легень у контексті COVID-19
У великих клінічних дослідженнях було підтверджено, що у пацієнтів з АГ блокатори РАС — іАПФ i БРА — знижують ризик виникнення СС ускладнень у разі інфекції НДШ (бактеріальної чи вірусної) як в активний період хвороби, так і при тривалому спостереженні.14,15
Відповідно до позиції European Society of Hypertension (ESH) актуальні доступні дані не обґрунтовують іншого застосування блокаторів РАС у хворих на COVID-19. У пацієнтів в стабільному стані, зі слабко або помірно вираженими симптомами, а також у пацієнтів, які мають ризик розвитку COVID-19, лікування АГ та інших ССЗ з використання іАПФ i БРА слід проводити відповідно до клінічних настанов ESC i ESH з 2018 року.9,16 У хворих на COVID-19 з тяжкими симптомами або сепсисом прийняття рішення щодо продовження чи припинення терапії з використанням цих ЛЗ або інших гіпотензивних ЛЗ слід здійснювати в індивідуальному порядку, із врахуванням діючих клінічних настанов.9,16
З моменту появи цієї позиції були опубліковані нові дані. Аналіз включав 6292 хворих на COVID-19 (їх дані були отримані з медичних баз у Ломбардії), до яких було підібрано контрольну групу із загальної популяції. Відсоток пацієнтів, які отримували іАПФ або БРА (та інші гіпотензивні ЛЗ), був більшим серед пацієнтів із COVID-19, ніж у контрольній групі, проте в багатофакторному аналізі не було виявлено зв'язку між застосуванням іАПФ або БРА (та інших гіпотензивних ЛЗ) та ризиком розвитку COVID-19.17 В іншому аналізі було оцінено взаємозв'язок між прийомом гіпотензивних ЛЗ і ризиком інфікування SARS-CoV-2 та його тяжкого перебігу у 12 594 осіб із медичної бази в Нью-Йорку із проведеним тестом на наявність SARS-CoV-2. Не було виявлено, щоб застосування іАПФ/БРА або інших базових гіпотензивних ЛЗ асоціювалося зі значущо більшим ризиком розвитку COVID-19 або більш тяжким перебігом захворювання.18
У цитованому вище аналізі 8910 хворих на COVID-19 з Азії, Європи та США не було виявлено відмінностей щодо частоти АГ у хворих, які померли, та хворих, які вижили.23 У багатофакторному аналізі використання АПФ (але не БРА) та статинів асоціювалося з меншим ризиком смерті під час госпіталізації.23 У 609 хворих на COVID-19, госпіталізованих в Італії, серед яких 311 мали АГ, у багатофакторному аналізі факторами ризику смерті у групі пацієнтів із АГ були клінічний стан на момент поступлення та вік, проте не виявлено зв’язку між ризиком смерті та вживанням іАПФ або БРА.19
Підсумовуючи, у хворих на АГ cлід дотримуватися тих же запобіжних заходів, що й у випадку інших людей того ж віку і з такими ж супутніми захворюваннями.9,16
Позиція ESH була першим документом, у якому оцінено застосування іАПФ i БРА під час пандемії COVID-19. Пізніше 11 інших товариств, зокрема ESC (див. рамка 3), висловили схожу з ESH позицію, щоб у хворих на COVID-19 продовжувати лікування з використанням іАПФ або БРА.9,16
Рамка 3
Артеріальна гіпертензія (АГ) та COVID-19 (відповідно до позиції ESC)21
• Немає даних, які б вказували на те, що АГ як така становить незалежний фактор ризику тяжких ускладнень або смерті в хворих на COVID-19.
• Незважаючи на численні спекуляції, немає жодних доказів того, що попереднє лікування з застосуванням іАПФ або БРА збільшує ризик розвитку COVID-19 або його тяжкого перебігу.
• Лікування АГ слід проводити відповідно до діючих клінічних настанов ESC i ESH; немає необхідності змінювати рекомендації під час пандемії COVID-19.
• Немає необхідності у тому, щоб хворі на АГ, які перебувають на самоізоляції, звертались під час пандемії у лікарню для проведення рутинних контрольних оглядів. Вони можуть проходити періодичний домашній моніторинг артеріального тиску і, якщо необхідно, використовувати відеоконференції або телефонні консультації.
• У пацієнтів із АГ можливий підвищений ризик порушень серцевого ритму через захворювання серця, що спричинене АГ, або частішу наявність гіпокаліємії при тяжкій формі COVID-19.
• У госпіталізованих пацієнтів може бути доцільним тимчасово припинити антигіпертензивну терапію, якщо виникає гіпотензія або гостре пошкодження нирок, які є вторинними до тяжкої COVID-19.
• У пацієнтів, що вже раніше отримували лікування з приводу АГ, та яким необхідна інвазивна вентиляція, парентеральне введення антигіпертензивних ЛЗ показане лише у тому випадку, якщо зберігається тяжка АГ.
Підсумок
Перша публікація про нову вірусну інфекцію з'явилася 21 січня 2020 року.20 Відтоді кількість наукових повідомлень про COVID-19 подвоюється кожні два тижні — 30 квітня у базі PubMed зареєстровано їх майже 7500. Кількість заражених осіб збільшується набагато швидше, ніж кількість публікацій, та все ще багато питань залишаються без відповіді. Це означає, що необхідно постійно відстежувати повідомлення, оскільки позиції та рекомендації експертів — сформульовані на підставі скупих даних, як правило, низької якості, а також клінічного досвіду — можуть швидко змінюватися.
1. Goyal P., Choi J.J., Pinheiro L.C. і співавт.: Clinical characteristics of Covid-19 in New York City. N. Engl. J. Med., 17.04.2020; doi: 10.1056/NEJMc2010419
2. Guan W., Ni Z., Hu Y. і співавт.: Clinical characteristics of coronavirus disease 2019 in China. N. Engl. J. Med., 28.02.2020; doi: 10.1056/NEJMoa2002032
3. Huang C., Wang Y., Li X. і співавт.: Clinical features of patients infected with 2019 novel coronavirus in Wuhan, China. Lancet, 2020; 395: 497–506
4. Pollack C.V., Schreiber D., Goldhaber S.Z. і співавт.: Clinical characteristics, management, and outcomes of patients diagnosed with acute pulmonary embolism in the emergency department: initial report of EMPEROR (Multicenter Emergency Medicine Pulmonary Embolism in the Real World Registry). J. Am. Coll. Cardiol., 2011; 57: 700–706
5. Liu Y., Yang Y., Zhang C. і співавт.: Clinical and biochemical indexes from 2019-nCoV infected patients linked to viral loads and lung injury. Sci. China Life Sci., 2020; 63: 364–374
6. Konstantinides S.V., Meyer G., Becattini C. і співавт.: 2019 ESC guidelines for the diagnosis and management of acute pulmonary embolism developed in collaboration with the European Respiratory Society (ERS). Eur. Respir. J., 2019; 54. https://erj.ersjournals. com/content/54/3/1901647 (доступ: 26.04.2020)
7. Danzi G.B., Loffi M., Galeazzi G., Gherbesi E.: Acute pulmonary embolism and COVID-19 pneumonia: a random association? Eur. Heart J., 30.03.2020, ehaa254. https://doi. org/10.1093/eurheartj/ehaa254 (доступ: 26.04.2020)
8. Xie Y., Wang X., Yang P., Zhang S.: COVID-19 complicated by acute pulmonary embolism. Radiol. Cardiothorac. Imaging, 2020; 2: e200067
9. Kreutz R., Algharably E.A.E., Azizi M. і співавт.: Hypertension, the renin-angiotensin system, and the risk of lower respiratory tract infections and lung injury: implications for COVID-19. Cardiovasc. Res., 2020; cvaa097; https://doi.org/10.1093/cvr/cvaa097https:// doi.org/10.1093/cvr/cvaa097 (доступ: 27.04.2020)
10 Gutiéerrez F., Masiáa M., Mirete C. і співавт.: The influence of age and gender on the population-based incidence of community-acquired pneumonia caused by different microbalmicrobial pathogens. J. Inf., 2006; 53: 166–174
11. Koivula I., Sten M., Makela P.H.: Risk factors for pneumonia in the elderly. Am. J. Med., 1994; 96: 313–320
12. Choi J., Jang J., An Y. і співавт.: Blood pressure and the risk of death from non-cardiovascular diseases: a population-based cohort study of Korean adults. J. Prev. Med. Public Health, 2018; 51: 298–309
13. Cangemi R., Calvieri C., Taliani G. і співавт.: Left atrium dilatation and left ventricular hypertrophy predispose to atrial fibrillation in patients with community-acquired pneumonia. Am. J. Cardiol., 2019; 124: 723–728
14. Rafailidis P.H., Matthaiou D.K., Varbobitis I. і співавт.: Use of ACE inhibitors and risk of community-acquired pneumonia: a review. Eur. J. Clin. Pharmacol., 2008; 64: 565–573
15. Van de Garde E.M., Souverein P.C., van den Bosch J.M. і співавт.: Angiotensin-converting enzyme inhibitor use and pneumonia risk in a general population. Eur. Respir. J., 2006; 27: 1217–1222
16. https://www.eshonline.org/spotlights/esh-statement-on-covid-19/ (доступ: 27.04.2020)
17. Mancia G., Rea F., Ludergnani M. і співавт.: Renin–angiotensin–aldosterone system blockers and the risk of Covid-19. N. Engl. J. Med., 1.05.2020; doi: 10.1056/NEJMoa2006923
18. Reynolds H.R., Adhikari S., Pulgarin C. і співавт.: Renin–angiotensin–aldosterone system inhibitors and risk of Covid-19. N. Engl. J. Med., 1.05.2020; doi: 10.1056/NEJMoa2008975
19. Tedeschi S., Giannella M., Bartoletti M. і співавт.: Clinical impact of renin-angiotensin system inhibitors on in-hospital mortality of patients with hypertension hospitalized for COVID-19. Clin. Infect. Dis., 27.04.2020; doi: 10.1093/cid/ciaa492
20. Dong N., Yang X., Ye L. і співавт.: Genomic and protein structure modelling analysis depicts the origin and infectivity of 2019-nCoV, a new coronavirus which caused a pneumonia outbreak in Wuhan, China. bioRxiv, 22.01.2020. https://www.biorxiv.org/content/10.1101/ 2020.01.20.913368v2 (доступ: 26.04.2020)
21. https://www.escardio.org/Education/COVID-19-and-Cardiology/ESC-COVID-19-Guidance (доступ: 28.04.2020)
22. Wang D., Hu B., Hu C. і співавт.: Clinical characteristics of 138 hospitalized patients with 2019 novel coronavirus-infected pneumonia in Wuhan, China. JAMA, 2020; 323: 1061–1069
23. Mehra M.R., Desai S.S., Kuy S. і співавт.: Cardiovascular disease, drug therapy, and mortality in Covid-19. N. Engl. J. Med., 1.05.2020; doi: 10.1056/NEJMoa2007621