DEFINICIÓN Y ETIOPATOGENIAArriba
El asma es una enfermedad heterogénea que suele caracterizarse por una inflamación crónica de las vías aéreas. Se define por la aparición de síntomas tales como: sibilancias, disnea, sensación de opresión torácica y tos —de presentación e intensidad variable—, así como obstrucción al flujo espiratorio de intensidad variable. La limitación del flujo aéreo está causada por la contracción de la musculatura lisa y por el engrosamiento de la pared bronquial, junto con la aparición de tapones de moco y con el paso de tiempo también por la remodelación de la pared bronquial. El asma se puede clasificar según la etiología en: alérgica (inicio más frecuente en la infancia, a menudo se asocia con otras enfermedades atópicas, a veces existen antecedentes familiares de enfermedades atópicas, resultados generalmente positivos de pruebas cutáneas con alérgenos inhalados, con anticuerpos IgE alérgeno específicos en sangre, habitualmente con eosinofilia en el esputo inducido, y buena respuesta a los glucocorticoides inhalados) y no alérgica (normalmente en adultos, frecuentemente de curso progresivo, resultados negativos de pruebas cutáneas, no se detectan anticuerpos IgE alérgeno específicos en sangre, frecuentemente con peor respuesta a los glucocorticoides inhalados). Además se distinguen otros 3 fenotipos del asma: de inicio tardío, asma con limitación fija al flujo aéreo espiratorio y asma coexistente con obesidad.
En función del tipo de inflamación en las vías respiratorias (establecido sobre la base del tipo de células inflamatorias predominantes en el esputo inducido), se diferencian: asma eosinofílica, asma neutrofílica, y asma paucigranulocítica.
En la práctica clínica diaria tiene un significado básico la clasificación del asma según el grado de control →más adelante.
En la patogenia del asma el papel más importante lo desempeña la subpoblación de linfocitos colaboradores, que producen un perfil característico de citoquinas (IL-4, IL-5, IL-13), que influyen en la producción de IgE por los linfocitos B, así como en el aumento, diferenciación y activación de eosinófilos y mastocitos. En el asma alérgica los mastocitos son activados por alérgenos, mediados por IgE. Una vez activados, liberan los mediadores responsables de la obstrucción bronquial (p. ej. histamina, cisteinil leucotrienos, prostaglandina D2). La patogenia del asma no alérgica no es completamente conocida. Se sospecha un proceso inmunológico inducido por una infección vírica o bacteriana. En casos de asma no alérgica eosinofílica un papel importante lo desempeñan los linfocitos Th2 y las citoquinas por ellos secretadas, así como las células linfoides naturales tipo 2 (ILC2), que producen un perfil de las citoquinas similar al de los linfocitos Th2.
El cuadro histopatológico del asma no alérgica es similar al del asma alérgica. La lesión del epitelio bronquial estimula los procesos de regeneración, cuyo resultado es la remodelación de la pared bronquial, que hace irreversible la obstrucción en casos especialmente graves, debido a cambios estructurales permanentes de la pared bronquial.
Factores que desencadenan ataques y exacerbaciones de asma o que causan su persistencia: alérgenos, infecciones del aparato respiratorio (principalmente virales), humo de tabaco (tabaquismo activo y pasivo), agentes irritantes (p. ej. aerosoles y productos de limpieza de uso doméstico, vapores de pinturas, otras exposiciones ocupacionales), ejercicio físico (manifestaciones se presentan típicamente hasta 20 minutos desde el cese de actividad, pero pueden aparecer durante un esfuerzo prolongado, en general entre los minutos 10 y 20 de ejercicio), emociones fuertes (risa, llanto, enfado) o trastornos mentales (p. ej. ataques de pánico que provocan hiperventilación), contaminación de aire, cambios del tiempo, alimentos y aditivos alimentarios, fármacos (β-bloqueantes, AINE).
Factores que aumentan el riesgo de exacerbaciones del asma (independientemente de la presencia de síntomas): síntomas de asma no controlados (incluido el uso excesivo de agonistas β2 de acción corta; un uso mensual de >1 envase con 200 dosis se asocia a un aumento del riesgo de muerte), falta de uso de glucocorticoides inhalados (falta de adhesión al tratamiento prescrito, técnica de inhalación inadecuada), VEF1 baja (sobre todo si <60 % del valor de referencia, gran mejoría después de inhalar un broncodilatador), problemas psicológicos o socioeconómicos graves, exposición al humo del tabaco o a alérgenos (en personas alérgicas), enfermedades coexistentes (obesidad, rinosinusitis crónica, alergia alimentaria), eosinofilia en el esputo o sangre, embarazo, ≥1 exacerbación grave de asma en los últimos 12 meses, antecedente de intubación o de ingreso para tratamiento del asma en la unidad de cuidados intensivos, FENO aumentado (en enfermos tratados con glucocorticoides inhalados).
Factores de riesgo de persistencia de la obstrucción bronquial: falta del uso de glucocorticoides inhalados, exposición al humo de tabaco o a otras sustancias nocivas (también en el lugar de trabajo), VEF1 inicial baja, producción crónica y excesiva de moco en las vías respiratorias, eosinofilia en el esputo o en la sangre, parto prematuro, bajo peso al nacer, mayor ganancia ponderal en la infancia.
CUADRO CLÍNICO E HISTORIA NATURALArriba
Las manifestaciones tienen un carácter paroxístico e intensidad variable, y pueden no presentarse fuera de los episodios de crisis y las exacerbaciones, incluso durante un tiempo prolongado.
1. Síntomas: disnea paroxística, sobre todo espiratoria (ocasionalmente acompañada de sensación de opresión torácica), que se resuelve espontáneamente o con el tratamiento; respiración sibilante; tos paroxística seca, que puede acompañar a la disnea o puede ser el único síntoma (la llamada variante de asma con tos). La tos aislada en adultos raramente es un síntoma asmático. En el asma alérgica coexisten síntomas de otras enfermedades alérgicas, con mayor frecuencia de rinitis alérgica. Generalmente, durante una crisis o exacerbación de asma se presenta >1 de los síntomas mencionados.
2. Signos: sibilancias dispersas bilaterales (sobre todo espiratorias) y roncus, espiración prolongada (de vez en cuando los signos son audibles solamente durante la espiración forzada); durante las exacerbaciones se observa un aumento de trabajo de los músculos respiratorios accesorios con tiraje intercostal y taquicardia. En las exacerbaciones muy graves los fenómenos auscultatorios pueden no estar presentes (lo que se denomina tórax silencioso).
3. Historia natural: el asma puede manifestarse a cualquier edad. Cuando aparece en adultos con más frecuencia es de origen no alérgico y tiene un curso más grave. La enfermedad es a menudo episódica, con tendencia a la remisión, pero en muchos casos las manifestaciones vuelven a presentarse en la edad adulta. El asma cursa con exacerbaciones que se desarrollan de forma brusca (en minutos u horas) o gradualmente (en muchas horas o días), pudiendo llegar a causar la muerte en casos no tratados. El asma no controlada, de años de evolución, conduce a una obstrucción progresiva e irreversible.
DIAGNÓSTICOArriba
Exploraciones complementarias
1. Espirometría: en la mayoría de los enfermos la espirometría basal es normal. Es característica una obstrucción de intensidad variable (>12 % y 200 ml de diferencia en el VEF1 o CVF entre las siguientes mediciones o como efecto del tratamiento). En la prueba broncodilatadora a menudo se observa una mejoría importante del VEF1 y/o CVF (según GINA >12 % y 200 ml; si se produce una mejoría de >15 % y >400 ml, el diagnóstico es más fiable), y frecuentemente se resuelve la obstrucción (en el asma grave o con remodelación bronquial la obstrucción puede ser irreversible). En la prueba de provocación con metacolina o histamina se observa la hiperreactividad bronquial (considerar en los pacientes con manifestaciones típicas de asma, pero con espirometría normal; un resultado positivo también se presenta a veces en otras patologías bronquiales o en la rinitis alérgica, mientras que un resultado negativo tiene un alto valor para descartar el asma [en pacientes no tratados con glucocorticoides]). En situaciones especiales, el diagnóstico puede confirmarse mediante pruebas de provocación específicas con alérgeno (en asma alérgica se realiza raramente), AAS, factores presentes en el ambiente laboral o con ejercicio físico.
2. Pico del flujo espiratorio (PEF): variabilidad característica diaria media (de 2 semanas) de PEF ([PEFmáx – PEFmín]/PEFmedio) >10 %. Son mediciones usadas para confirmar el diagnóstico, controlar la enfermedad (considerar en casos graves o con baja percepción de los síntomas) e identificar los factores que provocan síntomas (p. ej. factores laborales).
3. Radiografía de tórax: es útil solamente para diferenciar de otras causas de los síntomas; en general es normal, en las exacerbaciones pueden aparecer signos de hiperinsuflación pulmonar y de las complicaciones de la exacerbación (p. ej. neumotórax).
4. Pulsioximetría y gasometría arterial: se deben realizar para valorar la gravedad y controlar el curso de las exacerbaciones →más adelante.
5. Pruebas que detectan la alergia IgE dependiente: pruebas cutáneas, concentración de IgE total y específica: pueden revelar el alérgeno responsable de la alergia en enfermos con asma alérgica (tener en cuenta los datos de la anamnesis).
6. Examen del esputo inducido dirigido a la detección de eosinófilos: en los centros que tienen experiencia puede ser utilizado para ajustar la intensidad de tratamiento en los enfermos con asma moderada o grave.
7. Determinación de la concentración del óxido nítrico en el aire espirado (FENO): se incrementa en casos no tratados de asma con inflamación eosinofílica. En enfermos no tratados con anterioridad, el FENO aumentado (>50 ppb) se relaciona con una buena respuesta al tratamiento con glucocorticoides inhalados, pero los valores menores no permiten identificar a los enfermos en los que se puede renunciar a la administración de glucocorticoides inhalados.
Criterios diagnósticos
El diagnóstico de asma (según GINA) requiere confirmar los síntomas de la enfermedad, así como de la obstrucción bronquial en las pruebas funcionales →tabla 3.9-1. Si las manifestaciones son intensas, los datos de la anamnesis y de la exploración física sugieren asma, y otro diagnóstico es poco probable, se puede iniciar el tratamiento, y posteriormente evaluar su eficacia y realizar un proceso diagnóstico adecuado a los 1-3 meses desde la mejoría del estado de paciente.
Confirmación del diagnóstico en enfermos que ya reciben tratamiento:
1) si los síntomas y la obstrucción bronquial tienen una intensidad variable típica, el diagnóstico es correcto
2) si los síntomas son variables, pero no hay variabilidad del grado de obstrucción → repetir la prueba broncodilatadora después de suspender el broncodilatador o en presencia de síntomas:
a) resultado normal → considerar diagnósticos alternativos
b) VEF1 >70 % del valor de referencia → realizar una prueba de provocación y en caso de obtener un resultado negativo disminuir las dosis del glucocorticoide inhalado en un 25-50 % o suspender LABA y repetir la valoración en 2-4 semanas
c) VEF1<70 % del valor de referencia → aumentar la intensidad del tratamiento (dosis del fármaco controlador →tabla 3.9-2) y repetir la valoración después de 3 meses
3) si los síntomas son leves y la función pulmonar es normal → repetir la prueba broncodilatadora después de suspender el broncodilatador o en presencia de síntomas:
a) resultado normal → considerar diagnósticos alternativos
b) disminuir las dosis del fármaco controlador: si aparecen los síntomas y la función pulmonar empeora → diagnosticar asma; si esto no ocurre → considerar la suspensión del fármaco controlador y una estrecha observación del paciente ≥12 meses
4) si persiste la disnea y una obstrucción bronquial permanente → aumentar la intensidad del tratamiento durante 3 meses y repetir la valoración. En caso de ausencia de mejoría volver al tratamiento anterior y derivar al enfermo a un especialista para continuar el diagnóstico (considerar la coexistencia de asma y EPOC).
Diagnóstico diferencial
EPOC, disfunción de las cuerdas vocales, hiperventilación con ataques de pánico, insuficiencia cardíaca, bronquiectasias, fibrosis quística, infecciones respiratorias. Con menor frecuencia: tumor o cuerpo extraño en las vías respiratorias, estenosis traqueal después de traqueotomía, bronquiolitis obliterante, síndromes hipereosinofílicos, aspergilosis broncopulmonar alérgica, granulomatosis eosinofílica con vasculitis, traqueobroncomalacia. Otras causas de tos crónica →Tos y de disnea paroxística →Disnea.
TRATAMIENTOArriba
Tratamiento crónico
El asma no puede curarse por completo, pero un tratamiento adecuado en general permite alcanzar el control de la enfermedad.
Objetivos del tratamiento:
1) conseguir y mantener el control de los síntomas y una actividad diaria normal (incluyendo la capacidad de realizar actividad física)
2) minimizar el riesgo de exacerbaciones, evitar el deterioro de la función pulmonar y de los efectos indeseables del tratamiento.
La evaluación de la enfermedad, que es fundamental a la hora de tomar decisiones sobre el tratamiento, incluye:
1) El control de los síntomas → según la evaluación durante las últimas 4 semanas se distingue:
a) asma bien controlada: los síntomas aparecen durante el día, ≤2 × semana, sin despertares nocturnos causados por el asma, la necesidad de utilizar el tratamiento sintomático se presenta ≤2 × semana (no incluye el tratamiento preventivo antes de un esfuerzo físico) y sin limitación de las actividades de la vida diaria a causa del asma
b) asma parcialmente controlada: se cumplen 2 o 3 criterios de los anteriormente mencionados
c) asma no controlada: se cumple ≤1 de los criterios anteriormente mencionados.
Para evaluar los síntomas se puede utilizar el Cuestionario de Control del Asma (ACQ), el Test de Control del Asma, o el cuestionario Asthma APGAR. No evaluar el grado de la gravedad de la enfermedad sobre la base de la intensidad de los síntomas antes de iniciar el tratamiento, sino pasados algunos meses con el tratamiento, cuando se establezca el nivel de intensidad (→fig. 3.9-1), necesario para obtener y mantener el control del asma:
a) asma leve: controlada con el tratamiento de grado 1 o 2
b) asma moderada: controlada con el tratamiento de grado 3
c) asma grave: es necesario el tratamiento de grado 4 o 5, o el asma sigue sin controlarse a pesar del tratamiento (→Formas especiales del asma).
2) Los factores de riesgo de las exacerbaciones y la persistencia de obstrucción bronquial →más arriba.
3) La función pulmonar.
4) Los factores relacionados con el tratamiento (técnica de inhalación, seguimiento de las recomendaciones médicas, efectos adversos del tratamiento).
5) La valoración de la actitud del paciente ante la enfermedad y de sus expectativas.
6) La evaluación de la presencia e intensidad de enfermedades concomitantes (rinitis, reflujo gastroesofágico, obesidad, apnea obstructiva del sueño, trastornos de ansiedad y depresivos).
Repetir la evaluación periódicamente y adaptar el tratamiento al estado actual del enfermo.
Es de gran importancia el trabajo en colaboración con el enfermo para que pueda participar en el tratamiento y en la adhesión a las recomendaciones médicas. El grado de participación depende del compromiso del paciente y de sus habilidades cognitivas. El paciente debe participar en la toma de decisiones terapéuticas: esto disminuye la gravedad de los síntomas y el riesgo de exacerbaciones. La educación debe abarcar información sobre:
1) el diagnóstico y la naturaleza de la enfermedad
2) los métodos terapéuticos (incluida la clasificación en fármacos de control y de urgencia, las técnicas de inhalación de fármacos, los efectos adversos del tratamiento)
3) las técnicas de disminución de exposición a los factores que provocan los episodios de asma
4) la vigilancia de los síntomas de asma
5) el manejo de exacerbaciones (incluida la información sobre el momento de solicitar ayuda médica).
En la primera visita el enfermo debe recibir los materiales impresos con toda la información mencionada.
Se debe elaborar un plan escrito de manejo del asma junto con el paciente. Este plan debe incluir, entre otros, la información sobre el tratamiento crónico y el manejo de exacerbaciones. El ámbito de las decisiones tomadas por el mismo enfermo depende de su grado de cooperación y de sus habilidades cognitivas. Para la vigilancia de los síntomas puede ser útil usar un diario. Se debe verificar con regularidad los conocimientos del paciente sobre el asma y las técnicas de inhalación de fármacos. Es necesario tener en cuenta las habilidades de comunicación y cognitivas del paciente (su deterioro se asocia al empeoramiento de los resultados terapéuticos). En estos casos: en primer lugar siempre se debe proporcionar la información más importante, utilizando términos sencillos y hablando lentamente. Es necesario asegurarse de que el paciente entiende lo que se le dice (hay que pedir que repita la información proporcionada), que tenga apoyo de las personas que lo cuiden, y que se sienta cómodo y no tema formular preguntas. Se debe tener en cuenta (sobre todo a la hora de tomar la decisión de aumentar la intensidad del tratamiento) que incluso ~50 % de los pacientes con asma no se adhiere a las recomendaciones relativas al uso de fármacos, de manera tanto periódica como permanente. Los factores asociados a la falta de adhesión a las recomendaciones incluyen, entre otros:
1) problemas con el uso de inhalador (manejo complicado, artritis que dificulta el uso de inhalador, dosificación múltiple durante el día, uso de distintos inhaladores, precio demasiado alto)
2) falta de adhesión no intencionada (falta de comprensión de las recomendaciones, olvidos)
3) falta de adhesión intencionada, cuando el paciente cree que el tratamiento es innecesario, niega el diagnóstico del asma, tiene expectativas terapéuticas erróneas, teme los efectos adversos o no confía en el médico.
Tratamiento farmacológico
El tratamiento farmacológico de asma se basa en el uso crónico de antinflamatorios para controlar el proceso de inflamación bronquial. Los glucocorticoides son los antinflamatorios más comúnmente utilizados y los más eficaces. Adicionalmente, a menudo se utilizan broncodilatadores, que sin embargo tienen carácter complementario y no deben utilizarse nunca sin asociación a un antinflamatorio.
La mayoría de los fármacos básicos se utiliza en inhaladores: lo más importante es educar al paciente sobre la técnica correcta de inhalación y verificar que lo hacen correctamente en cada ocasión.
Fármacos utilizados en el asma:
1) Fármacos que controlan el curso de la enfermedad: glucocorticoides inhalados, agonistas β2 inhalados de acción larga (LABA), anticolinérgicos de acción prolongada (LAMA) y antileucotrienos.
2) Fármacos sintomáticos (administrados según demanda): agonistas β2 inhalados de acción rápida (de acción corta, y formoterol de acción rápida y prolongada), anticolinérgicos inhalados de acción corta. En este grupo se incluyen también los glucocorticoides orales y otros fármacos (→más adelante) utilizados a corto plazo para controlar las exacerbaciones.
3) Métodos adicionales de tratamiento en el asma grave: anticuerpos monoclonales, glucocorticoides orales, antibioticoterapia crónica, termoplastia bronquial.
1. Fármacos controladores del curso de la enfermedad:
1) Glucocorticoides inhalados: los antinflamatorios más eficaces y fármacos de elección para controlar el curso del asma (preparados y dosificación →tabla 3.9-2). Son seguros si se utilizan a largo plazo a dosis bajas o intermedias, y a corto plazo a dosis altas. Presentan efectos adversos principalmente locales: candidiasis orofaríngea, disfonía, a veces tos por irritación. Prevención: enjuagues bucales después de inhalación (en caso de inhaladores de dosis medida [MDI] utilizar cámara espaciadora), o mediante la administración de un glucocorticoide inhalado en forma de profármaco (ciclesonida). Un uso prolongado a dosis altas puede producir efectos adversos generales →Síndrome de Cushing.
PERSPECTIVA CHILENA
La ciclesonida no se encuentra registrada como medicamento en Chile.
2) LABA →tabla 3.9-2. Nunca utilizar sin un glucocorticoide inhalado. Para estar seguro de que el paciente nunca usará un LABA solo, se puede prescribir un inhalador que asocie un LABA con un glucocorticoide (es más cómodo para el enfermo y facilita la adhesión al tratamiento). Los preparados combinados que contienen formoterol (agonista β2 de acción rápida y prolongada) y una baja dosis de glucocorticoide inhalado (budesonida o beclometasona) pueden utilizarse tanto de manera regular (como tratamiento controlador) como a demanda (dosis diaria máx. de formoterol 72 µg en caso de utilizar un preparado combinado con budesonida y 48 µg en caso de utilizar un preparado con beclometasona). Los efectos adversos más frecuentes son: taquicardia, fasciculaciones musculares, e hipopotasemia, que aparecen con menos frecuencia que en el caso de los agonistas β2 de acción corta.
3) LAMA: como fármaco adicional en enfermos que requieren un tratamiento de asma de pasos 4 o 5. Se utiliza el tiotropio (en solución inhalada tipo soft mist inhaler [SMI]) 5 µg 1 × d o preparaciones combinadas de 3 fármacos: glucocorticoide inhalado, LABA y LAMA →tabla 3.9-2.
4) Fármacos antileucotrienos: montelukast a dosis de 10 mg 1 × d VO. Informar al enfermo que debe retirar el fármaco y contactar con el médico en el caso de que se presenten trastornos mentales.
No administrar de rutina metilxantinas en forma de liberación prolongada (p. ej. teofilina), debido a su baja eficacia en el asma y al riesgo elevado de efectos adversos graves →Enfermedad pulmonar obstructiva crónica (EPOC).
2. Fármacos utilizados a demanda (sintomáticos):
Para el uso a demanda, se prefiere un preparado que contiene un glucocorticoide inhalado a dosis baja y formoterol, tanto en los pacientes que lo usan con regularidad como en aquellos que lo utilizan a demanda. En pacientes que reciben de manera crónica un glucocorticoide inhalado con un LABA distinto a formoterol, se debe utilizar a demanda un agonista β2 inhalado de acción corta (solo o en forma de preparado que contiene un glucocorticoide inhalado, si está disponible):
1) Agonistas β2 inhalados de acción rápida y corta (SABA: fenoterol, salbutamol →tabla 3.9-2). Se deben utilizar solamente para controlar los síntomas del asma o para prevenir el broncoespasmo inducido por esfuerzo físico. Producen una resolución rápida de los síntomas, con un inicio de la acción a los pocos minutos y un efecto máximo después de ~15 min, su efecto se mantiene durante 4-6 h. No utilizar SABA en monoterapia, ni siquiera en enfermos con la forma más leve del asma. Efectos adversos más comunes: taquicardia, arritmias, temblor muscular e hipopotasemia.
2) Anticolinérgico de acción corta (ipratropio) →tabla 3.9-2; en exacerbaciones: en enfermos con exacerbaciones graves es beneficioso asociar este fármaco a SABA de manera precoz. El inicio de acción se produce a los ~15 min, y el efecto máximo después de 1-2 h, su efecto se mantiene durante ~6 h. Efectos adversos: sensación esporádica de sequedad o sabor amargo en la boca; la aplicación ocular accidental puede provocar una exacerbación de glaucoma de ángulo estrecho.
3) Glucocorticoides orales: prednisona, prednisolona, metilprednisolona. Administrar para controlar las exacerbaciones del asma. Considerar el tratamiento crónico en los casos más graves del asma no controlada y en los enfermos con exacerbaciones frecuentes a pesar del tratamiento de grado 4, debido a los efectos adversos →Síndrome de Cushing. Tomar la decisión junto con el enfermo, que debería ser informado tanto sobre el riesgo de no tomar la medicación como de los graves efectos no deseados de la terapia. Administrar glucocorticoides VO 1 × d por la mañana, continuando la administración de los glucocorticoides inhalados. La dosis administrada de manera crónica no debería sobrepasar los 7,5 mg/d en conversión a prednisolona. Un tratamiento crónico con glucocorticoides VO requiere la prevención de osteoporosis →Osteoporosis. Todos los enfermos que requieren el tratamiento de grado 5 deben derivarse al centro especializado.
3. Fármacos biológicos. Anticuerpos monoclonales contra:
1) IgE (omalizumab): anticuerpo monoclonal anti-IgE utilizado en asma alérgica grave no controlada, a dosis de 150-600 mg VSc. (dependiendo de la concentración inicial de IgE en suero y de la masa corporal), 1-4 inyecciones cada 2-4 semanas. Se debe evaluar la eficacia después de 4-6 meses.
2) IL-5: en el asma grave, no controlada, a pesar de un tratamiento del grado 4, y con eosinofilia (reslizumab 3 mg/kg iv. 1 × 4 semanas, o mepolizumab 100 mg VSc 1 × 4 semanas).
3) Receptor de la IL-5 (benralizumab): se utiliza en enfermos con asma con eosinofilia, con enfermedad no controlada a pesar de un tratamiento de grado 4 o 5 (30 mg VSc cada 4 semanas, pasados 3 meses cada 8 semanas).
4) Receptor de la IL-4 (dupilumab): se utiliza en enfermos con asma con eosinofilia, no controlada a pesar de la administración de glucocorticoides inhalados a dosis altas con LABA o que requieren la administración de glucocorticoides orales (1.ª dosis 400 o 600 mg, a continuación 200 o 300 mg cada 2 semanas).
PERSPECTIVA CHILENA
En Chile, las guías del Ministerio de Salud para el tratamiento del asma por el sistema de Garantías Explicitas en Salud (GES) están actualizadas solo hasta el 2013 y no incluyen fármacos biológicos. Su uso en el sistema público está restringido a pacientes incluidos en protocolos o con capacidad de comprarlos por sí mismos. En el sistema privado deben ser adquiridos por el paciente.
4. Inmunoterapia alergénica específica: considerar la inmunoterapia específica sublingual con alérgenos (SLIT) en adultos con rinitis alérgica concomitante, alergia a los ácaros del polvo, con VEF1 >70 % del valor de referencia y exacerbaciones a pesar del tratamiento con glucocorticoides inhalados. Este tratamiento es moderadamente eficaz pero seguro (los efectos adversos afectan principalmente a la boca y tracto digestivo). La inmunoterapia subcutánea reduce los síntomas y el uso de fármacos, pero se relaciona con un riesgo de efectos adversos (incluido el shock anafiláctico) y con inconvenientes para el enfermo (tratamiento prolongado, necesidad de someterse a la observación después de recibir la vacuna).
5. Principios de tratamiento farmacológico:
La selección del tratamiento depende de la gravedad de los síntomas (control del asma), la probabilidad de adhesión del paciente a las recomendaciones y de sus preferencias; la intensidad de tratamiento se debe ajustar de manera periódica en función del grado de control del asma →fig. 3.9-1. En las guías GINA se distinguen 5 grados de tratamiento, que reflejan su intensidad, y 2 vías de farmacoterapia, en los que el tratamiento de base consiste en:
1) Un preparado con glucocorticoide inhalado a dosis baja y formoterol, para utilizar solamente a demanda, o tanto con regularidad como a demanda. En este segundo caso, en los grados 4 y 5 se deben seleccionar para el uso regular los preparados con glucocorticoide inhalado a dosis intermedias. Según GINA, es el manejo preferente en la mayoría de los enfermos.
2) Glucocorticoide inhalado administrado de manera regular (en monoterapia o con otros fármacos, con mayor frecuencia LABA): en esta vía el tratamiento únicamente a demanda se utiliza solo en el grado 1, y el enfermo debe tomar un glucocorticoide inhalado cada vez que recibe un SABA a demanda (o tomar a demanda un preparado con SABA y glucocorticoide inhalado, si está disponible).
Las vías de manejo no son excluyentes. No hay contraindicaciones de cambio de manejo de una vía a otra. La toma de un preparado compuesto solamente a demanda (de preferencia en la mayoría de los enfermos con asma leve) disminuye el riesgo de exacerbaciones en un grado similar que el uso regular de glucocorticoide inhalado a dosis bajas, pero se asocia a una peor función pulmonar y a un peor control de los síntomas. Al tomar la decisión sobre el tratamiento es necesario tomar en cuenta la opinión del paciente: si prefiere tomar el fármaco de manera regular para lograr efectos óptimos, o solo a demanda, aceptando peores resultados terapéuticos.
La intensidad de tratamiento inicial en los pacientes no tratados hasta el momento depende de la gravedad de los síntomas:
1) síntomas raros (<2 × mes) → se prefiere un tratamiento a demanda del preparado que contiene un glucocorticoide inhalado a dosis baja y formoterol (de un inhalador); la alternativa es la administración de glucocorticoide inhalado cada vez que se toma un SABA a demanda
2) los síntomas aparecen >2 × mes, pero <2 × d → iniciar el tratamiento a partir del paso 2
3) los síntomas se presentan durante la mayoría de los días, o bien los síntomas nocturnos despiertan al enfermo ≥1 × semana → iniciar a partir del paso 3
4) los síntomas son más intensos o la función pulmonar (evaluada mediante espirometría) está deteriorada → iniciar el tratamiento a partir del paso 4 (en enfermos con los síntomas muy intensos también se puede aplicar un tratamiento a corto plazo con un glucocorticoide oral, como en las exacerbaciones del asma).
En cada grado de tratamiento se deben recomendar los fármacos a demanda para el control rápido de los síntomas. La administración del fármaco a demanda con demasiada frecuencia indica un control inadecuado del asma y la necesidad de intensificar el tratamiento controlador de la enfermedad.
La mayoría de los fármacos controladores permite conseguir mejoría en unos días desde el inicio de tratamiento (1-2 semanas en caso de glucocorticoides inhalados), pero el efecto completo puede observarse después de 3-4 meses, y en caso de asma grave o inadecuadamente tratada durante un tiempo prolongado incluso más tarde. La frecuencia de las visitas depende de la gravedad inicial de la enfermedad y la colaboración del paciente. Normalmente, la visita de control se realiza pasados 1-3 meses desde la primera consulta, a continuación cada 3 meses, y después de una exacerbación en las 2 semanas posteriores. Si no se ha podido controlar la enfermedad, se debe incrementar la intensidad de tratamiento, comprobando previamente la adhesión del paciente a las recomendaciones y la técnica de la toma de fármacos. En los casos en los que no se ha conseguido el control del asma a pesar del tratamiento de paso 3, se deben evaluar otras enfermedades o causas de asma grave (→más adelante).
Si se consigue mantener el control del asma durante ≥3 meses → considerar disminuir la intensidad del tratamiento. Se debe seleccionar el momento idóneo (p. ej. no disminuir la intensidad de tratamiento durante una infección de aparato respiratorio, un viaje, o en embarazadas). Actuación recomendada:
1) Enfermos que utilizan un glucocorticoide inhalado en monoterapia o con un LABA → reducir la dosis del glucocorticoide inhalado un 50 % o modificar la dosificación a 1 × d (en pacientes que utilizan glucocorticoides inhalados a dosis bajas [en monoterapia o con un LABA]). En los enfermos que utilizan un glucocorticoide inhalado con un LABA el abandono del LABA se asocia a un mayor riesgo de exacerbación.
2) Enfermos que utilizan, de forma regular y como tratamiento a demanda, un fármaco que contiene un glucocorticoide inhalado y el formoterol → cambiar a un preparado con una dosis de glucocorticoide inhalado reducida en el 50 %.
3) Enfermos que requieren glucocorticoides orales (además de un glucocorticoide inhalado a dosis alta y LABA) → disminuir gradualmente la dosis del glucocorticoide oral, luego administrar el medicamento cada 2 días (el porcentaje de eosinófilos en el esputo inducido ayuda a ajustar la dosis de glucocorticoide oral).
En pacientes con factores de riesgo de exacerbaciones o con obstrucción bronquial persistente, los eventuales intentos de disminuir la intensidad de tratamiento deben realizarse bajo un control estricto.
A continuación se enumeran los pasos que se pueden considerar, además de la evaluación de los síntomas, para la vigilancia de la enfermedad y el ajuste terapéutico con el fin de mejorar la eficacia de tratamiento:
1) Monitorización del PEF: en los enfermos con asma grave y/o aquellos que tienen dificultad para evaluar la gravedad de los síntomas. Generalmente, el paciente realiza la medición 2 × d, cada vez midiendo PEF 3 veces y anotando el mejor resultado. Existen dispositivos que permiten un registro digital de los resultados (p. ej. con el teléfono). Los pacientes debidamente capacitados pueden utilizar la información sobre la magnitud del PEF para tomar las medidas que prevengan el ulterior desarrollo de la exacerbación (p. ej. modificación de tratamiento o contacto con el médico).
2) Monitorización de FENO, utilizada para ajustar la intensidad de tratamiento del asma alérgica (sobre todo en estudios científicos o en casos seleccionados).
3) Examen del esputo inducido para la detección de eosinófilos (en los centros que tienen experiencia, para ajustar la intensidad de tratamiento en el asma moderado o grave).
Métodos no farmacológicos
1. Aconsejar a todos los enfermos realizar una actividad física sistemática. Informar sobre el riesgo de aparición de los síntomas tras un esfuerzo físico, así como sobre los métodos para su prevención.
2. Durante cada visita recomendar a los enfermos fumadores el abandono del hábito tabáquico. Ofrecer acceso a programas de apoyo o a farmacoterapia. Es necesario también evitar una exposición pasiva al humo de tabaco.
3. En todos los enfermos que trabajan realizar una anamnesis detallada en cuanto a la exposición relacionada con el trabajo y su influencia en los síntomas de la enfermedad.
4. Las técnicas de respiración controlada probablemente disminuyen la gravedad de los síntomas y mejoran la calidad de vida, pero no influyen en los indicadores objetivos; pueden complementar el tratamiento farmacológico.
5. Recomendar a los enfermos una alimentación rica en frutas y verduras, y a los pacientes con obesidad utilizar métodos de reducción de peso.
6. En enfermos adultos que padecen un asma de tipo alérgico no se ha confirmado con claridad la eficacia de los métodos en los que se disminuye la exposición a alérgenos presentes en los interiores. Las intervenciones aisladas no son eficaces. En los enfermos alérgicos al polen se puede recomendar quedarse en casa y evitar la ventilación de las viviendas en los períodos en los que la concentración de polen en el aire sea más alta.
7. Identificar a los enfermos en los que el estrés emocional dificulta el tratamiento del asma, y ayudarlos en la elección de métodos de manejo adecuados (técnicas de relajación, técnicas de respiración controlada, ayuda psicológica). Dirigir a los enfermos con síntomas de ansiedad/depresión a un psicólogo o a un psiquiatra.
8. Recomendar a los enfermos con asma, sobre todo de grado moderado o grave, la vacunación anual contra la gripe.
9. Realizar una anamnesis detallada sobre los fármacos utilizados por el enfermo y su eventual relación con la exacerbación de los síntomas; esto se refiere sobre todo a AINE y β-bloqueantes (incluidos en forma de gotas oftálmicas).
10. Termoplastia bronquial: método experimental utilizado en el marco de ensayos clínicos en los enfermos más graves. La eficacia se mantiene probablemente durante 10 años o más, y el perfil de seguridad es aceptable.
11. Métodos terapéuticos no convencionales. No hay datos de buena calidad que confirmen la eficacia en el tratamiento del asma de métodos como fitoterapia y suplementos dietéticos, homeopatía, acupuntura, ionización de aire (el ozono producido por los ionizadores puede irritar la vía aérea), terapia manual (masaje y quiropraxia), espeleoterapia (permanencia periódica debajo de la tierra, p. ej. en una mina de sal). Si el paciente decide utilizarlos, se le debe recomendar con firmeza que continúe con el tratamiento de eficacia demostrada.
Tratamiento de la exacerbación
1. La actuación dependerá sobre todo de la gravedad de la exacerbación (valoración →fig. 3.9-2).
Si el enfermo sabe evaluar de forma autónoma la intensidad de los síntomas, modificar el tratamiento (según el plan de acción escrito) y la exacerbación no es grave, se debe:
1) aumentar la frecuencia de inhalación del fármaco utilizado a demanda
2) intensificar el tratamiento controlador:
a) si usa solo un glucocorticoide inhalado → aumentar la dosis en 4 veces (considerar aumentarla hasta obtener una dosis alta: máx. 2000 mg/d de beclometasona o una dosis equivalente de otro glucocorticoide inhalado)
b) si usa un glucocorticoide inhalado con formoterol, tanto como tratamiento controlador como según demanda → no modificar la dosificación básica del fármaco y limitarse a administrar dosis adicionales según demanda (dosis máx. diaria de formoterol es de 72 µg en caso de usar un preparado combinado con budesonida y de 48 µg en caso de usar un preparado con beclometasona)
c) si usa un glucocorticoide inhalado a dosis bajas con formoterol como tratamiento controlador y SABA como fármaco a demanda → aumentar 4 veces la dosis del fármaco controlador (no sobrepasar la dosis máx. diaria de formoterol →más arriba)
d) si usa un glucocorticoide inhalado a dosis baja con salmeterol como tratamiento controlador y SABA como fármaco según demanda → utilizar inhalador con dosis más altas del glucocorticoide inhalado y del salmeterol o administrar dosis adicionales del glucocorticoide inhalado desde un inhalador separado.
Si no se produce mejoría en 48 h tras intensificar este tratamiento o la exacerbación es grave (p. ej. PEF <60 % del valor de referencia o del valor máximo para el enfermo), el enfermo debe empezar a usar glucocorticoides VO (→más adelante) y consultar a un médico.
2. Objetivos del tratamiento. Lo más rápidamente posible:
1) eliminar la hipoxemia: a través del tratamiento con oxígeno (mediante una cánula nasal o una mascarilla →Oxigenoterapia para obtener una SpO2 93-95 % [PaO2 ≥60 mm Hg])
2) eliminar la obstrucción bronquial: a través de las inhalaciones de agonistas β2 de acción rápida
3) disminuir el estado inflamatorio y prevenir las recidivas de las exacerbaciones: a través de la administración precoz de glucocorticoides sistémicos.
Tratamiento farmacológico
1. Los SABA son los fármacos de elección: salbutamol o fenoterol inhalado (preparados →tabla 3.9-2).
Dosificación de salbutamol:
1) De pMDI con espaciador: inicialmente 4-10 dosis de 100 µg cada 20 min durante 1 h (hasta 20 dosis en exacerbaciones graves); luego 4-10 dosis cada 3 o 4 h en exacerbaciones leves, 6-10 dosis cada 1-2 h en exacerbaciones moderadas. Las exacerbaciones graves a veces requieren más dosis. Si el enfermo reacciona bien al tratamiento y los síntomas no reaparecen durante unas horas, las dosis adicionales no son necesarias.
2) De nebulizador (idealmente impulsado por oxígeno): puede ser más fácil en exacerbaciones graves, sobre todo al principio del tratamiento; 2,5-5,0 mg cada 15-20 min. En caso de exacerbación grave administrar una nebulización continua 10 mg/h.
En casos excepcionales salbutamol iv. Dosificación: 4 µg/kg en 10 min, luego en perfusión continua 0,1-0,2 µg/kg/min, bajo control de frecuencia cardíaca; o VSc 0,5 mg.
2. Anticolinérgicos de acción corta: ipratropio (preparados →tabla 3.9-2) junto con un SABA en pacientes ambulatorios con exacerbación grave y en todos los pacientes en el departamento de emergencias u hospitalizados con exacerbación moderada o grave:
1) MDI: 4-8 dosis (de 20 µg), repetir cada 15-20 min, en exacerbación grave hasta 20 dosis en 10-20 min
2) nebulizador: 0,5-1 mg, repetir cada 15-20 min o nebulización continua (junto con salbutamol)
3) preparado combinado de fenoterol e ipratropio (1 ml contiene 0,5 mg de fenoterol y 0,25 mg de bromuro de ipratropio): 1-4 ml (20-80 gotas), repetir en caso de necesidad.
3. Glucocorticoides sistémicos: utilizar en el tratamiento de todas las exacerbaciones del asma (excepto las más leves), en general durante 5-7 días. Si es posible, el fármaco se debe administrar dentro de la primera hora tras el diagnóstico de la exacerbación. Los efectos clínicos son visibles después de 4-6 h. La administración VO es tan eficaz como la iv., bajo la condición de que el enfermo pueda tomar comprimidos y no los vomite (si eso ocurre, administrar la dosis equivalente de glucocorticoides iv.). Si el tratamiento con glucocorticoides VO dura <3 semanas, no hay que reducir la dosis gradualmente, pero de forma precoz añadir el glucocorticoide inhalado. Dosificación: VO 30-50 mg de prednisona, prednisolona o metilprednisolona hasta una mejoría satisfactoria; metilprednisolona iv.: dosificación más arriba o hidrocortisona iv. (dosis inicial 100-200 mg, posteriormente 50-100 mg cada 6 h).
4. Otros fármacos:
1) Sulfato de magnesio iv.: considerar su uso en exacerbación grave, cuando los fármacos anteriormente mencionados no logran el efecto deseado. Dosificación: 1,0-2,0 g durante 20 min. La nebulización de salbutamol con una solución isotónica del sulfato de magnesio es más eficaz que con NaCl al 0,9 %.
2) Antibióticos solamente en caso de una infección respiratoria bacteriana.
3) No administrar derivados de teofilina.
Tratamiento de insuficiencia respiratoria →Insuficiencia respiratoria aguda
Vigilancia del tratamiento
Evaluar de forma continua o frecuente:
1) la gravedad de los síntomas y signos, y la respuesta al tratamiento
2) la función pulmonar (PEF, eventualmente o VEF1; si es posible, evaluar antes del inicio del tratamiento, pero sin retrasarlo, luego repetir esta medición de forma seriada); en enfermos en estado grave no realizar las pruebas de función pulmonar; repetir la determinación del PEF después de 1 h de tratamiento; en caso de empeoramiento evaluar la necesidad de tratamiento en la UCI; la mejoría del PEF hasta unos valores >60-80 % del valor máx. normalmente indica una buena respuesta al tratamiento
3) frecuencia respiratoria
4) pulso
5) SpO2 (pulsioximetría); en enfermos graves, con factores de riesgo de hipercapnia (p. ej. con EPOC concomitante) o con SpO2 <90 % → gasometría
6) radiografía o ecografía de tórax: no realizar de forma rutinaria; están indicadas si se sospechan complicaciones (neumotórax, neumonía) y en el diagnóstico diferencial (p. ej. de insuficiencia cardíaca).
Requieren una vigilancia estricta los enfermos con riesgo alto de mortalidad por asma, es decir, aquellos en los cuales se observa ≥1 de los siguientes factores:
1) han tenido exacerbación de asma con riesgo vital y han requerido ventilación mecánica
2) en el último año estuvieron hospitalizados o necesitaron una intervención médica urgente por motivo del asma
3) utilizan o recientemente han dejado el tratamiento con glucocorticoides VO
4) no utilizan actualmente glucocorticoides inhalados
5) necesitan inhalaciones frecuentes de agonistas β2 según demanda
6) padecen un trastorno mental, tienen antecedentes de problemas psicosociales o no siguen las recomendaciones.
Actuación después de exacerbación
1. Criterios que deben cumplirse antes del alta hospitalaria tras un tratamiento inicial en el servicio de urgencias:
1) reducción de la intensidad de los síntomas: el enfermo no requiere dosis adicionales de SABA, la disnea no le dificulta el decúbito
2) función pulmonar (PEF o VEF1) >60 % del valor de referencia/valor máx.; si es de un 40-60 % del valor de referencia/valor máx. → evaluar los factores de riesgo de exacerbación grave y la disponibilidad de los cuidados a domicilio
3) SpO2 normal.
2. Antes del alta hospitalaria:
1) confirmar si existen factores de riesgo que puedan haber causado la exacerbación y, en caso de necesidad, recomendar un manejo adecuado
2) verificar si el enfermo sabe manejar el inhalador y si sabe cómo administrar los medicamentos
3) evaluar y, en caso de necesidad, modificar el plan de manejo en el asma
4) aumentar la dosis del glucocorticoide inhalado (en general para 2-4 semanas), y empezar a utilizar un glucocorticoide inhalado en enfermos no tratados de forma regular hasta ahora
5) establecer la fecha de la cita de control (en general después de 2-7 días).
VIGILANCIAArriba
La evaluación de la enfermedad (como antes del inicio de tratamiento →más arriba) y de los resultados del tratamiento se debe repetir en cada visita médica. La función pulmonar (mediante prueba espirométrica broncodilatadora) debe evaluarse antes de iniciar el tratamiento, pasados 3-6 meses de tratamiento antinflamatorio, después periódicamente (≥1 × 2 años, con mayor frecuencia en enfermos con exacerbaciones recurrentes y con factores de riesgo de obstrucción establecida) y en caso de necesidad. Prestar atención a las preocupaciones y dudas del paciente. En los enfermos con asma grave o con baja percepción de los síntomas recomendar la vigilancia del PEF. Puede resultar útil apuntar la presencia y las exacerbaciones de los síntomas, la necesidad del uso del tratamiento sintomático y la confirmación del uso de fármacos de uso regular (puede ser en un programa en un dispositivo electrónico personal).
SITUACIONES ESPECIALESArriba
Embarazo
1. Durante el embarazo puede empeorar o mejorar el control del asma. El asma mal controlada y la hipoxemia del feto suponen un mayor peligro para el feto que los efectos adversos de los fármacos. La educación de la paciente es muy importante.
2. Las reglas del tratamiento crónico y del tratamiento de las exacerbaciones son similares a las reglas generales vigentes. Los fármacos preferidos son los glucocorticoides inhalados (en caso necesario también orales) y agonistas β2 inhalados de acción corta (los datos acerca de la seguridad de LABA son limitados).
3. Si durante las 48 h precedentes al parto la paciente se administró una dosis total alta de agonistas β2, se debe controlar la glucemia del neonato durante las primeras 24 h de vida.
4. Las mujeres que durante >2 semanas antes del parto habían estado recibiendo prednisona a dosis >7,5 mg/d, durante el parto deberían recibir hidrocortisona iv. a dosis de 100 mg cada 6-8 h.
5. Durante el período de lactancia se pueden usar todos los fármacos antiasmáticos.
Cirugías
1. Antes de la cirugía se debe realizar una prueba de la función pulmonar, idealmente con la antelación adecuada para intensificar el tratamiento de asma (p. ej. tratamiento corto con glucocorticoides VO) en caso de necesidad.
2. Los enfermos sometidos a cirugía que asocien un gran estrés quirúrgico (no incluye procedimientos pequeños y cirugías con anestesia local) y que durante ≥3 semanas en los últimos 6 meses tomaron glucocorticoides sistémicos a dosis equivalente a ≥20 mg/d de prednisona, deberían recibir hidrocortisona iv. 50-100 mg cada 8 h (la primera dosis antes de la cirugía) en el período perioperatorio (hasta 24 h después de la cirugía).
3. Recordar la posibilidad de alergia a anestésicos.
Asma en enfermos de edad avanzada
A pesar de tener una función pulmonar más deteriorada, los enfermos tienen una peor percepción de los síntomas. Los principios del tratamiento no se diferencian de los utilizados en enfermos más jóvenes. Prestar una atención especial a:
1) la técnica correcta de uso de los inhaladores (incluidas las eventuales alteraciones de la capacidad física y/o de las funciones cognitivas)
2) los factores económicos o los temores a posibles efectos adversos, lo que dificulta la adquisición y toma de los fármacos
3) el listado completo de los fármacos tomados por el enfermo (para verificar la eventual relación con el empeoramiento del control del asma y la valoración de las interacciones de los medicamentos)
4) la aplicación de esquemas de tratamiento simples (evitar el uso de diferentes tipos de inhaladores)
5) los intentos de abandonar el hábito tabáquico.
Actuación durante la pandemia de COVID-19
Asegurar al enfermo que no debe retirar los fármacos tomados, sobre todo los glucocorticoides inhalados. Los principios del tratamiento crónico no han cambiado durante la pandemia de COVID-19. En enfermos con sospecha o confirmación de infección por COVID-19, dentro de lo posible, se debe evitar el uso de la nebulización y la realización de espirometría.
Formas especiales del asma
1. Asma difícil de tratar y asma grave. El asma difícil de tratar es el asma que no se controla con un tratamiento de pasos 4 o 5, o que requiere dicho tratamiento para preservar un buen control de los síntomas y reducir el riesgo de exacerbaciones. El asma grave (subcategoría de asma difícil de tratar) es un asma que sigue sin controlarse a pesar del tratamiento optimizado de máxima intensidad, y a pesar de que estén controlados los factores concomitantes que puedan agravar la enfermedad, o que se intensifica tras la reducción de dosis altas de fármacos.
El manejo abarca:
1) la confirmación del diagnóstico (→Diagnóstico diferencial): pueden ser útiles p. ej. las pruebas:
a) de imagen (radiografía de tórax, TC de alta resolución, TC de senos paranasales, ecocardiografía)
b) de laboratorio (hemograma, proteína C-reactiva, IgG, IgA, IgM, IgE, anticuerpos precipitantes contra Aspergillus, anticuerpos contra el citoplasma de neutrófilos, NT-proBNP)
c) dirigidas hacia las enfermedades alérgicas (pruebas cutáneas, IgE específica en suero)
d) funcionales del aparato respiratorio (TLCO)
e) broncoscopia (en enfermos seleccionados)
2) la evaluación de los factores que deterioran el curso de la enfermedad:
a) adhesión a las recomendaciones médicas (incluidas las técnicas de uso del inhalador)
b) enfermedades concomitantes (rinosinusitis nasal, reflujo gastroesofágico, obesidad y apnea obstructiva del sueño)
c) factores de riesgo modificables y factores desencadenantes de los síntomas (tabaquismo, exposición ambiental, contacto con alérgenos, uso de fármacos [β-bloqueantes, AINE])
d) abuso de SABA
e) efectos adversos de fármacos
f) ansiedad, empeoramiento del estado de ánimo, problemas sociales
g) otros factores que dificultan el control del asma (→Definición y etiopatogenia)
3) la optimización del tratamiento:
a) educación del enfermo y elaboración de un plan de actuación en asma
b) optimización del tratamiento farmacológico (considerar añadir fármacos adicionales, como p. ej. LABA, LAMA, ARLT, si no han sido utilizados hasta el momento)
c) minimización de la exposición a los factores de riesgo modificables (recomendar firmemente el abandono completo del hábito tabáquico a los fumadores [puede considerarse la determinación de la concentración de la cotinina en orina o saliva] y la evitación de la exposición pasiva al humo de tabaco)
d) consideración de los métodos no farmacológicos adicionales (p. ej. actividad física, reducción de peso corporal, vacunación contra la gripe, técnicas de limpieza del moco de las vías aéreas)
e) tratamiento adecuado de enfermedades concomitantes
f) consideración de intentos del tratamiento con dosis altas de glucocorticoides inhalados, si no se han administrado antes.
Diagnosticar asma grave, si:
1) a los 3-6 meses de la optimización del tratamiento, el asma sigue sin controlar, o
2) con los intentos de reducir la intensidad de tratamiento (en primer lugar, se reduce la dosis de glucocorticoide oral o este se retira, y a continuación se retiran todos los fármacos adicionales), se pierde el control del asma. En este caso, se debe restablecer el tratamiento anterior.
Actuación posterior:
1) repetir los pasos descritos más arriba
2) considerar la introducción del manejo multidisciplinar
3) evaluar la presencia de inflamación de tipo 2 ("residual"), resistente al tratamiento, durante el uso de dosis altas de glucocorticoide inhalado, o de la dosis más baja posible de glucocorticoide oral. Esta inflamación está presente, si se cumple ≥1 de los siguientes criterios:
a) recuento de eosinófilos en la sangre periférica ≥150/µl
b) recuento de eosinófilos en el esputo ≥2 %
c) FENO ≥20 ppb
d) rasgos clínicos del empeoramiento del asma tras contacto con un alérgeno.
Si el enfermo no cumple con los criterios de inflamación de tipo 2:
1) considerar un diagnóstico adicional: examen del esputo inducido, TC de alta resolución, broncoscopia
2) optimizar el tratamiento adicional (evaluar la introducción de un anticolinérgico de acción prolongada, un antibiótico macrólido, glucocorticoide inhalado a dosis bajas, y retirar fármacos que no causan mejoría)
3) evaluar la termoplastia bronquial.
Si el enfermo cumple con los criterios de inflamación de tipo 2:
1) evaluar de manera objetiva la adhesión a las recomendaciones, p. ej. a partir de la información sobre la compra de fármacos prescritos, o mediante inhalador con contador de dosis electrónico, o determinando la concentración sanguínea de prednisona
2) considerar el aumento de dosis de glucocorticoides inhalados, por 3-6 meses a modo de prueba
3) considerar el tratamiento biológico; utilizar durante 4 meses, y a continuación evaluar la respuesta. Si la eficacia es incierta, se debe prolongar el período de prueba unos 6-12 meses. En caso de falta de respuesta al tratamiento biológico, hay que suspenderlo y eventualmente considerar la administración de otro fármaco biológico.
No utilizar nebulizadores para administrar fármacos de manera rutinaria. En centros con experiencia en la evaluación del recuento de eosinófilos en esputo, este método es útil a la hora de ajustar el tratamiento.
2. Asma premenstrual: progresión de los síntomas y reducción del PEF 2-5 días antes de la menstruación que mejora con el inicio de la menstruación. Puede ser útil el uso de antileucotrienos y anticonceptivos orales.
3. La enfermedad respiratoria exacerbada por la aspirina (EREA; en inglés NSAID-Exacerbated Respiratory Disease, NERD) es un tipo característico de asma que aparece en un 5-10 % de los adultos asmáticos. Empieza con una rinorrea intensa, lleva a la sinusitis y luego al asma. Son frecuentes los pólipos nasales y la eosinofilia. Se caracteriza por aparición de ataques de asma, frecuentemente acompañados de rinorrea, irritación conjuntival y eritrodermia de cabeza y cuello que duran desde más de diez minutos hasta unas horas después de la toma del ácido acetilsalicílico o de otro AINE (los enfermos pueden tomar paracetamol [en dosis única <1 g], salicilamida, celecoxib). A pesar de evitar el uso de AAS y otros AINE, el asma se mantiene y con frecuencia tiene un curso grave. El único método objetivo para establecer este diagnóstico es la prueba de provocación con AAS que se realiza solamente en un centro especializado en el que también se puede realizar la desensibilización. Una administración constante de AAS de varios meses de duración (después de la desensibilización) disminuye los síntomas sinonasales y mejora el control del asma.
4. Asma relacionada con el trabajo →Asma relacionada con el trabajo.
5. Broncoespasmo provocado por esfuerzo físico (denominado asma por ejercicio). El broncoespasmo aparece a consecuencia de la hiperreactividad bronquial, generalmente 5-10 min después de terminar el ejercicio físico y cede espontáneamente en 30-45 min (frecuentemente en enfermos sin un buen control del asma). El diagnóstico se confirma si se produce la disminución del VEF1 ≥10 % durante la prueba de ejercicio o un test de reemplazo (prueba de hiperventilación, prueba de provocación bronquial con solución de NaCl al 4,5 % o con manitol). Se debe recomendar al enfermo el uso de un agonista β2 inhalado de acción rápida (salbutamol o fenoterol) 15 min antes del ejercicio. En personas en las que a pesar de eso el ejercicio sigue provocando síntomas y en personas que todos los días tienen que tomar el agonista β2 de acción corta → recomendar el uso de un glucocorticoide inhalado de forma regular (eventualmente + LABA) y/o un fármaco antileucotrieno o antihistamínico (en enfermos con alergia). La frecuencia de aparición y el aumento del broncoespasmo inducido por ejercicio disminuyen con el entrenamiento y un calentamiento adecuado. Las personas que realizan ejercicios a temperaturas bajas pueden utilizar mascarillas que calientan el aire inspirado.
6. Coexistencia del asma y de la EPOC →Enfermedad pulmonar obstructiva crónica (EPOC).
TABLAS Y FIGURAS
Criterios diagnósticos del asma en adultos, adolescentes y niños de 6-11 años
|
El asma es una enfermedad heterogénea que habitualmente se caracteriza por una inflamación crónica de las vías aéreas. Cursa con síntomas tales como sibilancias, disnea, sensación de opresión torácica, y con tos de frecuencia e intensidad variable en función de la mayor o menor dificultad del flujo espiratorio del aire a su paso por las vías respiratorias.
|
|
Rasgo diagnóstico
|
Criterios que indican el diagnóstico de asma
|
|
1. Presencia de síntomas variables del sistema respiratorio
|
|
Sibilancias, disnea, opresión torácica y tos
(la manera de describir estos síntomas puede ser distinta dependiendo del origen y edad, p. ej. los niños pueden describir disnea como "respiración difícil")
|
– Habitualmente >1 tipo de síntomas de las vías respiratorias (en adultos, la tos como único síntoma raramente está causado por el asma)
– La presencia y la intensidad de los síntomas varía con el tiempo
– Los síntomas frecuentemente se intensifican por la noche o al despertar
– Los síntomas se desencadenan habitualmente por un esfuerzo físico, la risa, alérgenos, aire frío
– Con frecuencia los síntomas aparecen o se intensifican en el contexto de infecciones víricas
|
|
2. Confirmación del grado de variabilidad del flujo espiratorio por las vías respiratorias
|
|
2.1 confirmación de la limitación del flujo espiratorio por las vías respiratorias
y
2.2. confirmación de la existencia de una variabilidad excesiva de la función pulmonar (≥1 de las pruebas mencionadas más adelante)
|
Al menos 1 vez durante el proceso diagnóstico, en caso de confirmar disminución de VEF1, es necesario confirmar la disminución de VEF1/CVF (normal: >0,75-0,80 en adultos y >0,90 en niños)
El diagnóstico es más seguro cuanto más variabilidad haya y cuanto con más frecuencia se diagnostique. Si el resultado inicial es negativo, se puede repetir la prueba durante la presencia de los síntomas o a primeras horas de la mañana
|
|
Resultado positivo de la prueba broncodilatadora (la probabilidad de obtener un resultado positivo es mayor si el paciente abandona los broncodilatadores antes de la prueba: SABA ≥4 h antes, LABA utilizado 2 × d ≥15 h antes, LABA utilizado 1 × d ≥36 h antes)
|
Adultos: aumento de VEF1 en >12 % y >200 ml en comparación con el valor inicial, 10-15 min después de la inhalación de 200-400 µg de salbutamol (el diagnóstico es más fiable si la mejoría de VEF1 es >15 % y >400 ml)
Niños: aumento de VEF1 de >12 % del valor de referencia
|
|
Variabilidad excesiva de PEF en las mediciones realizadas 2 × d durante 2 semanasª
|
Adultos: variabilidad diaria media de PEF >10 % a
Niños: variabilidad diaria media de PEF >13 % a
|
|
Mejoría importante de la función pulmonar, pasadas 4 semanas del tratamiento antinflamatorio
|
Adultos: aumento del VEF1 en >12 % y >200 ml en comparación con el valor inicial (o PEF en >20 % b), pasadas 4 semanas de inicio de tratamiento sin evidenciar infección de las vías respiratorias durante este período
|
|
Resultado positivo de la prueba de provocación bronquial
|
Adultos: disminución del VEF1 en >10 % y >200 ml en comparación con el valor inicial
Niños: disminución del VEF1 en >12 % del valor de referencia o PEF en >15 %
|
|
Resultado positivo de la prueba inhalatoria de provocación bronquial (habitualmente se realiza solo en adultos)
|
Disminución del VEF1 en ≥20 % en comparación con el valor inicial después de la inhalación de la dosis estándar de metacolina o ≥15 % en la prueba de hiperventilación estándar, con el uso de solución hipertónica de NaCl o de manitol
|
|
Variabilidad excesiva de la función pulmonar en las siguientes visitas (criterio sensible, pero poco específico)
|
Adultos: variabilidad del VEF1 >12 % y >200 ml en mediciones efectuadas durante las visitas consecutivas, sin evidenciar infección de vías respiratorias durante este período
Niños: variabilidad del VEF1 >12 % o variabilidad del PEF >15 % b en mediciones efectuadas durante las visitas consecutivas (también en las exploraciones que se hacen durante la infección de las vías respiratorias)
|
|
a La variabilidad diaria del PEF se calcula sobre la base de las mediciones PEF 2 × d durante el día (el valor máximo de las 24 h reducido en el valor mínimo de las 24 h y dividido por el valor medio de las 24 h) e indica el valor medio de mediciones de la semana.
b Para mediciones del PEF se debería utilizar el mismo medidor de flujo espiratorio máximo, ya que los resultados de las mediciones con medidores diferentes pueden variar hasta en un 20 %. La reversibilidad de la obstrucción (mejoría después de la inhalación del fármaco broncodilatador) puede anularse durante una exacerbación grave de asma y durante una infección viral de las vías respiratorias. Si el resultado de la prueba broncodilatadora durante la primera visita es negativo, la conducta posterior dependerá de la disponibilidad de otras exploraciones y de la necesidad de tratamiento. Si es necesario empezar el tratamiento de forma urgente, es posible realizarlo y planificar las pruebas diagnósticas en las próximas semanas. Hay que considerar otras enfermedades que puedan parecerse al asma (→texto) y confirmar el diagnóstico del asma lo antes posible.
Diagnóstico de asma en enfermos ya tratados →texto.
VEF1 — volumen espiratorio forzado en el primer segundo, LABA — agonista β2 de acción prolongada (inhalado), PEF — pico del flujo espiratorio (el valor máximo de las 3 mediciones), SABA — agonista β2 de acción corta (inhalado)
A partir de: Global Strategy for Asthma Management and Prevention, 2022; Initiative for Asthma (GINA); www.ginasthma.org; modificado
|
Fármacos inhalados utilizados en el tratamiento del asma en adultos
|
Fármaco
|
Forma
|
Dosificación
|
|
Agonistas β2 inhalados de acción corta (SABA)
|
|
Fenoterol
|
MDI 100 µg
|
Según demanda: 1-2 dosis
|
|
Salbutamol
|
MDI 100 µg
DPI 100 y 200 µg
Solución para nebulización 1 y 2 mg/ml
|
Según demanda: 1-2 dosis
Dosificación en la exacerbación →texto
|
|
Agonistas β2 inhalados de acción prolongada (LABA)
|
|
Formoterol (fumarato dihidrato)
|
MDI 12 μg
DPI 4,5, 9 y 12 μg
|
1-2 dosis 2 × d (máx. 54 o 72 μg/d →texto)
|
|
Salmeterol
|
MDI 25 µg
DPI 50 µg
|
1-2 dosis 2 × d (máx. 200 μg/d)
|
|
Glucocorticoides inhalados
|
|
Beclometasona
|
MDI 100 y 200 µg
|
50-100 μg 2 × d (dosis baja)
>100-200 μg 2 × d (dosis media)
>200 μg 2 × d (dosis alta)
|
|
Budesonida
|
MDI 200 μg
DPI 100, 200 y 400 μg
Susp. para nebulización 0,125, 0,25 y 0,5 mg/ml
|
100-200 μg 2 × d (dosis baja)
>200-400 μg 2 × d (dosis media)
>400 μg 2 × d (dosis alta)
|
|
Ciclesonida
|
MDI 80 y 160 µg
|
80-160 μg 1 × d (dosis baja)
>160-320 μg 1 × d (dosis media)
>320 μg 1 × d (dosis alta)
|
|
Fluticasona (propionato)
|
MDI 50, 125 y 250 µg
DPI 50, 100, 125, 250 y 500 μg
Susp. para nebulización 0,25 y 1 mg/ml
|
50-125 μg 2 × d (dosis baja)
>125-250 μg 2 × d (dosis media)
>250 μg 2 × d (dosis alta)
|
|
Fluticasona (furoato)
|
Disponible solamente en forma de preparados combinados
|
100 μg 1 × d (dosis baja-media)
200 μg 1 × d (dosis alta)
|
|
Mometasona
|
DPI 400 µg
|
110-220 µg/d (dosis baja)
>220-440 µg/d (dosis media)
>440 µg/d (dosis alta)
|
|
Preparados combinados LABA + glucocorticoides en un inhalador
|
|
Formoterol + budesonida
|
DPI 4,5 µg/80 µg, 4,5 µg/160 µg, 9 µg/320 µg
MDI 4,5 μg/160 μg
|
1-2 dosis 2 × d
|
|
Salmeterol + fluticasona (propionato)
|
MDI 25 μg/50, 125 o 250 μg
DPI 50 μg/100, 250 o 500 μg
|
1-2 dosis 2 × d
|
|
Formoterol + beclometasona
|
MDI 6 μg/100 μg, 6 μg/200 μg
DPI 6 µg/100 µg
|
1-2 dosis 2 × d
|
|
Vilanterol + fluticasona (furoato)
|
DPI 22 μg/92 μg y 22 μg/184 μg
|
1 dosis 1 × d
|
|
Fármacos anticolinérgicos de acción corta (SAMA)
|
|
Ipratropio
|
MDI 20 µg
Solución para nebulización (0,25 mg/ml)
|
En exacerbaciones →texto
|
|
Fármacos anticolinérgicos de acción prolongada (LAMA)
|
|
Tiotropio
|
SMI 2,5 µg
|
2 dosis 1 × d
|
|
Preparados combinados SAMA + SABA en un inhalador
|
|
Ipratropio + fenoterol
|
MDI 20 μg/50 μg
Solución para nebulización
|
En exacerbaciones →texto
|
|
Preparados combinados LABA + LAMA + glucocorticoides en un inhalador
|
|
Formoterol + glicopirronio + beclometasona
|
MDI 6 µg/10 µg/100 µg
|
2 dosis 2 × d
|
|
Indacaterol + glicopirronio + mometasona
|
DPI 150 μg/50 μg/160 μg
|
1 dosis 1 × d
|
|
DPI — inhalador de polvo seco, MDI — inhalador de dosis medida, SMI — inhalador de niebla fina
|

Fig. 3.9-1. Tratamiento de control del asma crónica en adultos (a partir de la GINA 2023, modificado)
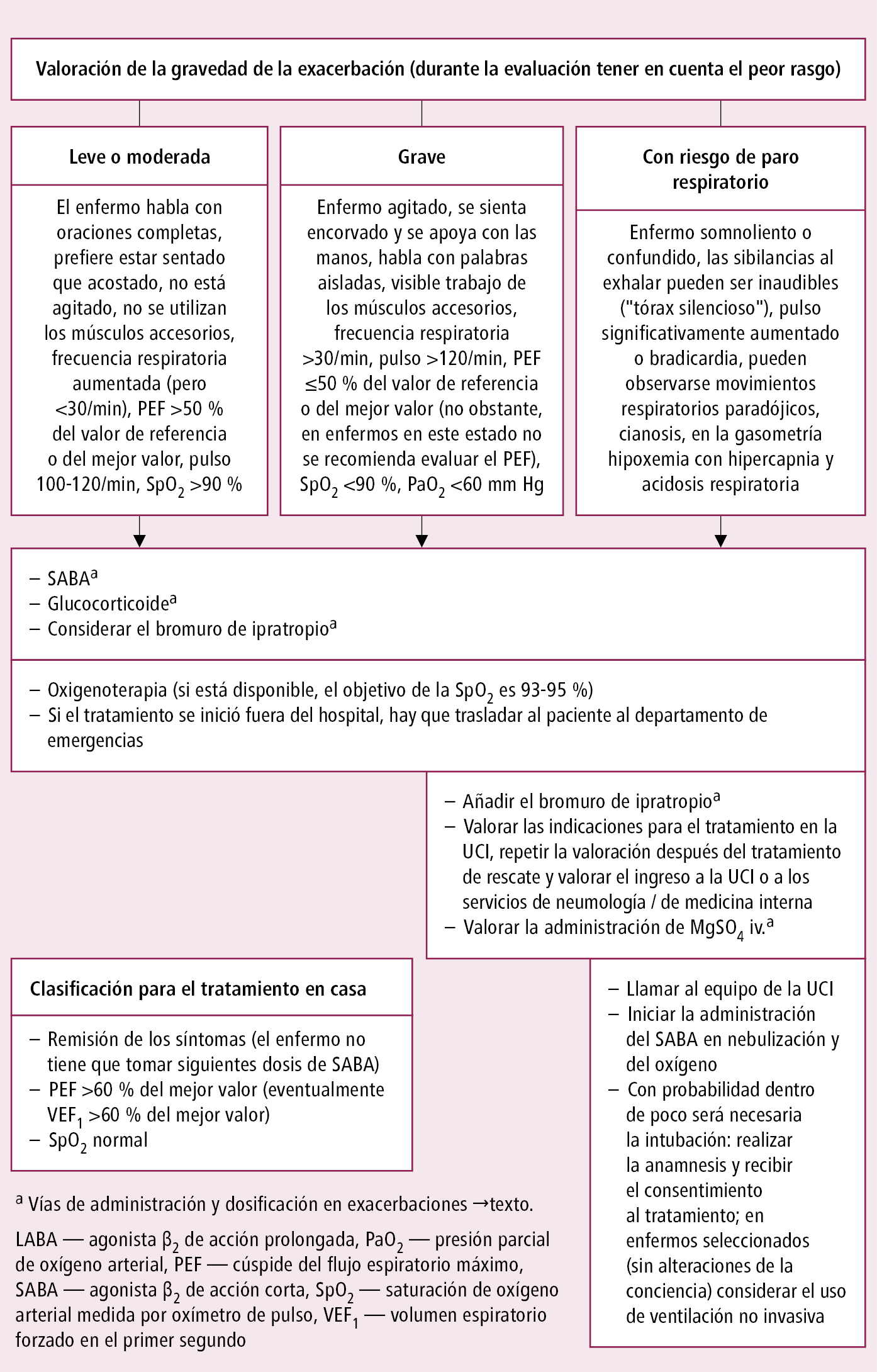
Fig. 3.9-2. Algoritmo de actuación en exacerbaciones del asma, en función de la gravedad (a partir de las guías de la GINA, modificado)
 Español
Español
 English
English
 українська
українська






